Chemická Kinetika
Chemická Kinetika
můžete být obeznámeni s acidobazické titrace, že použití fenolftaleinu jako endpoint indikátor. Možná jste si však nevšimli, co se stane, když řešeníkterý obsahuje fenolftalein v přítomnosti přebytečné báze, může stát několik minut. Ačkoli roztok má zpočátku růžovou barvu, postupně se stává bezbarvý jakofenolftalein reaguje s OH-iontem v silně zásaditém roztoku.
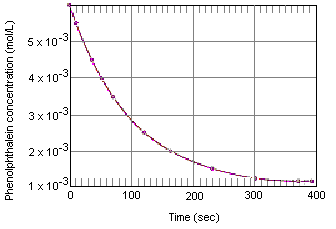
níže uvedená tabulka ukazuje, co se stane s koncentrací fenolftaleininu v roztoku, který byl zpočátku 0,005 M ve fenolftaleinu a 0,61 M v OH-iontu. Jak vidíte, když jsou tato data vykreslena v grafu níže, fenolftaleinkoncentrace klesá o faktor 10 po dobu asi čtyř minut.
Experimental Data for the Reaction Between Phenolphthalein and ExcessBase
| Concentration of Phenolphthalein (M) |
Time (s) | |
| 0.0050 | 0.0 | |
| 0.0045 | 10.5 | |
| 0.0040 | 22.3 | |
| 0.0035 | 35.7 | |
| 0.0030 | 51.1 | |
| 0.0025 | 69.3 | |
| 0.0020 | 91.6 | |
| 0.0015 | 120.4 | |
| 0.0010 | 160.9 | |
| 0.00050 | 230.3 | |
| 0.00025 | 299.6 | |
| 0.00015 | 350.7 | |
| 0.00010 | 391.2 |
Experimenty jako ten, který nám dal údajů ve výše uvedené tabulce areclassified jako měření z chemické kinetiky (z řeckého kmene znamená „přestěhování“). Jedním z cílů těchto experimentů je popsat rychlost reakcerychlost, s jakou reaktantyjsou transformovány na produkty reakce.
termín rychlost se často používá k popisu změny v množstvíkterá se vyskytuje za jednotku času. Míra inflace je například změna vprůměrné náklady na sběr standardních položek za rok. Rychlost, s jakou objektcestuje prostorem, je vzdálenost ujetá za jednotku času, například míle za hodinu nebokilometry za sekundu. V chemické kinetice je ujetá vzdálenost změnou vkoncentrace jedné ze složek reakce. Rychlost reakce prosazování změny v koncentraci jednoho z reaktantů,![]() (X)
(X)![]() , který se vyskytuje v průběhu daného období
, který se vyskytuje v průběhu daného období![]() t.
t.
![]()
Praxe Problém 1:
Použít data ve výše uvedené tabulce pro výpočet sazby na fenolftalein, který reaguje s OH – iontů během každé z následujících období:
(a) Během prvního časového intervalu, kdy fenolftalein koncentrace padá z 0.0050 M 0.0045 M.
(b) Během druhého intervalu, kdy koncentrace klesne z 0.0045 M 0.0040 M.
(c) Během třetího intervalu, kdy koncentrace klesne z 0.0040 M 0.0035 M.
Klikněte zde, aby se zkontrolujte, zda vaše odpověď na Praxi Problém 1.
kliknutím sem zobrazíte řešení praktického problému 1.
![]()
Okamžité Reakce a RateLaw pro Reakci
rychlost reakce mezi fenolftaleinu a OH-iontů není konstantní, mění se s časem. Stejně jako většina reakcí, rychlost této reakcepostupně klesá s konzumací reaktantů. To znamená, že rychlost reakcezměny během měření.
, Aby se minimalizovalo chybu to přináší do našich měření, to seemsadvisable k měření rychlosti reakce v průběhu období, které jsou krátké, v případě času to bere pro reakci dojít. Můžeme se například pokusit změřit nekonečně malou změnu koncentrace![]() d(X)
d(X)![]() ke které dochází v nekonečně krátkém časovém období. Poměr těchto veličin je znám jako okamžitá rychlost reakce.
ke které dochází v nekonečně krátkém časovém období. Poměr těchto veličin je znám jako okamžitá rychlost reakce.
![]()
okamžitá rychlost reakce v kterémkoli okamžiku může být vypočítánaz grafu koncentrace reaktantu (nebo produktu) versus čas. Graf níže ukazuje, jak může být rychlost reakce pro rozklad fenolftaleinu vypočtena z grafu koncentrace versus čas. Rychlost reakce v každém okamžikuv čase se rovná sklonu tečny nakreslené k této křivce v tomto okamžiku.

okamžitá rychlost reakce lze měřit kdykoli mezi themoment, při které reakce jsou smíšené a reakce dosáhne rovnováhy.Extrapolace těchto dat zpět do okamžiku, kdy jsou činidla smíchána, dává počáteční okamžitou rychlost reakce.
![]()
Sazba Zákony a rychlostní Konstanty
zajímavý je výsledek, kdy okamžitou rychlost reactionis vypočtené v různých bodech podél křivky v grafu v předchozí kapitole. Rychlost reakce v každém bodě této křivky je přímoproporční koncentraci fenolftaleinu v daném okamžiku.
Rychlost = k (fenolftalein)
protože tato rovnice je experimentální zákon, který popisuje rychlost reakce, nazývá se zákon rychlosti reakce. Proporcionalityconstant, k, je známý jako rychlostní konstanta.
Praxe Problém 2:
Vypočítat rychlostní konstanty pro reakce mezi fenolftaleinu a OH – iontů, pokud okamžitá rychlost reakce je 2.5 x 10-5 mol na litr za sekundu, když je koncentrace fenolftaleinu 0,0025 m.
kliknutím sem zkontrolujete odpověď na praktický problém 2.
kliknutím sem zobrazíte řešení praktického problému 2.
Praxe Problém 3:
Použít rychlostní konstanta pro reakci mezi fenolftaleinu a OH – iontů pro výpočet počáteční okamžitá rychlost reakce pro experimentální údaje uvedené v předchozí tabulce.
kliknutím sem zkontrolujete odpověď na problém 3.
kliknutím sem zobrazíte řešení problému 3.
![]()
různé způsoby vyjádření rychlosti reakce
obvykle existuje více než jeden způsob měření rychlosti reakce. Můžeme studovat rozkladu vodíku, jodid, například měřením rychlosti, o níž buď H2 nebo I2 je vytvořena v následující reakce nebo použije na kterém AHOJ je spotřebována.
2 HI(g) H2(g) + I2(g)
Experimentálně zjistili jsme, že rychlost, při které I2 je tvořen je úměrné náměstí AHOJ koncentrace v každém okamžiku v čase.
![]()
Co by se stalo, kdybychom studovali rychlost, při které se vytváří H2?Vyvážená rovnice naznačuje, že H2 a I2 musí být vytvořeny napřesně stejnou rychlostí.
![]()
Co by se však stalo, kdybychom studovali rychlost, jakou je HI spotřebovánv této reakci? Protože HI je spotřebováno, musí být změna jeho koncentrace anegativním číslem. Podle konvence je rychlost reakce Vždy hlášena jako pozitivníčíslo. Proto musíme změnit znaménko před hlášením rychlosti reakce pro areaktant, který je spotřebován v reakci.
![]()
záporné znaménko dělá dvě věci. Matematicky převádí negativnízměna koncentrace HI na pozitivní rychlost. Fyzicky nám to připomíná, žekoncentrace reaktantu se časem snižuje.
jaký je vztah mezi rychlostí reakce získanou monitorováním tvorby H2 nebo I2 a rychlostí získanou sledováním HI zmizí? Stechiometrie reakce říká, že dvě molekuly HI jsoukonzumované pro každou vyrobenou molekulu H2 nebo I2. To znamená, žerychlost rozkladu HI je dvakrát rychlejší než rychlost, při které se vytvářejí H2 a I2. Tento vztah můžeme přeložit do matematické rovnice následujícím způsobem.
![]()
výsledkem je, že rychlostní konstanta získaná ze studia rychlost, při které H2and I2 jsou vytvořeny v této reakci (k) není totéž jako rychlostní konstanta získaná sledování rychlost, jakou AHOJ je spotřebována (k‘)
Praxe, Problém 4:
Vypočítat rychlost, jakou AHOJ zmizí v následující reakce v okamžiku, kdy I2 je tvořen ve výši 1,8 x 10-6 molů na litr za sekundu:
2 HI(g) ![]() H2(g) + I2(g)
H2(g) + I2(g)
Klikněte zde, aby se zkontrolujte, zda vaše odpověď na Praxi Problém 4.
kliknutím sem zobrazíte řešení problému 4.
![]()
Rychlost Zákona Proti Stechiometrii z aReaction
V roce 1930, Sir Christopher Ingold a spolupracovníci na Univerzitě ofLondon studována kinetika substituční reakce, jako je například následující.
CH3Br(aq) + OH-(aq)
CH3OH(aq) + Br-(aq)
zjistili, že rychlost této reakce je úměrná theconcentrations obou reaktantů.
Rate = k(CH3Br) (OH -)
když provedli podobnou reakci na mírně odlišném startingmateriálu, dostali podobné produkty.
(CH3)3CBr(aq) + OH-(aq)![]() (CH3)3COH(aq) + Br-(aq)
(CH3)3COH(aq) + Br-(aq)
Ale teď, rychlost reakce byla úměrná koncentraci pouze jeden z reaktantů.
Rychlost = k((CH3)3CBr)
Tyto výsledky ilustrují důležitý bod: sazba zákona pro areaction nelze předvídat ze stechiometrie reakce; musí být determinedexperimentally. Někdy je zákon rychlosti v souladu s tím, co od něj očekávámestoichiometrie reakce.
2 HI(g) H2(g) + I2(g)
Rate = k(HI)2
Often, however, it is not.
| 2 N2O5(g) |
Rychlost = k(N2O5) |
![]()
Pořadí Molecularity
Některé reakce se vyskytují v jediném kroku. Reakce, při které se chlorin převádí z ClNO2 na NO za vzniku NO2 a ClNO, je dobrým příkladem jednostupňové reakce.
ClNO2(g) + NO(g)
NO2(g) + ClNO(g)
Other reactions occur by a series of individual steps. N2O5,for example, decomposes to NO2 and O2 by a three-step mechanism.
| Step 1: | N2O5 |
|
| 2. Krok: | NO2 + NO3 |
|
| 3. Krok: | NO + NO3 |
kroky v reakci jsou klasifikovány z hlediska molecularity,který popisuje počet molekul spotřebováno. Když je spotřebována jedna molekula, krok se nazývá unimolekulární. Když dvě molekuly jsoukonzumované, je to bimolekulární.
praktický problém 5:
Určete molekullaritu každého kroku reakce, kterým se N2O5 rozkládá na NO2 a O2.
Klikněte zde pro kontrolu odpovědi na cvičný problém 5.
kliknutím sem zobrazíte řešení praktického problému 5.
reakce lze také klasifikovat podle jejich pořadí. Složení N2O5 je reakce prvního řádu, protože reakce závisí na koncentraci N2O5 zvýšené na první sílu.
Rychlost = k(N2O5)
rozklad HI je druhého řádu reakce, protože míra reakce závisí na koncentraci AHOJ zvýšen na druhou.
Rychlost = k (HI)2
když rychlost reakce závisí na více než jednomagentu, klasifikujeme reakci podle pořadí každého činidla.
Praxe Problém 6:
Klasifikovat řád reakce mezi no a O2 za vzniku NO2:
2 no(g) + O2(g) ![]() 2 NO2(g)
2 NO2(g)
Předpokládejme následující kurz práva pro tuto reakci:
Rate = k(NO)2 (O2)
kliknutím sem zkontrolujete odpověď na problém 6.
rozdíl mezi molekulárností a pořadím reakce je důležitý. Molekulárnost reakce nebo krok v reakci popisuje, co se děje na molekulární úrovni. Pořadí reakce popisuje, cose děje v makroskopickém měřítku. Pořadí reakce určujeme sledováním reakceobjeví se produkty reakce nebo reaktanty zmizí. Molekulárnost reakceje něco, co odvodíme, abychom vysvětlili tyto experimentální výsledky.
![]()
Kolize Teorie Modelu Chemických Reakcí,
kolize teorie modelu chemických reakcí, které mohou být použity toexplain pozorovaná četnost zákony pro jednokrokové a vícekrokové reakce. Tento model předpokládá, že rychlost jakéhokoli kroku reakce závisí na frekvenci kolizí mezi částicemi zapojenými do tohoto kroku.
níže uvedený obrázek poskytuje základ pro pochopení důsledkůmodel teorie kolizí pro jednoduché jednostupňové reakce, například následující.
ClNO2(g) + NO(g) ![]() NO2(g) + ClNO(g)
NO2(g) + ClNO(g)

kinetická molekulární teorie předpokládá, že počet kolizí persecond v plynu závisí na počtu částic na litr. Rychlost tvorby NO2 a ClNO v této reakci by proto měla být přímo úměrná koncentracím ClNO2 I NO.
Rychlost = k(ClNO2)(NE)
kolize teorie model naznačuje, že míra jakýkoli krok v areaction je úměrná koncentraci činidla spotřebovaného v tomto kroku. Zákon o jednostupňové reakci by proto měl souhlasit se stechiometrií reakce.
následující reakce se například vyskytuje v jediném kroku.
CH3Br(aq) + OH-(aq) ![]() CH3OH(aq) + Br-(aq)
CH3OH(aq) + Br-(aq)
Když se tyto molekuly srazit ve správné orientaci, pár ofnonbonding elektrony na OH – iontů může být věnován na atom uhlíku uprostřed je CH3Br molekuly, jak je znázorněno na obrázku níže.
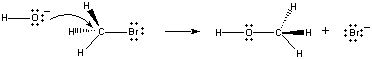
Když se to stane, uhlík-kyslík dluhopisů formy zároveň, že thecarbon-brom dluhopis je rozbité. Čistým výsledkem této reakce je substituce anoh-iontu za br-ion. Protože reakce probíhá v singlestep, které zahrnuje kolize mezi dvěma reaktantů, rychlost této reakce je úměrné koncentraci obou reaktantů.
Rate = k(CH3Br) (OH -)
ne všechny reakce se vyskytují v jednom kroku. Následující reakce nastane vtři kroky, jak je znázorněno na obrázku níže.
(CH3)3CBr(aq) + OH-(aq)![]() (CH3)3COH(aq) + Br-(aq)
(CH3)3COH(aq) + Br-(aq)
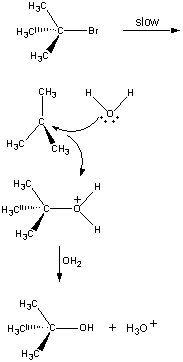
V prvním kroku, (CH3)3CBr moleculedissociates do dvojice iontů.
| První krok | 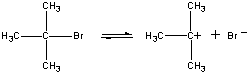 |
kladně nabité (CH3)3C+ ion thenreacts s vodou v druhém kroku.
| Druhý krok | 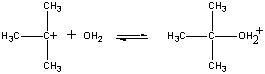 |
produkt této reakce pak ztrácí proton buď OH-iontů nebo vody v posledním kroku.
| Třetí krok | 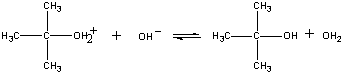 |
druhý a třetí kroky této reakce jsou mnohem rychlejší thanfirst.
| (CH3)3CBr |
Slow step | |
| (CH3)3C+ + H2O |
Fast step | |
| (CH3)3COH2+ + OH- |
Fast step |
The overall rate of reaction is therefore more or less equal to the rateof the first step. První krok se proto nazývá krok omezující rychlost vTato reakce, protože doslova omezuje rychlost, při které mohou být produkty reakce vytvořeny. Protože v kroku omezujícím rychlost je zapojeno pouze jedno činidlo, celková rychlost reakce je úměrná koncentraci pouze tohoto činidla.
Rychlost = k ((CH3)3CBr)
zákon rychlosti pro tuto reakci se proto liší od toho, co bychom předpokládali ze stechiometrie reakce. Ačkoli reakce spotřebuje oba (CH3)3CBRAND OH -, rychlost reakce je pouze úměrná koncentraci (CH3) 3CBr.
zákony rychlosti chemických reakcí lze vysvětlit následujícímiobecná pravidla.
rychlost je každý krok reakce je přímo úměrná koncentraci činidla spotřebovaného v tomto kroku.
zákon celkové rychlosti reakce je určen posloupností kroků nebo mechanismem, kterým se reaktanty převádějí na produkty reakce.
celkovému zákonu rychlosti pro reakci dominuje zákon rychlosti pro nejpomalejší krok reakce.