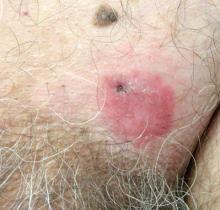
en 70-årig mand præsenterede en ikke-pruritisk erythematøs skællet plak i venstre suprapubisk region af 6 måneders varighed, der ikke havde reageret på terbinafincreme 1% efter 1 måneds behandling af mistanke om tinea cruris. Hans medicinske historie var bemærkelsesværdig for hypertension, hyperlipidæmi, kronisk obstruktiv lungesygdom, godartet prostatahyperplasi, en abdominal aortaaneurisme, alkoholafhængighed, tobaksforstyrrelse og utilsigtet vægttab på 15 lb i løbet af det sidste år.
diagnosen: Ekstramammær Paget sygdom
en biopsi af plakken afslørede en intraepidermal proliferation af store celler med rigelig klar cytoplasma og store vesikulære kerner fordelt over epidermis (Figur 1). De neoplastiske celler farvede positive for både periodisk syre-Schiff-plet (figur 2) og CK7 (figur 3). Kemi-og leverfunktionspanel, urinanalyse, carcinoembryoniske antigenniveauer og prostata-specifikke antigenniveauer var inden for referenceområdet. Et komplet antal blodlegemer afslørede mild megaloblastisk anæmi. Efterfølgende computertomografi af brystet, maven og bækkenet afslørede en abdominal aortaaneurisme og prostataforstørrelse uden tegn på potentielle maligniteter. Koloskopi afslørede flere hyperplastiske polypper og et rørformet adenom. Cystoskopi var normal, bortset fra tegn på prostataforstørrelse. Urincytologi var ikke bemærkelsesværdig. Patienten blev henvist til udskæring af læsionen med Mohs mikrografisk kirurgi. Opfølgning blev anbefalet hver 3.måned i de første 2 år efter operationen og derefter hver 6. måned for at overvåge for tilbagefald eller sekundære neoplasmer.
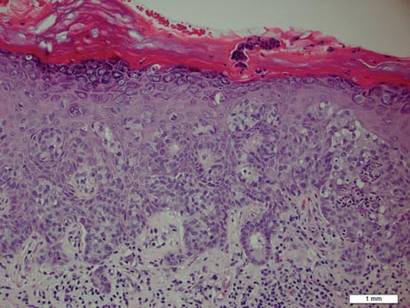
Figur 1. Intraepidermal proliferation af store celler med rigelig klar cytoplasma og store vesikulære kerner fordelt over hele epidermis som individuelle celler og som variabelt store aggregater af celler (H&E, original forstørrelse lutr 200). (Referencelinje angiver 1 mm.)
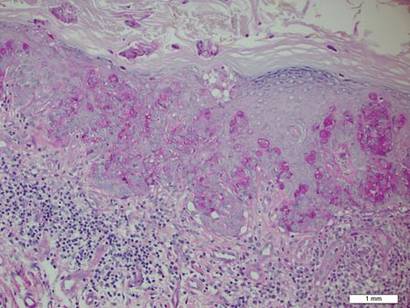
figur 2. Granulær cytoplasma var positiv ved periodisk syre-Schiff-farvning (oprindelig forstørrelse kurr 200). (Referencelinje angiver 1 mm.)
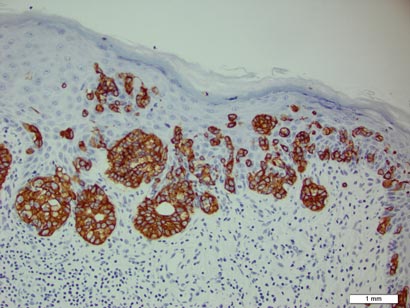
figur 3. Neoplastiske Paget-celler var karakteristisk positive ved farvning for CK7 (oprindelig forstørrelse på 200). (Referencelinje angiver 1 mm.)
Sir James Paget beskrev først brystpaget sygdom i brystvorten i 1874 i sin rapport om 15 kvinder med hududbrud i brystvorten og areola og efterfølgende karcinom i det underliggende bryst.1 Paget beskrev også en patient med en lignende udbrud på glanspenis og Crocker2 beskrevet ekstramammær Paget sygdom (EMPD) af pungen og penis i 1889. Den primære forskel mellem mammary Paget disease og EMPD er den anatomiske placering.
Ekstramammær Paget sygdom er en sjælden tilstand, der typisk rammer patienter i alderen 50 til 80 år og er mere almindelig hos kvinder og hvidhudede løb.3 Ekstramammær Paget-sygdom målretter ofte kutane steder, der er rige på apokrine kirtler. Det mest berørte sted er vulva efterfulgt af perineal, perianal, scrotal og penis hud. Mindre almindeligt kan aksiller, skinker, lår, øjenlåg og eksterne auditive kanaler blive påvirket.4
patienter med EMPD er typisk til stede med velafgrænsede, ikke-opløselige, erythematøse og eksematiske plaketter, der kan have forbundet skorpe, skalering, papillomatøse ekskrescenser, lichenificering, sårdannelse eller blødning. Det mest almindelige symptom er kløe, efterfulgt af forbrænding, irritation, smerte og ømhed.5 ti procent af patienterne er asymptomatiske. Det gennemsnitlige interval mellem symptomdebut og diagnose er 2 år.5
histopatologi afslører diffust infiltrerende, uregelmæssige, neoplastiske Paget-celler i epidermis, der er store og vakuolerede med rigelig Lyseblå cytoplasma og store vesikulære kerner, som kan være centralt eller lateralt komprimeret. Cellerne kan fordeles enkeltvis eller i grupper som tråde, reder eller kirtelmønstre inden for den nedre epidermis, rete-Kamme og adneksale strukturer. Hyperkeratose, acanthosis og parakeratose kan også være til stede. Paget-celler pletter til immunhistokemiske markører af apokrin og eccrin-afledning inklusive cytokeratiner med lav molekylvægt, groft cystisk sygdomsvæskeprotein 15, periodisk syre-Schiff-plet og carcinoembryonisk antigen.5 Perrotto et al6 undersøgte 98 prøver fra 61 patienter og fandt, at CK7 var positiv i alle EMPD-prøver, mens CK20 og groft cystisk sygdomsvæskeprotein 15 var positive i store undergrupper af både primær og sekundær EMPD. Tilfælde af EMPD sekundært til anorektalt adenocarcinom var stort set erbb2 (tidligere HER2/neu) negative og CDKS2 positive.6
diagnose af EMPD bør efterfølges af en grundig undersøgelse for underliggende carcinomer. I en gennemgang af 197 tilfælde af EMPD havde 24% af patienterne med EMPD en associeret underliggende in situ eller invasiv apokrin carcinom, som var forbundet med en højere dødelighed end hos patienter uden denne underliggende malignitet. Derudover havde 12% af EMPD-patienterne en associeret underliggende intern malignitet.7 disse maligniteter kan omfatte carcinomer i urinrøret, blæren, vagina, livmoderhalsen, endometrium, prostata, tyktarm og endetarm. Perianal EMPD har en højere frekvens af associerede maligniteter end vulvar EMPD.5 placeringen af EMPD er relateret til placeringen af den underliggende malignitet; for eksempel er perianal EMPD forbundet med kolorektal adenocarcinomer, og EMPD i penis, pungen og lysken er forbundet med genitourinære maligniteter. Undersøgelser for at søge efter tilknyttede maligniteter hos patienter med EMPD kan omfatte bækken-ultralyd og/eller magnetisk resonansafbildning, hysteroskopi, koloskopi, sigmoidoskopi, cystoskopi, intravenøst pyelogram, mammogram og/eller røntgenbillede af brystet.