Identificer et molekyles mest sure H
en metodisk tilgang fungerer bedst. Kort sagt skal du scanne molekylet for sure funktionelle grupper og derefter rangere reaktiviteten af disse grupper. Den mest sure funktionelle gruppe holder normalt den mest sure H i hele molekylet.
“Scan and rank” lyder simpelt, men det skjuler flere vanskeligheder, der er uddybet nedenfor.
Scan et molekyle for kendte sure funktionelle grupper
sure protoner er normalt bundet til O eller N. Derfor er det første skridt at kigge efter alle OH og NH obligationer.
Når du finder OH-og NH-bindinger, skal du dog beslutte, om disse bundne atomer skal klumpes i en funktionel gruppe med tilstødende atomer.
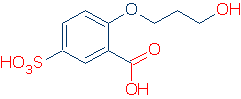
den eneste praktiske metode til at identificere en funktionel gruppe er allerede at kende nogle. For eksempel, hvis du ved, at ROH, RCO2H og RSO3H er almindelige sure funktionelle grupper, har du ingen problemer med at finde sure grupper i følgende molekyle (de korrekte grupper er markeret med rødt).
rang OH og Nh-surhedsgrad separat
pKa-værdierne for almindelige OH-og NH-syrer spænder over brede områder, og deres intervaller overlapper hinanden. Ranking fortsætter hurtigere, hvis du rangerer OH-og NH-syrerne separat, og sammenlign derefter de bedste kandidater i hver kategori.
den mest hensigtsmæssige metode til rangordning af sure grupper er allerede at kende deres karakteristiske pKa-værdier. Hvis du kender disse værdier for alle de sure grupper i dit molekyle, indeholder gruppen med den laveste pKa den mest sure H. sag lukket.
Hvis du ikke husker pKa-værdier for alle de sure grupper, kan et par generelle principper guide dig.
#1 betydning – positivt ladede syrer er stærkere end neutrale syrer. Negativt ladede syrer er sjældent sure. Hvis du sammenligner pKa-værdier for almindelige OH-syrer, vil du se, at ROH2+ syrer (som inkluderer H3O+ og R2OH+) er betydeligt stærkere end neutrale syrer, såsom RCO2H, PhOH og ROH. De eneste neutrale syrer, der er stærkere end ROH2+, er H2SO4 og visse andre RSO3H.
den formelle ladningsregel gælder endnu stærkere for NH-syrer. Forskellen i pKa mellem H3O+ og H2O er 18 enheder, mens forskellen i pKa mellem NH4+ og NH3 er en gigantisk 26 enheder.
#2 betydning-se efter aktiverende grupper, herunder RSO2, RC=O og Ph. følgende diagram viser, hvordan hver gruppe af atomer aktiverer en OH-syre (pKa-værdier spænder fra 16 til -2):
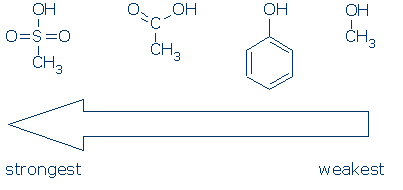
CH3 betragtes som en tilskuergruppe, uanset hvor den forekommer i disse molekyler. Det er ikke-polært og udøver ikke en signifikant feltinduktiv effekt, og det er ude af stand til at delokalisere ladning. Derfor er det muligt at erstatte CH3 med andre tilskuergrupper (for eksempel H og andre R) uden at påvirke reaktiviteten meget.
der skal fremsættes yderligere to punkter vedrørende aktiverende grupper.
for det første udøver grupperne en lignende virkning på NH-syrer (og aktiveringssekvensen er den samme: RSO2 > RC=O > Ph). Som det sker, behøver du kun at lære effekten af Ph på NH+ til dette kursus:
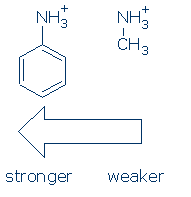
for det andet skal de aktiverende grupper være bundet direkte til OH (eller NH) gruppen for at aktivere den. Følgende forbindelser har lignende pKa-værdier, fordi de aktiverende grupper ikke er bundet direkte til OH: CH3C(=O)CH2OH, PhCH2OH og CH3CH2OH.
#3 betydning-alt andet lige er en OH-syre mere sur end en NH-syre. Dette princip kan være meget nyttigt, hvis det bruges korrekt. Min bekymring er, at du forstår, hvad der menes med “alt er lige.”Dette betyder, at O og N skal have den samme formelle afgift (punkt #1) og skal være bundet til den samme aktiverende gruppe (punkt #2). Forskelle i tilskuergrupper betyder dog ikke noget.
nogle gyldige sammenligninger inkluderer:
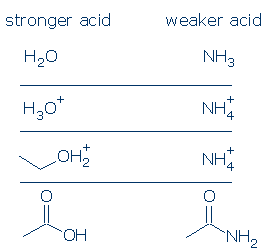
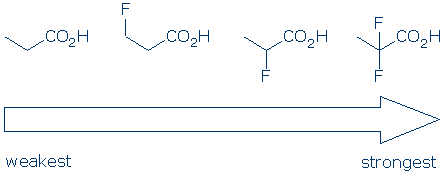
#4 betydning – inden for en funktionel gruppekategori skal du bruge substituenteffekter til at sammenligne syrer. Elektronegative substituenter forbedrer normalt surheden i en funktionel gruppe gennem en kombination af felt-og induktive effekter. Disse virkninger forbedres, når 1) substituenten er placeret tættere på den sure gruppe, og 2) der er flere substituenter. I betragtning af disse principper forventer vi, at surheden af disse carboksyliske syrer følger denne tendens: