Generic Name: epinastine hydrochloride
Dosage Form: ophthalmic solution
Medically reviewed by Drugs.com. Last updated on June 1, 2020.
- Overview
- Side Effects
- Dosage
- Professional
- Pregnancy
- More
Indications and Usage for Epinastine HCl Ophthalmic Solution
Epinastine HCl Ophthalmic Solution 0.알레르기 성 결막염과 관련된 가려움증 예방을 위해 05%가 표시됩니다.권장 복용량은 하루에 두 번 각 눈에 한 방울입니다.에피나 스틴은 임신 한 쥐에게 경구 투여 후 강아지의 체중 증가를 감소 시켰는데,이는 약 90,000 배였다.그러나 임산부에 대한 적절하고 잘 통제 된 연구는 없습니다. 동물 생식 연구가 항상 인간의 반응을 예측하는 것은 아니기 때문에 잠재적 인 이익이 태아에 대한 잠재적 위험을 정당화하는 경우에만 임신 중에 에피 나 스틴 안과용 용액 0.05%를 사용해야합니다.수유중인 쥐의 연구에 따르면 모유에서 에피나 스틴의 배설이 밝혀졌습니다. 이 약물이 인간의 우유에 배설되는지 여부는 알려져 있지 않습니다. 많은 약물이 인간의 우유에 배설되기 때문에,에피 나 스틴 안과용 용액 0.05%가 간호 여성에게 투여 될 때는주의를 기울여야합니다.2 세 미만의 소아 환자의 안전성과 효과는 확립되지 않았습니다.노인과 젊은 환자간에 안전성 또는 효과에 대한 전반적인 차이는 관찰되지 않았다.안과용액 설명안과용액 설명05% is a clear, colorless, sterile isotonic solution containing epinastine HCl, an antihistamine and an inhibitor of histamine release from the mast cell for topical administration to the eyes.
Epinastine HCl is represented by the following structural formula:
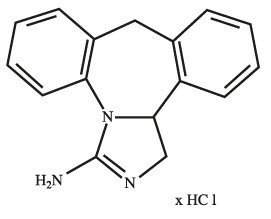
C16H15N3HCl Mol. Wt. 285.78
Chemical Name:
3-Amino-9,13b-dihydro-1H-dibenzimidazoazepine hydrochloride
Each mL contains: Active: Epinastine HCl 0.05% (0.5 mg/mL) equivalent to epinastine 0.044% (0.44 mg/mL); Preservative: Benzalkonium chloride 0.01%; Inactives: 에데 테이트 이 나트륨,이수화 물;정제수;염화나트륨;인산 나트륨,일 염기,무수;및 수산화 나트륨 및/또는 염산(산도 조절).이 경우,안과 용 용액은 약 250 내지 310 의 삼투압 범위를 갖는다.에피 나 스틴은 국소 적으로 활성 인 직접 수용체 길항제 및 비만 세포로부터의 히스타민 방출 억제제이다. 에피 나 스틴은 히스타민 1-수용체에 대해 선택적이며 히스타민 2-수용체에 대한 친 화성을 갖는다. 또한,에피 나스틴은 수용체에 대한 친 화성을 갖는다.알레르기 성 결막염이있는 14 명의 피험자는 7 일 동안 매일 두 번 각 눈에 0.05%의 에피 나 스틴 안액 한 방울을 투여 받았다. 7 일째에,낮은 전신 노출을 나타내는 약 2 시간 후에 평균 최대 에피 나 스틴 혈장 농도의 0.04 에피 나 스틴 혈장 농도에 도달 하였다. 이러한 농도 단일 복용량 다음 본 그 이상의 증가를 나타내는 동안,일 1 및 일 7 곡선(경매)값 아래 영역 변경 되지 않은 다중 투약과 전신 흡수에 아무 증가 나타내는 했다. 에피나스틴은 혈장 단백질에 64%결합되어 있습니다. 총 전신 클리어런스는 약 56 리터/시간이며 터미널 플라즈마 제거 반감기는 약 12 시간입니다. 에피나 스틴은 주로 변하지 않고 배설됩니다. 정맥 투여 량의 약 55%는 소변에서 변하지 않고 대변에서 약 30%로 회복됩니다. 10%미만이 대사됩니다. 신장 제거는 주로 활성 관상 분비를 통해 이루어집니다.생쥐 또는 쥐의 18 개월 또는 2 년식이 발암 성 연구에서 에피나 스틴은 최대 40 밀리그램/킬로그램 용량으로 발암 성이 없었다.새로 합성 된 배치에서 에피나 스틴은 인간 림프구를 이용한 에임스/살모넬라 분석 및 시험 관내 염색체 수차 분석에서의 돌연변이 유발성에 대해 음성이었다. 긍정적 인 결과는 각각 인간 말초 림프구와 79 세포,1980 년대에 실시 된 두 체외 염색체 수차 연구에서 에피 나스틴의 초기 배치와 함께 보였다. 에피 나 스틴은 중국 햄스터의 마우스 미세 핵 분석 및 염색체 수차 분석을 포함한 생체 내 분자 형성 연구에서 음성이었다. 이 분석에서는 쥐의 1 차 간세포를 이용한 생체 내/시험 관내 예정되지 않은 유전자 합성 분석 및 생체 내/시험 관내 예정되지 않은 유전자 합성 분석에서 음성이었다.에피 나 스틴은 수컷 쥐의 생식력에 아무런 영향을 미치지 않았다. 암컷 쥐의 생식력 감소는 최대 약 90,000 배의 경구 용량으로 관찰되었습니다.(1)결막 항원 챌린지 환자를 투여 한 후 결막 하 포닉스에 항원을 주입 한 임상 연구에서 알레르기 성 결막염 환자의 안구 가려움증 개선을위한 차량보다 유의하게 우수한 것으로 나타났습니다.; 그리고(2)환자가 그들의 자연 서식지에 있는 알레르기 절기 도중 투약되고 평가된 환경 분야 연구. 결과는 결막 항원 챌린지 후 3~5 분 이내에 에피 나 스틴 클로르 0.05%에 대한 신속한 작용 발병을 입증했습니다. 효과의 지속 시간 8 시간,하루에 두 번 처방 적합 하 게 표시 했다. 이 투약 요법은 타키필락시스의 증거 없이 최대 8 주 동안 안전하고 효과적인 것으로 나타났다.1.안과용액:안과용액:안과용액:안과용액:안과용액:안과용액:안과용액:안과용액:안과용액:안과용액:안과용액:안과용액:안과용액:안과용액05%은 공급 멸균에 불투명 흰색 LDPE 플라스틱 병을 적기 팁과 백색의 폴리프로필렌(PP)모자를 다음과 같다:
| 5mL10mL 병 | NDC51991-836-75 |
저장:20°-25°C(68°-77°F). 병을 단단히 닫고 어린이의 손이 닿지 않는 곳에 보관하십시오.점적기 끝의 무균 환자는 점적기 끝의 아무 표면든지에 만지지 말라 조언되어야 합니다,이것은 내용을 오염시킬지도 모르기 때문에(경고와 경고,5.1 를 보십시오).환자는 눈이 붉으면 콘택트 렌즈를 착용하지 말 것을 권고합니다. 환자는 콘택트 렌즈 관련 자극을 치료하기 위해 에피 나 스틴 안과용 용액 0.05%를 사용해서는 안된다는 점을 권고 받아야합니다. 환자는 또한 에피 나 스틴 안과용 용액 0.05%를 점안하기 전에 콘택트 렌즈를 제거 할 것을 권고 받아야합니다.에 피나 스틴 안과용 용액의 방부제 0.05%,염화 벤잘 코늄은 소프트 콘택트 렌즈에 흡수 될 수 있습니다. 10 분 후에 다시 삽입할 수 있습니다.에 의해 배포:브레 켄 리지 제약,주식 회사에 의해 제조:프리마 파르마,주식 회사
San Diego, CA 92121
Rev: 04/2020
2323 04/20
PRINCIPAL DISPLAY PANEL – 5 mL Bottle Carton
NDC 51991-836-75
Epinastine HCl
Ophthalmic
Solution,
0.05%
FOR USE IN THE
EYES ONLY
sterile
Rx Only
5 mL sterile
breckenridge
A Towa
Company

| EPINASTINE HYDROCHLORIDE epinastine hydrochloride solution/ drops |
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
Labeler – Breckenridge Pharmaceutical, Inc. (150554335)
| Establishment | |||
| Name | Address | ID/FEI | Operations |
| PrimaPharma, Inc. | 079699106 | MANUFACTURE(51991-836) | |