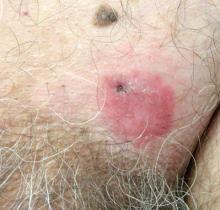
en 70 år gammel mann fikk en ikke-pruritisk erytematøs skjellete plakett i venstre suprapubisk region av 6 måneders varighet som ikke hadde respondert på terbinafinkrem 1% etter 1 måneders behandling av mistanke om tinea cruris. Hans medisinske historie var bemerkelsesverdig for hypertensjon, hyperlipidemi, kronisk obstruktiv lungesykdom, godartet prostatahyperplasi, abdominal aortaaneurisme, alkoholavhengighet, tobakksforstyrrelse og utilsiktet vekttap på 15 lb i løpet av det siste året.
Diagnosen: Ekstramammær Paget Sykdom
en biopsi av plakk viste en intraepidermal proliferasjon av store celler med rikelig klar cytoplasma og store vesikulære kjerner fordelt gjennom epidermis (Figur 1). De neoplastiske cellene farget positivt for både periodisk syre-Schiff-flekk (Figur 2) og CK7 (Figur 3). Kjemi – og leverfunksjonspanel, urinanalyse, karsinoembryoniske antigennivåer og prostataspesifikke antigennivåer var innenfor referanseområdet. Et komplett blodcelletall viste mild megaloblastisk anemi. Påfølgende computertomografi av brystet, magen og bekkenet viste en abdominal aortaaneurisme og prostataforstørrelse uten tegn på potensielle maligniteter. Koloskopi avslørte flere hyperplastiske polypper og en tubulær adenom. Cystoskopi var normalt, bortsett fra tegn på prostataforstørrelse. Urin cytologi var unremarkable. Pasienten ble henvist til excision av lesjonen Med Mohs mikrografisk kirurgi. Oppfølging ble anbefalt hver 3. måned de første 2 årene etter operasjonen og deretter hver 6. måned for å overvåke residiv eller sekundære neoplasmer.
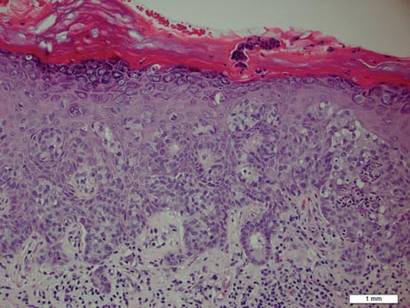
Figur 1. Intraepidermal proliferasjon av store celler med rikelig klar cytoplasma og store vesikulære kjerner fordelt over epidermis som individuelle celler og som variabelt store aggregater av celler (H&E, original forstørrelse ×200). (Referanselinjen indikerer 1 mm.)
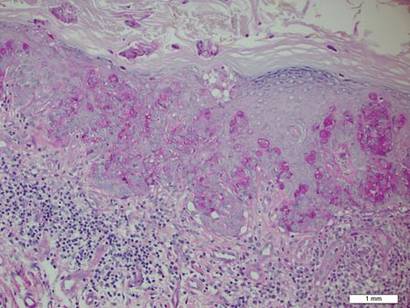
Figur 2. Granulær cytoplasma var positiv på periodisk syre-Schiff-farging (original forstørrelse ×200). (Referanselinjen indikerer 1 mm.)
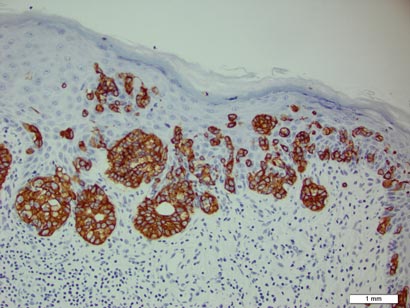
figur 3. Neoplastiske Paget-celler var karakteristisk positive på farging FOR CK7(original forstørrelse ×200). (Referanselinjen indikerer 1 mm.)
Sir James Paget først beskrevet mammary Paget sykdom i brystvorten i 1874 i sin rapport av 15 kvinner med hud utbrudd av brystvorten og areola og påfølgende karsinom i underliggende bryst.1 Paget beskrev også en pasient med lignende utbrudd på glanspenis og Crocker2 beskrev extramammary Paget disease (EMPD) i pungen og penis i 1889. Hovedforskjellen mellom mammary Paget disease OG EMPD er den anatomiske plasseringen.Extramammary Paget sykdom Er en sjelden tilstand som vanligvis rammer pasienter i alderen 50 til 80 år og er mer vanlig hos kvinner og hvite skinnede raser.3 Ekstramammær Paget sykdom retter seg ofte mot kutane steder som er rike på apokrine kjertler. Den mest berørte området er vulva etterfulgt av perineal, perianal, scrotal, og penile hud. Mindre vanlig kan axillene, baken, lårene, øyelokkene og eksterne hørskanaler påvirkes.4
PASIENTER med EMPD har typisk godt avgrensede, ikke-oppløselige, erytematøse og eksematiske plakk som kan ha assosiert skorpedannelse, avskalling, papillomatøse utvekster, lichenifisering, sårdannelse eller blødning. Det vanligste symptomet er kløe, etterfulgt av brenning, irritasjon, smerte og ømhet.5 Ti prosent av pasientene er asymptomatiske. Gjennomsnittlig intervall mellom symptomstart og diagnose er 2 år.5
Histopatologi avslører diffus infiltrerende, irregulære, neoplastiske Paget-celler i epidermis som er store og vakuolerte med rikelig blekblå cytoplasma og store vesikulære kjerner, som kan være sentralt eller lateralt komprimert. Cellene kan distribueres enkeltvis eller i grupper som tråder, reir, eller kjertel mønstre i nedre epidermis, rete rygger, og adnexal strukturer. Hyperkeratose, akanthose og parakeratose kan også være tilstede. Paget-celler flekker for immunhistokjemiske markører for apokrin-og ekkrinderivasjon, inkludert cytokeratiner med lav molekylvekt, gross cystisk sykdomsvæskeprotein 15, periodisk syre-Schiff-flekk og karsinoembryonisk antigen.5 Perrotto et al6 studerte 98 prøver fra 61 pasienter og fant AT CK7 var positiv i ALLE EMPD-prøver, mens CK20 og gross cystic disease fluid protein 15 var positive i store undergrupper av både primær OG sekundær EMPD. TILFELLER AV EMPD sekundært til anorektalt adenokarsinom var hovedsakelig erbb2 (TIDLIGERE HER2/neu) negative og CDX2 positive.6
DIAGNOSE AV EMPD bør følges av en grundig undersøkelse for underliggende karsinomer. I en gjennomgang av 197 TILFELLER AV EMPD hadde 24% av PASIENTENE MED EMPD et assosiert underliggende in situ eller invasivt adnexalt apokrint karsinom, som var assosiert med en høyere dødelighet enn hos pasienter uten denne underliggende maligniteten. I tillegg hadde 12% AV EMPD-pasientene en assosiert underliggende intern malignitet.7 disse malignitetene kan omfatte karsinomer i urinrøret, blæren, skjeden, livmorhalsen, endometrium, prostata, kolon og endetarm. Perianal EMPD har en høyere frekvens av assosiert malignitet enn vulvar EMPD.5 plasseringen AV EMPD er relatert til plasseringen av den underliggende maligniteten; for eksempel er perianal EMPD forbundet med kolorektale adenokarsinomer, OG EMPD av penis, skrot og lyske er forbundet med genitourinære maligniteter. Undersøkelser for å søke etter assosiert malignitet hos pasienter MED EMPD kan omfatte bekken ultralyd og / eller magnetisk resonans imaging, hysteroskopi, koloskopi, sigmoidoskopi, cystoskopi, intravenøs pyelogram, mammogram, og/eller brystet radiografi.