hjertemyocytten er den viktigste cellen som er involvert i remodeling. Fibroblaster, kollagen, interstitium og koronarbeinene i mindre grad, spiller også en rolle. Et vanlig scenario for remodeling er etter hjerteinfarkt. Det er myokardisk nekrose (celledød) og uforholdsmessig tynning av hjertet. Dette tynne, svekkede området er ikke i stand til å motstå trykket og volumbelastningen på hjertet på samme måte som det andre friske vevet. Som et resultat er det dilatasjon av kammeret som oppstår fra infarktområdet. Den innledende remodelleringsfasen etter et hjerteinfarkt resulterer i reparasjon av nekrotisk område og myokardisk arrdannelse som til en viss grad kan betraktes som gunstig siden det er en forbedring i eller vedlikehold AV LV-funksjon og hjerteutgang. Over tid, men som hjertet gjennomgår pågående remodeling, blir det mindre elliptisk og mer sfærisk. Ventrikulær masse og volumøkning, som sammen påvirker hjertefunksjonen negativt. Til slutt, diastolisk funksjon, eller hjertets evne til å slappe av mellom riene kan bli svekket, ytterligere forårsaker nedgang.
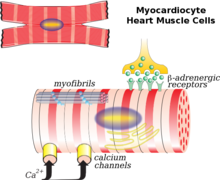
etter et hjerteinfarkt (MI) kan hjertemyocytdød utløses av nekrose, apoptose eller autofagi, noe som fører til tynning av hjerteveggen. De overlevende hjertemyocytene ordner enten parallelt eller i serie til hverandre, noe som bidrar til ventrikulær dilatasjon eller ventrikulær hypertrofi, avhengig av belastningsspenningen på ventrikulærveggen. Dessuten er redusert ekspresjon Av v1 mysoin og l-type kalsiumkanaler på hjerte myocytter også antatt å forårsake hjerte remodelling. Under normale kroppsforhold står fettsyre for 60 til 90% av energiforsyningen til hjertet. Post MI, som fettsyre oksidasjon avtar, fører det til redusert energiforsyning for hjerte myocytter, akkumulering av fettsyrer til giftige nivåer, og dysfunksjon av mitokondrier. Disse konsekvensene førte også til økningen i oksidativt stress på hjertet, forårsaker spredning av fibroblaster, aktivering av metalloproteinaser og induksjon av apoptose, som vil bli forklart nedenfor. Dessuten bidrar inflammatorisk immunrespons etter MI også til de ovennevnte endringene.i Tillegg er hjerteinterstitiumet som i stor grad besto Av type I og TYPE III kollagenfibre, også involvert i kardial remodeling. Kardial kollagen syntetiseres av fibroblaster og nedbrytes av metalloproteinaser. Fibroblaster aktiveres etter MI, noe som fører til økt kollagensyntese og fibrose i hjertet. Økt ekspresjon AV MMP1 og MMP9 førte til nedbrytning av kollagenfibre, og deretter utvidelse av hjertet. Flere signalveier som Angiotensin II, Transforming growth factor beta (TGF-beta) Og Endotelin 1 er kjent for å utløse syntese og nedbrytning av kollagenfibre i hjertet.Andre faktorer som høyt blodtrykk, aktivering av sympatisk system som frigjør noradrenalin, aktivering av renin-angiotensin system som frigjør renin og antidiuretiske hormoner er viktige bidragsytere til hjerte remodelling. Imidlertid antas atrielt natriuretisk peptid å være kardiobeskyttende.