biomateriały
badanie biomateriałów możliwe jest poprzez bardzo ogólną, ale spójną definicję w parkach i jeziorach . Zgodnie z nimi biomateriał można zdefiniować jako dowolny materiał używany do produkcji urządzeń zastępujących część lub funkcję ciała w bezpieczny, niezawodny, ekonomiczny i fizjologicznie akceptowalny sposób.
aby w zadowalający sposób wykonać funkcję wymiany, powiększenia lub podtrzymania struktury, implant musi naśladować lub dopasowywać się do właściwości tkanki. Literatura donosi o istnieniu różnych rodzajów przeszczepów kostnych stosowanych w implantach: autologicznych (pochodzących od tej samej osoby); homologicznych (od osoby tego samego gatunku odbiorcy); i heterologicznych (gdy gatunki dawcy i biorcy nie są takie same – na przykład bydło ).
przeszczepy autologiczne mają pewne wady, na przykład: interwencja w zdrowym obszarze ciała pacjenta; chorobowość okolicy dawcy, wyższy okres rekonwalescencji; podatność na infekcje; oraz postępująca i stała resorpcja . Tak więc, implanty w syntetycznych biomateriałach, takich jak ceramika i polimery, zostały szeroko opracowane i stosowane. Według Pereiry, Buono i Zavaglii zapotrzebowanie na biomateriały wzrosło z 5 do 15% każdego roku.
Klasyfikacja biomateriałów
według Batha i Santosa biomateriały można podzielić na cztery klasy , zgodnie z ich kompatybilnością z otaczającymi tkankami:
Biotolerant: Implant oddzielony od otaczającej kości warstwą tkanki miękkiej nad interfejsem. Brak kontaktu w osteogenezie. Warstwa jest indukowana przez uwolnienie implantu monomerów, jonów i / lub produktów korozji. Prawie wszystkie polimery syntetyczne i większość metali należą do tej kategorii.
Bioinert: Implanty w bezpośrednim kontakcie z tkanką kostną, występujące w osteogenezie. Jednak nie ma reakcji chemicznej między tkanką a implantem. Nie ma, przynajmniej w ilościach wykrywalnych przez komórki, uwalniania żadnego składnika. Przykładami biomateriałów bioinert są: tlenek glinu, tlenek cyrkonu, Tytan, tantal, niob i węgiel.
bioaktywność: istnieje interakcja między implantem a tkanką kostną, zakłócająca bezpośrednio osteogenezę. Dzięki podobieństwu chemicznemu mineralna część tkanki kostnej wiąże się z implantem, promując osteoprzewodnictwo. Głównymi materiałami tej klasy są: ca-fosforan, vitro-ceramika i hydroksyapatyt.
Biorezorbowalne: materiały, które po pewnym czasie w kontakcie z tkankami, kończą się degradacją, solubilizacją lub fagocytozą przez organizm. Są one interesujące w zastosowaniach klinicznych, w których nie zaleca się ponownego otwarcia w celu usunięcia implantu. Przedstawicielami tej klasy są fosforan trójwapniowy (TCP) i PLLA (kwas Poli-L-mlekowy).
biomateriały metaliczne
czasami pierwiastki metaliczne w ich naturalnych formach i w małych ilościach są tolerowane przez organizm, takie jak żelazo (Fe) w krwinkach czerwonych, kobalt (Co) w syntezie witaminy B12 i w wiązaniach sieciowych elastyny obecnej w tętnicy aorty . Jednak w dużych ilościach większość metali nie jest tolerowana przez organizm.
niektóre metale są stosowane jako substytuty tkanek twardych, na przykład w całkowitych protezach stawu biodrowego i kolanowego, płytkach i śrubach do mocowania złamań, urządzeniach do mocowania kolumn i implantach dentystycznych ze względu na ich doskonałe właściwości mechaniczne i odporność na korozję . Według Barbucciego materiał metalowy stosowany do budowy protez ortopedycznych, urządzeń do osteosyntezy i implantów dentystycznych powinien mieć następujące cechy:
- odporność Graniczna równa lub większa niż 800 MPa;
- odporność na korozję (lokalna i ogólna);
- biokompatybilność.
biokompatybilność nie jest efektem ani unikalnym zjawiskiem. Odnosi się do szeregu procesów obejmujących różne mechanizmy interakcji, ale współzależnych w odniesieniu do materiałów i tkanek. Jest to zdolność materiału do wykonywania określonej funkcji w organizmie bez powodowania toksycznych lub szkodliwych skutków dla systemów biologicznych .
te cechy są tak restrykcyjne, że tylko niewielka liczba klas materiałów metalicznych może być z powodzeniem stosowana.
pierwszym stopem opracowanym specjalnie do stosowania w organizmie człowieka była „stal wanadowa”, używana do produkcji płyt i śrub do złamań kości . Wśród biomateriałów metalicznych najczęściej stosowane są austenityczne stale nierdzewne typu 316 LVM, stopy Co-Cr-Mo, Co-Ni-Cr-Mo, Czysty tytan i Ti-6Al-4V . Niektóre przykłady przedstawiono na rysunku 1.

Rysunek 1: metalowe urządzenia do zastosowań medycznych: a) głowa kości udowej; B) kolano przegubowe; C) płytka stawu żuchwowego.
w tej pracy zajmiemy się dokładniej stopami co i Ti, których zastosowanie w szybkim prototypowaniu DMLS w dziedzinie medycyny jest bardziej wyraziste.
stopy kobaltu
stopy kobaltu zostały pierwotnie zaproponowane do implantów chirurgicznych ponad 70 lat temu . Istnieją zasadniczo dwa rodzaje stopów Co do zastosowań medycznych. Stop Co-Cr-Mo do powlekania i obrobione stopy co-Ni-Cr-Mo . American Society for Testing and Materials (ASTM) wymienia cztery stopy Co, które są zalecane do stosowania w implantach chirurgicznych: coating alloy Co-Cr-Mo (F75) i obrobione stopy Co-Cr-W-Ni (F90), Co-Ni-Cr-Mo (F562) i Co-Cr-Mo (F1537).
stopy te są klasą materiałów o wysokiej odporności na korozję w środowiskach fizjologicznych i na zużycie, przewyższając stal nierdzewną . Ponadto jego najwyższa granica wytrzymałości i odporność na zmęczenie umożliwiają jego zastosowanie tam, gdzie wymagana jest długa żywotność bez występowania złamań lub naprężeń/zmęczenia . Wiele właściwości pochodzi z krystalograficznego charakteru kobaltu, efektu wzmacniającego Cr i Mo oraz tworzenia węglików o wysokiej twardości .
takie szczególne właściwości doprowadziły do zastosowania tych stopów w różnych zastosowaniach medycznych, szczególnie w tych, które mają na celu zastąpienie powierzchni stawowych. Decydujące w tym wyborze są ich właściwości odporności na zużycie, korozję i niski współczynnik tarcia.
przykładem zastosowania jest artroplastyka stawu biodrowego (THA). Nowsze systemy składają się z pręta udowego przymocowanego do modularnej głowy podlegającej koordynacji z komponentem panewkowym . System ten jest znany jako MoM (metal na metalu) – w odniesieniu do powierzchni kontaktu – i jest lepszy niż systemy MoP (metal na polietylen), stosowane w odniesieniu do objętościowego tempa zużycia i innych parametrów do tej pory, jak podano w . Rysunek 2 przedstawia przykład systemów MOP i MoM dla THA.

Rysunek 2: po lewej: MoP; po prawej: Mama.
kolejnym przykładem zastosowania stopów Co, z którym praca ta jest bezpośrednio związana, jest całkowita rekonstrukcja stawu skroniowo-żuchwowego. Ten rodzaj protezy, znany jako proteza Christensena, jest w użyciu od ponad 30 lat i charakteryzuje się promowaniem stabilnej, niezawodnej i przewidywalnej odbudowy, zapewniającej zmniejszenie poziomu bólu, poprawę funkcjonalności i wyższy stopień ruchu . Rysunek 3 przedstawia protezę skroniowo-żuchwową.
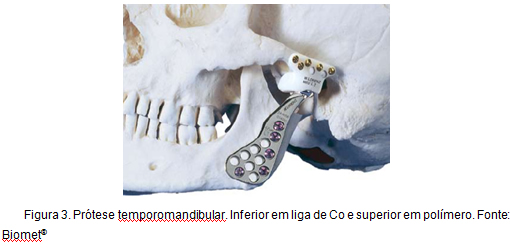
Rysunek 3: proteza skroniowo-Żuchwowa.
Stopy tytanu
Odkryte w 1791 roku przez Williama Gregora, brytyjskiego mineraloga, Tytan-a ostatnio jego stopy – są używane od dziesięcioleci w utrwalaniu złamań i rekonstrukcji stawów, ponieważ spełniają niezbędne wymagania w zastosowaniach biomedycznych, takich jak: odporność na ścieranie, biokompatybilność, bioadhezja (indukcja wzrostu kości), moduł sprężystości (im bliżej ludzkiej kości – 10-30 GPa -, tym lepiej), odporność na zmęczenie i dobra przetwarzalność , .
Tytan ma strukturę heksagonalną zamkniętą (hcp) związaną z fazą alfa, która może ulec zmianie alotropowej w temperaturze 881 ° c Dla sześciennej struktury centrowanej na ciele (bcc) znanej jako faza beta. Manipulacja tymi cechami krystalograficznymi poprzez dodanie spoiw i procesów termomechanicznych pozwala na uzyskanie stopów o różnych właściwościach.
klasy tytanu, które zostały początkowo wprowadzone jako biomateriały, to ASTM F67 (komercyjnie Czysty tytan w klasach 1, 2, 3 i 4), ASTM F136 (Stop Ti-6Al-4V Extra Low Interstitial) i ASTM F1472 (stop Ti-6Al 4W-standard) . W tych materiałach niektóre pierwiastki stopowe stabilizują fazę alfa, podczas gdy inne stabilizują fazę beta. Można ustabilizować fazę alfa, w tym aluminium, cyny i cyrkonu, podczas gdy faza beta może być stabilizowana z wanadu, molibdenu, niobu, chromu, żelaza i manganu . Należy zatem zauważyć, że Stop ASTM F136 jest przykładem stabilizowanego stopu alfa / beta.
część odporności na zużycie obserwowanej w tytanie i jego stopach wynika z tworzenia pasywnej warstwy tlenkowej składającej się głównie z TiO2, która przylega do powierzchni metalu i chroni go, a także jest w dużej mierze odpowiedzialna za biokompatybilność materiału. Warstwę tę można otrzymać przez anodowe utlenianie elektrolitu kwasu octowego, a gdy oceniana jest obecność tytanu w tkance przylegającej do implantu, jest ona znacznie mniejsza w anodowanym implancie w porównaniu do tych bez anodowania powierzchniowego .
ciężki uraz w strukturze twarzy wymaga dużej liczby płytek i śrub, a implanty tytanowe są szczególnie odpowiednie ze względu na właściwości wymienione w tym przeglądzie. Istnieją płytki i śruby do obszaru czaszkowo-szczękowo-twarzowego w różnych konfiguracjach, dzięki czemu lekarz może dostosować system do anatomii pacjenta. Rysunek 4 przedstawia przykład zastosowania tytanu w utrwalaniu złamań czaszkowo-szczękowo-twarzowych.

Rysunek 4: płytki do mocowania złamań czaszkowo-szczękowo-twarzowych.
inne zastosowanie , które demonstruje wszechstronność materiału, występuje w prętach śródszpikowych dla złamań kości piszczelowej zamkniętych i złożonych, gdzie implant (ryc. 5) jest wskazany w przypadku większych złamań kości i poddawanych większym obciążeniom mechanicznym (piszczeli).
Rysunek 5: wał śródszpikowy piszczelowy w Ti.
biomateriały Ceramiczne
rozwój materiałów ceramicznych do zastosowań biomedycznych koncentruje się głównie w dziedzinie ortopedii i stomatologii . Jest to klasa materiałów, która zawiera kilka cech biomateriałów. Ma przedstawicieli bio-obojętnych, biorezorbowalnych, bioaktywnych i porowatych klas wzrostu tkanek .
potencjał ceramiki jako biomateriałów wynika z jej podobieństwa do środowiska fizjologicznego, ze względu na podstawową budowę jonów, które znajdują się również w środowisku fizjologicznym (wapń, potas, magnez, sód itp.) i innych, których toksyczność jest bardzo ograniczona (cyrkon i tytan).
ceramika bio-obojętna jest bardziej reprezentatywna w związkach tlenku glinu (Al2O3), tlenku Cyrkonu (ZrO2) i tlenku cyrkonu stabilizowanego tlenkiem itru (ZrO2 (Y2O3)). Ich zdolność do nie reagowania z otaczającą tkanką, odporność na korozję, wysoka odporność na zużycie i wysoka odporność mechaniczna są podstawowymi cechami w ich zastosowaniu jako powierzchnie przegubowe narażone na obciążenia i tarcie.
w sercu bioaktywnej i bioresorbowalnej ceramiki można znaleźć związki takie jak hydroksyapatyt (HA), fosforany wapnia, zwłaszcza fosforan β-triwapniowy (β-TCP), a także bioglasy i ceramikę szklaną, których skład składa się z szerokiej gamy tlenków (SiO2, P2O5, Cao, CaF2, Na2O, Al2O3, m.in. ta2o5 i TiO2.) .
Park, J; Jeziora, R. S. „biomateriały-wstęp”. Springer. 3ª edição. 2007. s. 2.
„Zastosowanie przeszczepu, współpracowników i heterólogo w diáfise kości udowej myszy: porównanie przeszczepu zamarza i Lio”. Brazylijskiego czasopisma Ortopedii i Traumatologii. Marzec 2005 r.
Marzola, C; Toledo syn, J. L. „Podstawy Chirurgii Szczękowo-Twarzowej Buco-implanty, materiały aloplásticos”. Rozdział X.
Pereira, M. M, Buono, V. T. L; Zavaglia, C. A. C. „Materiały metalowe: Nauka i zastosowania jako biomateriały. In: Oréfice, R., Pereira, M. M; Mansour, H. S. „biomateriały: podstawy i zastosowania”. Rio de Janeiro. Kultura medyczna, 2006, rozdz. 2, p. 39-58.
Bath, S. V. „Biomaterials „” Dom Wydawniczy Naros. Nova Delhi, Indie. 2002. P. 181
Santos, Los Angeles „opracowanie fosforanu wapnia wzmocnionego włóknami do stosowania w medycynie i stomatologii”. Uniwersytet Stanowy Campinas. 2002.
Wong, J. and; Bronzinho, J. D. „Biomaterials”” Taylor e Francis Group. LLC. 2007. P. 1-1.
Barbucci, R. „Integrated Biomateriais Science”” Kluwer Academic / Plenum Publishers. Nova Iorque, 2002. CHAP. 6. P. 289-290.
Bertol, L. S. „Wkład w naukę szybkiego prototypowania, skanowania 3D i wybór materiałów, projektowanie implantów i niestandardowe”. Pracy magisterskiej. Universidade Federal do Rio Grande do Sul. Porto Alegre 2008.
Donachie M. „Metals Handbook Desk Edition”. Wydanie 2, zredagowane przez Davis, J. R. ASM International. 1998.
Disegi, J.; Kennedy, R. L; Pilliar, R. „Cobalt-Base Alloys for Biomedical Application”. ASTM STP 1365. 1999.
Shi, D. „Introduction to Biomaterials”. Tsinghua University Press, World Scientific. 2006. p – 123.
Marti, A. „Cobalt-base alloys used in bone surgery”. Injury-międzynarodowe czasopismo opieki nad poszkodowanymi. 2000 (31).
Wnek, G. E; Bowlin, G. L. „Encyclopedia of Biomaterials and Biomedical Engineering”. Vol 2. 2ª edição. Informa Healthcare. 2008.
Sieber, H. P; Rieker, C. B; Köttig, P. „Analysis of 118 second-generation metal-on-metal retrieved hip implants”. Journal of Bone & Joint Surgery (Br). 1998; 80-B: 46-50.
Garret, W. R; Abbey, P. A; Christensen, R. „Rekonstrukcja stawu skroniowo-żuchwowego za pomocą niestandardowej całkowitej protezy stawu skroniowo-żuchwowego: zastosowanie u pacjenta operowanego wielokrotnie”. A reprint from Surgical Technology International VI.
Leyens, C; Manfred, P. „Titanium and Titanium alloys: fundamentals and applications”. Wiley-VCH. Pierwsze wydanie. 2003. p-1.
Jaszemski, M. J; Tantrolo, D. J; Lewandrowski, K; Hasirci, V; Altobelli, D. E; Wise, D. L. „biomateriały w ortopedii”. Marcel Dekker Sp. Z O. O. 2004. p-2.
Lütjering, G; Williams, J. C. „Titanium – Engineering Materials and Processes. Springer-Verlag. Wydanie drugie. 2003. p-399.
Brown, S. A; Lemons, J. E. „Medical applications of titanium and its alloys: the material and biological issues”. Przebieg sympozjum, które odbyło się w 1994 roku w Phoenix w Arizonie. STP 1272 ASTM. 1996.
Brunette, D. M; Tengvall, P; Textor, m; Thomsen, P. „Titanium in medicine: material science, surface science, engineering, biological responses and medical applications”. Springer-Verlag. 2001. p – 28.
Larsson, C; Thomsen, P; Aronsson, B. O; Rodahl, M; Lausmaa, J; Kasemo, B; Ericson, L. E. „Bone response to surface-modified titanium implants: studies on the early tissue response to machined and electropolished implants with different oxide thicknesses”. Biomaterias 17 (1996) 605-616. Elsevier .
Jorgenson D. S; Centeno, J. A; Mayer M. H; Topper, M. J; Nossov, P. C; Mullick, F. G; Manson, p. n. „biologic response to passive dissolution of titanium craniofacial microplates”. Biomateriały 20 (1999) 675-682. Elsevier.
Zimmer Sirus® – System gwoździ śródszpikowych. Zimmer, 2007.
Shakelford, J. F. „Bioceramics – Advanced ceramics; V.1”. Gordon and Breach Science Publishers, 1999. p-5.
Hench, L. L. „Bioceramika: od koncepcji do kliniki”. J. Am. Ceram. Soc., 74 (7) 1487-510 (1991).
Hench, L. L; Wilson, J. „An introduction to Bioceramics”. World Scientific Publishing Co, 1993. p – 25.
Bubok, V. A. „Bioceramika-wczoraj, dziś, jutro”. Metalurgia proszków i ceramika metalowa, t. 39, nr 7-8, 2000.
konfigurowalne protezy
rekonstrukcja czaszkowo-szczękowo-twarzowa za pomocą szybkiego prototypowania
szybkie prototypowanie to technika wytwarzania części metodą addytywną. Model 3D stworzony w systemie CAD jest podzielony na profile 2D, które są następnie konstruowane przez urządzenia do szybkiego prototypowania warstwa po warstwie. Obecnie dostępnych jest kilka technik, takich jak: Stereolitografia (SLA), bezpośrednie spiekanie laserowe metali (DMLS), laserowe topienie powierzchni (LSM), Modelowanie osadzania stapianego (FDM), drukowanie 3D (3DP) i Spawanie wiązką elektronów (EBW) .
w pierwszej dekadzie stosowania techniki DMLS, od 1994 do 2004 roku, była ona zdominowana, przynajmniej w zastosowaniach komercyjnych, przez materiały opracowane specjalnie dla procesu DMLS, a mianowicie z naciskiem na poprawę przetwarzalności i właściwości akceptowalnych dla najczęstszych zastosowań. Obecnie dostępna jest szeroka gama stopów do stosowania w DML, takich jak lekkie stopy tytanu. Szczególnie interesujące w obszarze medycznym są Ti-6Al – 4V-tytan, aluminium, wanad i ticp-komercyjnie Czysty tytan. Oba charakteryzują się doskonałymi właściwościami mechanicznymi, odpornością na korozję, niską masą właściwą, a zwłaszcza biokompatybilnością .
tradycyjnie rapid prototyping (RP) jest stosowany w przemyśle i inżynierii jako środek do produkcji niezawodnych prototypów w krótkim czasie, co przynosi zyski w kosztach . W ostatnim czasie RP rozszerzyła swoje zastosowanie poza produkty inżynieryjne. Jego zastosowanie w medycynie do produkcji niestandardowych implantów i protez, badania anatomii i planowania chirurgicznego obejmują ważne dziedziny badawcze . Apelacja dotycząca dziedziny medycyny występuje w obliczu istotnych przeszkód, takich jak fakt, że przypadek nigdy nie jest sobie równy – dlatego standaryzacja w produkcji implantów nie jest korzystna – i kwestie dotyczące niejasnych punktów regionu operacji utrudniają planowanie chirurgiczne .
wśród wad wrodzonych anomalie czaszkowo-twarzowe (CFA) są grupą bardzo zróżnicowaną i złożoną, która wpływa na znaczną część ludzi na świecie .
oprócz przypadków wrodzonych deformacji, istnieją wady czaszkowo – twarzowe nabyte z powodu innych zaburzeń-na przykład guzów. W ciągu ostatnich czterech dekad obserwuje się również rosnącą liczbę przypadków urazów twarzy, co jest ściśle związane ze wzrostem liczby wypadków samochodowych i przemocy w miastach.
we wszystkich przypadkach rehabilitacja czaszkowo-szczękowo-twarzowa jest częścią procesu reintegracji pacjentów ze społeczeństwem i promocji dobrego samopoczucia.
szybkie prototypowanie w rekonstrukcji czaszki i twarzy
konwencjonalny sposób wytwarzania implantu do naprawy wady czaszki polega na bezpośrednim modelowaniu implantu w miejscu operacji podczas operacji. Drukowanie odbywa się w wosku, a następnie wykorzystywane do produkcji formy biomateriału . Pod koniec lat 80 .pojawiły się wyniki pierwszych badań, które próbowały znaleźć sposób na wytworzenie modelu fizycznego bezpośrednio z cyfrowego trójwymiarowego modelu.
szybkie prototypowanie to metoda produkcji warstwa po warstwie, która może wytwarzać złożoną geometrię z modelu CAD .
jego zastosowanie w zastosowaniach medycznych zrewolucjonizowało planowanie złożonych operacji poprzez budowę przedoperacyjnych modeli anatomicznych, które pozwalają personelowi medycznemu na krytyczną ocenę każdego konkretnego przypadku . Otrzymał również duży nacisk na jego zastosowanie w niestandardowej produkcji implantów do rekonstrukcji czaszki i wad twarzy,,,.
przy budowie niestandardowych implantów wymagane jest wprowadzanie danych pacjentów. Dane są uzyskiwane z CT lub NMRI w plastrach poprzecznych 2D w formacie DICOM, którego grubość jest określana na urządzeniu podczas uzyskiwania obrazów. Liczba plasterków decyduje o rozdzielczości obrazu, a tym samym o modelu 3D. Plasterki 2D są przenoszone na oprogramowanie do modelowania medycznego, gdzie możliwe jest dostosowanie sygnału progowego w celu uzyskania, po interpolacji, reprezentacji 3D struktury kości .
po uzyskaniu modelu można go obsługiwać w oprogramowaniu CAD do modelowania implantu, który naprawi wadę kości.
wzorzysta bryła jest następnie konwertowana do formatu STL i może być prototypowana dowolną techniką szybkiego prototypowania.
najnowsze zastosowania, materiały i opisy przypadków
w obszarze napraw czaszkowo-szczękowo-twarzowych odnotowano kilka przypadków skutecznego zastosowania technologii modelowania 3D i szybkiego prototypowania w celu uzyskania niestandardowych implantów.
donoszono o wykorzystaniu obrazów tomograficznych w uzyskaniu wirtualnego modelu 3D dla wirtualnej procedury resekcji części szczęki dotkniętej nowotworem i późniejszego projektu implantu w celu zastąpienia dotkniętego obszaru techniką odbijania przez płaszczyznę symetrii, gdzie zdrowa część szczęki jest odbijana i wykorzystywana w rekonstrukcji usuniętego obszaru.
Rysunek 7: uzyskanie modelu 3D i implantu (po lewej). Implant zbudowany przez DMLS (po prawej) .
implant został zbudowany z tytanu (Ti-6Al-4V) przy użyciu techniki bezpośredniego spiekania laserowego metalu (DMLS). W tym procesie sproszkowany metal jest topiony w stałą część poprzez lokalne topienie zapewniane przez wiązkę laserową o wysokiej energii kierowaną przez komputer zgodnie z projektem części.
po wyprodukowaniu implantu został on zeskanowany techniką skanowania 3D w celu porównania wymiarowego z modelem wirtualnym. Różnice nie były większe niż 0,05 mm, co świadczy o dokładności metody.
Drstvensek et al odnotowano również udane przypadki, które pokazują wielki potencjał szybkiego prototypowania w dziedzinie medycyny. W jednym zgłoszonym przypadku leczono ciężką asymetrię twarzy (mikrosomię połowiczną). Zastosowana metodologia była podobna do zastosowanej przez Bertol et al. Modele 3D uzyskano z obrazów CT, a implant został opracowany w środowisku wirtualnym poprzez odzwierciedlenie nienaruszonej części.
Rysunek 8: wirtualny model obszaru, który ma być skonstruowany (po lewej); Implant wyprodukowany przez DMLS .
w innym przypadku opisanym przez Drstvensek i wsp.zastosowano te same techniki w produkcji implantu czaszki i tylnego skanowania 3D w celu kontroli wymiarowej. W porównaniu z modelem wirtualnym implant wykazywał różnice w zakresie od 0,8 do 1,0 mm w niektórych regionach. Według autora, ze względu na fakt, że dany region nie znajduje się w krytycznej części, implant został zatwierdzony i pomyślnie wdrożony. Techniką prototypowania stosowaną w obu przypadkach był DMLS, a materiałem był Ti-6Al-4V.
Rysunek 9: Proteza produkowana przez DMLS (po lewej). Wynik wirtualnej kontroli geometrycznej (po prawej).
ostatnio kilka badań skupiło się na skojarzeniu właściwości w produkcji implantów. Dzieje się tak na przykład w połączeniu właściwości odporności mechanicznej i korozji tytanowej z bioaktywnością ceramiki, takiej jak HA i α-TCP.
Ning i Zhou ocenili bioaktywność in vitro i In vivo biokompozytu wytworzonego z proszków HA i Ti metodą metalurgiczną proszków. Mieszaniny w różnych proporcjach HA / Ti zmieszano i zsyntetyzowano w temperaturze 1200° C. Wyniki pokazują, że kompozyty o najwyższej zawartości Ti mają zdolność do indukowania zarodkowania i wzrostu apatytu na swojej powierzchni, co zapewnia wzrost kości i czyni biokompozyty metalowo-ceramiczne kandydatami do wymiany kości.
Kim i wsp.osadzali gęste i jednolite folie HA i FHA (fluoro hydroksyapatytu) o grubości ~ 5 µm w podłożach tytanowych techniką zol-żel. Substrat wykazywał korzystny wzrost i proliferację osteoblastów, zwiększając aktywność i funkcję substratu.
w ramach tej samej pracy Bertol zgłosił dwa przypadki ze skojarzeniem Ti i α-TCP. Zindywidualizowany implant otrzymano poprzez ręczne formowanie na fizycznym modelu pacjenta uzyskanym z obrazów tomograficznych (podłoga orbitalna), natomiast drugi poddano obróbce mechanicznej według projektu Wirtualnego również uzyskanego z obrazów tomograficznych (żuchwa). W obu przypadkach implanty zostały pokryte α-TCP i pomyślnie wdrożone.
Rysunek 10:
nie tylko Tytan, ale także stopy Co wykorzystują kompozyty ceramiczne w celu poprawy niektórych jego właściwości. Yen i wsp. raportują elektrolityczną powłokę Stopu Co-Cr-Mo z ZrO2 do protezy biodra. W tym przypadku zastosowanie powłoki zmniejszyło zużycie komponentu metalicznego względem komponentu polimerowego i zmniejszyło współczynnik tarcia między powierzchniami.
„Projektowanie niestandardowych implantów medycznych przez warstwową produkcję”. Szkoła Inżynierii Mechanicznej i systemów. Uniwersytet NC-Wielka Brytania.
Ma, D; Lin F; Chua C. K. ” Rapid Prototyping Applications in Medicine. Część 1: NURBS-Based Volume Modeling”. International Journal of Advanced Manufacturing Technology. Springer-Verlag London Limited. 2001
Lima, B. C. „Engenharia Reversa e Prototipagem Rápida: Estudo de Casos”. s. 15-16. 2003.
Shellabear, M; Nyrhilä, O. „DMLS-Development History and State of the Art”. LANE, Erlanger. 2004.
Shellabear, M; Nyrhilä, O. „Advances in Materials and Properties of Direct Metal Laser-Syntered Parts”. LANE, Erlanger. 2004.
Molleó, I. L. „anomalie czaszkowo-twarzowe, genetyka i zdrowie: wkład w rozpoznanie aktualnej sytuacji opieki w systemie opieki zdrowotnej”. Unicamp. 2004.
Lima Silva, J. J.; Lima, A. A., A. S.; Torres, S. M. „złamania twarzy: analiza 105 przypadków”. Czasopismo Brasileira de cirurgia Craniomaxilofacial / brazylijskie Stowarzyszenie chirurgii czaszki-szczękowo-twarzowej. – Vol.12, №1 (Jan.2009).
Gopakumar, S. „RP in medicine: a case study in skull reconstructive surgery”. Rapid Prototyping Journal. Tom 10 * Numer 3 * 2004 * s. 207-211.
Bertol, L. S. „wkład w naukę szybkiego prototypowania, skanowania 3D i wybór materiałów, projektowanie implantów i niestandardowe”. Pracy magisterskiej. Universidade Federal do Rio Grande do Sul. Porto Alegre 2008.
Naber, H. „Advances in rapid prototyping technologies”, Materials and Manufacturing Conference, Metalex, Thailand. 1998.
Gibson, i; Cheung, L. K; Chow, S. P; Cheung, W. L; Beh, S. L; Savalani, m; Lee, S. H. „the use of rapid prototyping to assist medical applications”. Rapid Prototyping Journal 12/1 (2006) 53-58.
Hench, L. L. „Bioceramika: od koncepcji do kliniki”. J. Am. Ceram. Soc., 74 (7) 1487-510 (1991).
Wu, w; Shang, Y; Li, H; Wang, W. „Fabrication of repairing skull bone defects based on the rapid prototyping”. Journal of Bioactive and Compatible Polymers, Vol. 24-Maj 2009r.
Bertol, L. s; Junior, W. K; Silva, F. P. d. ; Aumund-Kopp, C. „Medical design: Direct Metal laser sintering of Ti-6Al-4V”. Materiały i wzornictwo (2010), doi: 10.1016/j.matdes.2010.02.050.
Oliveira, R. S. d; Brigato, R; Madureira, J. F. G; Cruz, A. A. V; Filho, F. V. D. M; Alonso, N; Machado, H. R. „Reconstruction of a large complex skull defect in a child: a case report and literature review”. Childs Nerv Syst (2007) 23:1097-1102.
Drstvensek, I; Hren, N. i; Strojnik, T; Brajlih, T; Valentan, B; Pogacar, V; Hartner, T. Z. „Applications of Rapid Prototyping in Cranio-Maxilofacial Surgery Procedures”. Internacional Journal of Biology and Biomedical Engineering. Numer 1, tom 2, 2008.
ning, C. Q; Zhou, Y. „in vitro bioaktywność biokompozytu wytwarzanego z proszków HA i Ti metodą metalurgii proszków. Biomateriały 23 (2002) 2909-2915.
ning, C. Q; Zhou, Y. „korelacje między bioaktywnością in vitro i In vivo kompozytów Ti / HA wytwarzanych metodą metalurgii proszków”. Acta Biomaterialia 4 (2008) 1944-1952.