miocyt serca jest główną komórką biorącą udział w przebudowie. Fibroblasty, kolagen, śródstopie i naczynia wieńcowe w mniejszym stopniu również odgrywają rolę. Częstym scenariuszem przebudowy jest po zawale mięśnia sercowego. Istnieje martwica mięśnia sercowego (śmierć komórek) i nieproporcjonalne przerzedzenie serca. Ten cienki, osłabiony obszar nie jest w stanie wytrzymać ciśnienia i obciążenia objętościowego na serce w taki sam sposób, jak inne zdrowe tkanki. W rezultacie dochodzi do dylatacji Komory powstającej w rejonie zawału. Początkowa faza przebudowy po zawale mięśnia sercowego powoduje naprawę obszaru martwiczego i blizn mięśnia sercowego, które mogą być do pewnego stopnia uznane za korzystne, ponieważ występuje poprawa lub utrzymanie funkcji LV i pojemności minutowej serca. Z czasem jednak, gdy serce ulega ciągłej przebudowie, staje się mniej eliptyczne i bardziej kuliste. Zwiększenie masy komór i objętości, które razem niekorzystnie wpływają na czynność serca. Ostatecznie funkcja rozkurczowa lub zdolność serca do relaksu między skurczami może zostać upośledzona, co dodatkowo powoduje spadek.
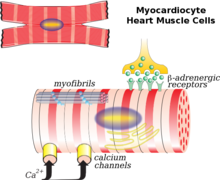
Po zawale mięśnia sercowego (MI) śmierć miocytów serca może być wywołana martwicą, apoptozą lub autofagią, co prowadzi do przerzedzenia ściany serca. Przetrwałe miocyty serca albo zorganizować równolegle lub szeregowo do siebie, przyczyniając się do rozszerzania komór lub przerost komór, w zależności od obciążenia stres na ścianie komory. Poza tym uważa się, że zmniejszona ekspresja mysoiny V1 i kanałów wapniowych typu L na miocytach serca powoduje również przebudowę serca. W normalnych warunkach ciała, kwasy tłuszczowe stanowią 60 do 90% zaopatrzenia w energię serca. Po MI, gdy utlenianie kwasów tłuszczowych zmniejsza się, prowadzi to do zmniejszenia podaży energii dla miocytów serca, nagromadzenia kwasów tłuszczowych do poziomu toksycznego i dysfunkcji mitochondriów. Konsekwencje te doprowadziły również do wzrostu stresu oksydacyjnego na serce, powodując proliferację fibroblastów, aktywację metaloproteinaz i indukcję apoptozy, co zostanie wyjaśnione poniżej. Poza tym, zapalna odpowiedź immunologiczna po MI również przyczynia się do powyższych zmian.
poza tym, śródstopie serca, które składa się w dużej mierze z włókien kolagenowych typu I i typu III, bierze również udział w przebudowie serca. Kolagen sercowy jest syntetyzowany przez fibroblasty i rozkładany przez metaloproteinazy. Fibroblasty są aktywowane po MI, co prowadzi do zwiększonej syntezy kolagenu i zwłóknienia serca. Zwiększenie ekspresji MMP1 i MMP9 doprowadziło do degradacji włókien kolagenowych, a następnie rozszerzenia serca. Wiadomo, że kilka szlaków sygnałowych, takich jak angiotensyna II, transformujący czynnik wzrostu beta (TGF-beta) i Endotelina 1, powoduje syntezę i degradację włókien kolagenowych w sercu.
inne czynniki, takie jak wysokie ciśnienie krwi, aktywacja układu współczulnego, który uwalnia noradrenalinę, aktywacja układu renina–angiotensyna, który uwalnia reninę i hormony antydiuretyczne, są ważnymi czynnikami przebudowy serca. Uważa się jednak, że atrialny peptyd natriuretyczny jest kardiochirurgiczny.