Biomaterials
det är möjligt att avgränsa studien av biomaterial genom en mycket allmän men sammanhängande definition av Park och sjöar . Enligt dem kan ett biomaterial definieras som vilket material som helst som används vid tillverkning av anordningar för att ersätta en del eller funktion av kroppen på ett säkert, pålitligt, ekonomiskt och fysiologiskt acceptabelt sätt.
för att på ett tillfredsställande sätt kunna utföra funktionen att ersätta, förstora eller stödja en struktur måste implantatet efterlikna eller matcha vävnadens egenskaper. Litteraturen rapporterar förekomsten av olika typer av bentransplantat som används i implantat: autologa (härledda från samma individ); homologa (från en individ av samma art av mottagaren); och heterologa (när givarens och mottagarens Art inte är samma – nötkreatur, till exempel ).
autologa transplantat har vissa nackdelar, till exempel: intervention i ett hälsosamt område av patientens kropp; givarområdet sjuklighet, högre återhämtningsperiod; mottaglighet för infektioner; och progressiv och konstant resorption . Således har implantat i syntetiska biomaterial såsom keramik och polymerer utvecklats och applicerats i stor utsträckning. Enligt Pereira, Buono och Zavaglia har efterfrågan på biomaterial ökat från 5 till 15% varje år.
klassificering av biomaterial
enligt Bath och Santos kan biomaterial klassificeras i fyra klasser , beroende på kompatibiliteten de har med omgivande vävnader:
Biotolerant: implantat separerat från det omgivande benet med ett lager mjukvävnad över gränssnittet. Ingen kontakt i osteogenesen. Skiktet induceras av implantatfrisättning av monomerer, joner och/eller korrosionsprodukter. Nästan alla syntetiska polymerer och de flesta metaller är denna kategori.
Bioinert: Implantat i direkt kontakt med benvävnad, som förekommer involvering i osteogenesen. Det finns emellertid ingen kemisk reaktion mellan vävnaden och implantatet. Det finns inte, åtminstone i mängder som kan detekteras av celler, frisättningen av någon komponent. Exempel på bioinert biomaterial är: aluminiumoxid, zirkoniumoxid, Titan, tantal, niob och kol.
bioaktiv: det finns interaktionen mellan implantatet och benvävnaden, som stör direkt i osteogenesen. Genom kemisk likhet binder mineraldelen av benvävnad till implantatet, vilket främjar osteokonduktion. Huvudmaterialen i denna klass är: Ca-fosfat, vitro-keramik och hydroxiapatit.
bioresorberbara: material som efter en viss tidsperiod i kontakt med vävnaderna hamnar genom att degraderas, solubiliseras eller fagocyteras av kroppen. De är av intresse för kliniska tillämpningar där det inte är tillrådligt att reoperationen tar bort implantatet. Representant för denna klass är trikalciumfosfat (TCP) och PLLA (poly-L-mjölksyra).
metalliska biomaterial
ibland tolereras metalliska element i sina naturliga former och i små mängder av kroppen, såsom järn (Fe) i röda blodkroppar, kobolt (Co) i syntesen av vitamin B12 och i tvärbindningarna av elastin som finns i aortaartären . Men i stora mängder tolereras de flesta metaller inte av kroppen.
vissa metaller används som substitut för hårda vävnader, till exempel i totala höft-och knäbyten, plattor och skruvar för fixering av frakturer, kolonnfixeringsanordningar och tandimplantat på grund av deras utmärkta mekaniska egenskaper och korrosionsbeständighet . Enligt Barbucci bör ett metallmaterial som används vid konstruktion av ortopediska proteser, osteosyntesanordningar och tandimplantat ha följande egenskaper:
- Gränsmotstånd lika med eller större än 800 MPa;
- korrosionsbeständighet (lokal och allmän);
- biokompatibilitet.
biokompatibilitet är inte en effekt eller ett unikt fenomen. Det hänvisar till en rad processer som involverar olika interaktionsmekanismer men ömsesidigt beroende av material och vävnad. Det är materialets förmåga att utföra en specifik funktion i kroppen utan att orsaka toxiska eller skadliga effekter på de biologiska systemen .
dessa egenskaper är så restriktiva att endast ett litet antal klasser av metalliska material kan användas framgångsrikt.
den första legeringen speciellt utvecklad för användning i människokroppen var” vanadinstål”, som användes för tillverkning av plattor och skruvar för benfrakturer . Bland de metalliska biomaterialen är austenitiska rostfria stål av typ 316 LVM, legeringar Co-Cr-Mo, Co-Ni-Cr-Mo, ren titan och Ti-6Al-4V de mest använda . Några exempel visas i Figur 1.

Figur 1: metalliska anordningar för medicinsk tillämpning: a) Lårbenshuvud; b) överlägsen artikulation knä; c) mandibulär ledplatta.
I detta arbete kommer vi att ta itu med mer specifikt legeringar Co och Ti, vars tillämpning i dmls snabba prototyper inom det medicinska området är mer uttrycksfull.
Koboltlegeringar
Koboltlegeringar föreslogs ursprungligen för kirurgiska implantat för mer än 70 år sedan . Det finns i princip två typer av Co-legeringar för medicinsk tillämpning. Legeringen Co-Cr-Mo för beläggning och de bearbetade legeringarna Co-Ni-Cr-Mo . American Society for Testing and Materials (ASTM) listar fyra Co-legeringar som rekommenderas för användning i kirurgiska implantat: coating alloy Co-Cr-Mo (F75) och bearbetade legeringar Co-Cr-W-Ni (F90), Co-Ni-Cr-Mo (F562) och Co-Cr-Mo (F1537).
dessa legeringar är en klass av material som är mycket resistenta mot korrosion i fysiologiska miljöer och att bära, överträffar rostfritt stål . Dessutom möjliggör dess överlägsna motståndsgräns och utmattningsbeständighet dess applicering där lång livslängd utan förekomst av frakturer eller stress/trötthet krävs . Många egenskaper härstammar från koboltens kristallografiska natur, boostereffekten av Cr och Mo, och karbiderna bildar hög hårdhet .
sådana speciella egenskaper har lett till användningen av dessa legeringar i olika medicinska tillämpningar, särskilt i de som syftar till att ersätta ledytorna. Deras egenskaper för slitstyrka, korrosion och låg friktionskoefficient är avgörande i detta val.
ett exempel på applikation är den totala Höftartroplastiken (THA). De nyare systemen består av en femoral stav fäst vid ett modulärt huvud som är föremål för samordning med den acetabulära komponenten . Detta system är känt som MoM (metall på metall) – med hänvisning till kontaktytan – och är bättre än MoP (metall på polyeten) system, som används i förhållande till den volymetriska slitagehastigheten och andra parametrar hittills, som rapporterats i . Figur 2 visar ett exempel på MOP och mamma system för THA.

Figur 2: till vänster: MoP; till höger: Mamma.
ett annat exempel på applicering av Co-legeringar, som detta arbete är direkt relaterat till, är den totala rekonstruktionen av den temporomandibulära leden. Denna typ av protes, känd som Christensen protes, har använts i över 30 år och kännetecknas av främjandet av en stabil, pålitlig och förutsägbar rekonstruktion, vilket ger minskning av smärtnivån, förbättring av funktionaliteten och högre grad av rörelse . Figur 3 illustrerar en temporomandibulär protes.
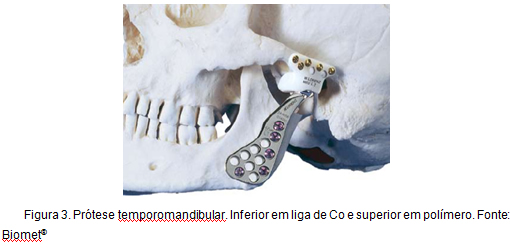
Figur 3: temporomandibulär protes.
titanlegeringar
upptäckt 1791 av William Gregor, en brittisk mineralog, titan-och mer nyligen dess legeringar-har använts i årtionden vid fixering av frakturer och gemensam rekonstruktion eftersom den uppfyller de nödvändiga kraven för biomedicinska tillämpningar, såsom: slitstyrka, biokompatibilitet, bioadhesion( induktion av bentillväxt), elasticitetsmodul (ju närmare det mänskliga benet-10-30 GPa -, desto bättre), utmattningsbeständighet och god bearbetbarhet,.
Titan har en hexagonal sluten packad (hcp) struktur som hänför sig till alfafasen, som kan genomgå en allotrop förändring vid 881 kcal C för den kroppscentrerade kubiska (bcc) strukturen som kallas betafasen. Manipuleringen av dessa kristallografiska egenskaper genom tillsats av bindemedel och termomekaniska processer möjliggör erhållande av legeringar med olika egenskaper.
titanklasserna som ursprungligen introducerades som biomaterial var ASTM F67 (kommersiellt rent titan i klass 1, 2, 3 och 4), ASTM F136 (legering Ti-6Al-4V Extra låg interstitiell) och ASTM F1472 (legering Ti-6Al 4W-standard) . I dessa material stabiliserar vissa legeringselement alfafasen medan andra stabiliserar betafasen. Man kan stabilisera alfafasen genom att inkludera aluminium, tenn och zirkonium, medan betafasen kan stabiliseras med vanadin, molybden, niob, krom, järn och mangan . Det noteras därför att legeringen ASTM F136 är ett exempel på stabiliserad alfa/beta-legering.
en del av slitstyrkan observerad i titan och dess legeringar beror på bildandet av ett passivt oxidskikt som huvudsakligen består av TiO2 som fäster vid metallens yta och skyddar den, förutom att den till stor del är ansvarig för materialets biokompatibilitet. Detta skikt kan erhållas genom anodisk oxidation i ättiksyraelektrolyt och, när närvaron av titan i vävnad intill implantatet utvärderas, det är väsentligt mindre i det anodiserade implantatet jämfört med de utan ytanodisering,.
allvarligt trauma i ansiktsstruktur kräver ett stort antal plattor och skruvar, och titanimplantaten är särskilt lämpliga på grund av de egenskaper som nämns i denna översyn. Det finns plattor och skruvar för kranio-maxillofacialområdet i olika konfigurationer så att läkaren kan anpassa systemet till patientens anatomi. Figur 4 är ett exempel på applicering av titan vid fixering av kranio-maxillofaciala frakturer.

Figur 4: plattor för fixering av kranio-maxillofaciala frakturer.
en annan applikation som visar materialets mångsidighet förekommer i de intramedullära stavarna för tibia stängd och sammansatt fraktur , där implantatet (Figur 5) indikeras för större benfrakturer och utsätts för större mekaniska påkänningar (tibia).
Figur 5: Tibial intramedullär axel i Ti.
keramiska biomaterial
utvecklingen av keramiska material för biomedicinska tillämpningar fokuserar främst inom områdena ortopedi och tandvård . Det är en klass av material som innehåller flera funktioner i biomaterial. Det har representanter för de bio-inerta, bioresorberbara, bioaktiva och porösa klasserna för vävnadstillväxt .
keramikens potential som biomaterial kommer från dess likhet med den fysiologiska miljön på grund av dess grundläggande sammansättning av joner som också finns i fysiologisk miljö (kalcium, kalium, magnesium, natrium, etc.) och andra vars toxicitet är mycket begränsad (zirkonium och Titan) .
den bioinerta keramiken är mer representativ i föreningarna av aluminiumoxid (Al2O3), zirkoniumoxid (ZrO2) och zirkoniumoxid stabiliserad med yttriumoxid (ZrO2 (Y2O3)). Deras förmåga att inte reagera med den omgivande vävnaden, korrosionsbeständighet, hög slitstyrka, och hög mekanisk beständighet är viktiga funktioner i deras användning som ledade ytor utsätts för belastningar och friktion , .
I hjärtat av bioaktiv och bioresorberbar keramik kan man hitta föreningar som hydroxiapatit (HA), kalciumfosfater, särskilt den sackarios-trikalciumfosfat (sackarios-TCP), liksom bioglasser och glaskeramik, vars sammansättning består av ett omfattande spektrum av oxider (SiO2, P2O5, CaO, CaF2, Na2O, Al2O3, Ta2O5 och TiO2, bland andra.) .
Park, J; sjöar, R. S.”biomaterial – en introduktion”. Springer. 3 msk. 2007. s. 2.
G. A., C. A., et al. ”Användning av homologt och heterologt transplantat i femoral diafys hos råttor: jämförelse mellan fryst och lyofiliserat bentransplantat”. Brasiliansk tidskrift för ortopedi och traumatologi. Mars 2005.
Marzola, C; Toledo Filho, Jl ”fundamentals of Oral Maxillofacial Surgery-implantat av alloplastiska material ””Kapitel X.
Pereira, m; Buono, VTL; Zavaglia, CAC” metalliska material: vetenskap och tillämpning som biomaterial. I: Orefice, R. A; Pereira, M. M; Mansur, H. S. ”biomaterial: fundamenta och tillämpningar”” Rio De Janeiro. Medicinsk kultur, 2006, Kap. 2, s. 39-58.
Bad, S. V.”biomaterial”. Narosa Förlag. Nova Dheli, Indien. 2002. s.181
Santos, L. A. ” utveckling av kalciumfosfatrefor i fråga om vad som är nödvändigt för att göra det möjligt att göra det.”Tese de Doutorado. State University of Campinas. 2002.
Wong, J. y; Bronzinho, J. D. ”biomaterial”. Taylor och Francis grupp. LLC. 2007. s. 1-1.
Barbucci, R. ”integrerad Biomateriais vetenskap”. Kluwer Akademiska / Plenum Förlag. New York.2002. kille.6. s. 289-290.
Bertol, L. S. ”Bidrag till studien av snabb prototypning, tredimensionell digitalisering och materialval i utformningen av anpassade implantat”” Master ’ s dissertation. Federala universitetet i Rio Grande do Sul. Porto Alegre. 2008.
Donachie M. ”metaller handbok skrivbord Edition”. 2: a upplagan, redigerad av Davis, Jr ASM International. 1998.
Disegi, J. A; Kennedy, R. L; Pilliar, R. ”kobolt-Baslegeringar för biomedicinsk tillämpning”. ASTM-STP 1365. 1999.
Shi, D. ”introduktion till biomaterial”. Tsinghua University Press, Världens Vetenskapliga. 2006. p-123.
Marti, A. ”kobolt-baslegeringar som används vid benoperation”. Skada-internationell tidskrift för vård av skadade. 2000 (31).
Wnek, G. E; Bowlin, G. L.”Encyclopedia of Biomaterials and Biomedical Engineering”. Vol 2. 2 msk. Informa Healthcare. 2008.
Sieber, H. P; Rieker, C. B; K Jacobttig, P. ”analys av 118 andra generationens metall-på-metall-hämtade höftimplantat”. Journal of Bone & Ledkirurgi (Br). 1998; 80-B: 46-50.
Garret, W. R; Abbey, P. A; Christensen, R. ”Temporomandibulär ledrekonstruktion med en anpassad Total temporomandibulär ledprotes: användning i den multiplicerade opererade patienten”. En nytryck från Surgical Technology International Vi.
Leyens, C; Manfred, P. ”Titan och titanlegeringar: fundamentals and applications”. Wiley-VCH. Första upplagan. 2003. p-1.
Yaszemski, M. J; Tantrolo, D. J; Lewandrowski, K; Hasirci, V; Altobelli, D. E; Wise, D. L. ”biomaterial i ortopedi”. Marcel Dekker Inc. 2004. p-2.
l Brasilitjering, G; Williams, J. C. ” Titan – tekniska material och processer. Springer-Verlag. Andra upplagan. 2003. p-399.
Brown, sa; citroner, je ”medicinska tillämpningar av titan och dess legeringar: materialet och biologiska problem”. Proceedings of a symposium hölls 1994 i Phoenix, Arizona. STP 1272. ASTM. 1996.
Brunett, D. M; Tengvall, P; Textor, m; Thomsen, P. ”Titan i medicin: materialvetenskap, ytvetenskap, teknik, biologiska svar och medicinska tillämpningar”. Springer-Verlag. 2001. p-28.
Larsson, C; Thomsen, P; Aronsson, B. O; Rodahl, M; Lausmaa, J; Kasemo, B; Ericson, L. E. ”Benrespons på ytmodifierade titanimplantat: studier av det tidiga vävnadssvaret på bearbetade och elektropolerade implantat med olika oxidtjocklekar”. Biomaterias 17 (1996) 605-616. Elsevier .
Jorgenson D. S; Centeno, J. A; Mayer M. H; Topper, M. J; Nossov, P. C; Mullick, F. G; Manson, P. N. ”biologiskt svar på passiv upplösning av Titan kraniofaciala mikroplattor”. Biomaterial 20 (1999) 675-682. Elsevier.
Zimmer Sirus – intramedullär Nagelsystem. Zimmer, 2007.
Shakelford, J. F.”Bioceramics – avancerad keramik; v.1″. Gordon och Breach Science Publishers, 1999. p-5.
Hench, ll ”Bioceramics: från koncept till klinik”. J. Am. Ceram. Soc., 74 (7) 1487-510 (1991).
Hench, L. L; Wilson, J.”En introduktion till Bioceramics”. World Scientific Publishing Co, 1993. p – 25.
Bubok, V. A.”Bioceramics – Igår, Idag, Imorgon”. Pulvermetallurgi och metallkeramik, Vol. 39, nr 7-8, 2000.
anpassningsbara proteser
Cranio-maxillofacial rekonstruktion via rapid prototyping
Rapid prototyping är tekniken för tillverkning av delar med tillsatsmetoden. En 3D-modell skapad i ett CAD-system delas in i 2D-profiler som sedan konstrueras genom snabb prototyputrustning lager för lager. Flera tekniker finns idag, såsom: Stereolitografi (SLA), Direktmetalllasersintrering (DML), Laser Ytsmältning (LSM), smält Deponeringsmodellering (FDM), 3D-utskrift (3DP) och Elektronstrålesvetsning (EBW) .
under det första decenniet av användningen av DMLS-tekniken, från 1994 till 2004, dominerades den, åtminstone i sina kommersiella tillämpningar, av material som utvecklats specifikt för DMLS-processen, nämligen med fokus på förbättringar i bearbetbarhet och egenskaper som är acceptabla för de vanligaste applikationerna. Numera finns ett brett utbud av legeringar tillgängliga för användning i DML, såsom lätta legeringar av Titan. Av särskilt intresse inom det medicinska området är Ti-6Al – 4V – titan, aluminium, vanadin och Ticp-kommersiellt rent titan. Båda kännetecknas av deras utmärkta mekaniska egenskaper, korrosionsbeständighet, låg specifik vikt och särskilt av dess biokompatibilitet .
traditionellt används rapid prototyping (Rp) inom industri och teknik som ett sätt att producera pålitliga prototyper på kort tid, vilket ger vinster i kostnad . Nyligen har RP utvidgat sin tillämpning utöver tekniska produkter. Dess användning inom det medicinska området till tillverkning av anpassade implantat och proteser, studiet av anatomi, och kirurgisk planering inkluderar viktiga forskningsområden . Överklagandet om det medicinska området uppstår inför betydande hinder, till exempel det faktum att ett fall aldrig är lika med varandra – varför standardisering i produktionen av implantat inte är fördelaktig – och frågor om de obskyra punkterna i operationsområdet gör kirurgisk planering svår .
bland de medfödda defekterna är kraniofaciala anomalier (CFA) en grupp som är mycket varierande och komplex som påverkar en betydande andel människor i världen .
förutom fall av medfödda deformiteter finns kraniofaciala defekter förvärvade på grund av andra störningar – tumörer, till exempel. Under de senaste fyra decennierna har en växande mängd fall av ansiktstrauma också observerats, vilket är nära kopplat till ökningen av bilolyckor och stadsvåld.
I alla fall är kranio-maxillofacial rehabilitering en del av processen för återintegrering av patienter i samhället och främjande av välbefinnande.
Rapid prototyping in skull and face reconstruction
det konventionella sättet att tillverka ett implantat för reparation av kranialdefekt består i direkt modellering av implantatet på operationsstället under operationen. Tryckningen görs i vax och används därefter vid tillverkning av en biomaterialform . I slutet av 1980-talet framkom resultaten av den första forskningen som försökte hitta ett sätt att producera en fysisk modell direkt från en digital tredimensionell modell .
Rapid prototyping är en tillverkningsmetod lager för lager som kan producera komplex geometri från en CAD-modell .
dess användning i medicinska tillämpningar har revolutionerat planeringen av komplexa operationer genom konstruktion av preoperativa anatomiska modeller som gör det möjligt för medicinsk personal att få en kritisk utvärdering av varje enskilt fall . Det har också fått stor vikt vid dess användning vid anpassad tillverkning av implantat för rekonstruktion av skallen och ansiktsbrister , , , , .
vid konstruktion av anpassade implantat krävs inmatning av patientdata. Data erhålls från CT eller NMRI i 2D tvärgående skivor i DICOM-format, vars tjocklek bestäms på utrustningen när bilderna erhålls. Antalet skivor är det som bestämmer bildupplösningen och därmed 3D-modellen. 2D-skivorna överförs till den medicinska modelleringsprogramvaran där det är möjligt att justera tröskelsignalen för att efter interpolering erhålla en 3D-representation av benstrukturen,.
efter erhållandet av modellen kan den hanteras i CAD-programvara för modellering av implantatet som kommer att reparera bendefekten.
det mönstrade fasta ämnet konverteras sedan till STL-formatet och kan prototypas med alla snabba prototyptekniker.
nya applikationer, material och fallrapporter
I kranio-maxillofacial reparationsområdet har flera fall av framgångsrik tillämpning av 3D-modelleringsteknik och snabb prototypning för att ha anpassade implantat rapporterats.
Bertol et al. rapporterade användningen av tomografibilder för att få en virtuell 3D-modell för virtuell resektionsprocedur av en del av käken som påverkas av en tumör och efterföljande implantatdesign för att ersätta den drabbade regionen med tekniken för spegling med symmetriplan, där den friska delen av käken speglas och används vid rekonstruktionen av den borttagna regionen.
Figur 7: Erhållande av 3D-modellen och implantatet (till vänster). Implantat byggt av DML (till höger) .
implantatet byggdes i Titan (Ti-6Al-4V) med hjälp av tekniken för direkt Metalllasersintrering (DML). I denna process smälts den pulveriserade metallen till en fast del genom den lokala smältningen som tillhandahålls av en laserstråle med hög energi riktad av datorn enligt delens utformning.
efter tillverkningen av implantatet skannades det med 3D-skanningstekniken för dimensionell jämförelse med den virtuella modellen. Skillnaderna var inte större än 0,05 mm, vilket visar metodens noggrannhet.
Drstvensek et al rapporterade också framgångsrika fall som visar den stora potentialen för snabb prototypning inom det medicinska området. I ett rapporterat fall behandlades en allvarlig ansiktsasymmetri (hemifacial mikrosomi). Den använda metoden liknade den som användes av Bertol et al. 3D-modeller erhölls från CT-bilder och implantatet utvecklades i virtuell miljö genom att spegla den opåverkade delen.
figur 8: virtuell modell av området som ska konstrueras (till vänster); implantat tillverkat av DMLS .
I ett annat fall rapporterat av Drstvensek et al användes samma tekniker vid tillverkning av ett skallimplantat och bakre 3D-skanning för dimensionell kontroll. I jämförelse med den virtuella modellen visade implantatet variationer på 0,8 till 1,0 mm i vissa regioner. Enligt författaren, på grund av att regionen i fråga inte ligger i en kritisk del, godkändes implantatet och genomfördes framgångsrikt. Prototyptekniken som användes i båda fallen var DML och materialet var Ti-6Al-4V.
Figur 9: Protes Tillverkad av DML (till vänster). Resultat av den virtuella geometriska inspektionen (till höger).
nyligen har flera studier fokuserat på egenskapsföreningen vid tillverkning av implantat. Detta sker till exempel i kombinationen av mekaniska resistansegenskaper och titankorrosion med bioaktiviteten hos keramik såsom HA och bisexuell-TCP.
Ning och Zhou , utvärderade bioaktiviteten in vitro och in vivo av biokomposit framställd av HA-och Ti-pulver med pulvermetallurgisk metod. Blandningar i olika proportioner av HA/Ti blandades och syntetiserades vid 1200 kcal C. resultaten visar att kompositerna med det högsta Ti-innehållet har förmågan att inducera kärnbildning och tillväxt av apatit på deras yta, vilket ger bentillväxt och gör metall/keramiska biokompositer kandidater för benbyte.
Kim et al deponerade täta och likformiga filmer av HA och FHA (hydroxyapatit-fluoro) med tjocklek ~ 5 OC i titansubstrat med användning av sol-gel-tekniken. Substratet presenterade gynnsam tillväxt och proliferation av osteoblaster, vilket ökar substratets aktivitet och funktion.
längs samma arbetslinje rapporterade Bertol två fall med sammanslutningen av Ti och XHamster-TCP. Ett anpassat implantat erhölls genom manuell gjutning på patientens fysiska modell erhållen från tomografiska bilder (orbitalgolv), medan den andra bearbetades enligt den virtuella designen också erhållen från tomografiska bilder (mandible). I båda fallen, implantaten belades med Macau-TCP och framgångsrikt genomfört.
Figur 10:
inte bara Titan utan även Co-legeringarna har använt keramikkompositer för att förbättra några av dess egenskaper. Yen et al rapporterar den elektrolytiska beläggningen av en legering Co-Cr-Mo med ZrO2 till en höftprotes. I detta fall minskade appliceringen av beläggningen slitage på metallkomponenten mot polymerkomponenten och minskade friktionskoefficienten mellan ytorna.
Khan, S. F.; Dalgarno K. W. ”Design av anpassade medicinska implantat genom skiktad tillverkning”. Skolan för mekanik och systemteknik. NC University-Storbritannien.
Ma, D; Lin F; Chua ck ”Rapid Prototyping Applications in Medicine. Del 1: NURBS-baserad Volymmodellering”. International Journal of Advanced Manufacturing Technology. Springer – Verlag London Limited. 2001
Lima, B. C. ”Engenharia Reversa e Prototipagem r Auccipida: Estudo de Casos”. pp 15-16. 2003.
Shellabear, M; Nyrhilyubbi, O. ”DMLS-utvecklingshistoria och toppmodern”. LANE, Erlanger. 2004.
Skalbjörn, M; Nyrhilyubbi, O. ”framsteg i material och egenskaper hos Direktmetalllasersynterade delar”. LANE, Erlanger. 2004.
Molle Brasilian, Il ”kraniofaciala anomalier, genetik och folkhälsa: bidrag till erkännandet av den nuvarande vårdsituationen i Unified Health System”” Unicamp. 2004.
Lima Silva, JJ de; Lima, AA s; Torres, SM” ansiktsfrakturer: analys av 105 fall” ” Revista Brasileira de Cirurgia Craniomaxilofacial / Brazilian Association of Cranio-Maxillofacial Surgery. – Vol.12, Nr 1 (Jan.2009).
Gopakumar, S. ” RP i medicin: en fallstudie i kranial rekonstruktiv kirurgi ”” Rapid Prototyping Journal. Volym 10 * nummer 3 * 2004 * s. 207-211.
Bertol, L. S. ”bidrag till studiet av snabba prototyper, tredimensionell digitalisering och val av material i utformningen av anpassade implantat”” Master avhandling. Federala universitetet i Rio Grande do Sul. Porto Alegre. 2008.
Naber, H. ”framsteg inom rapid prototyping technologies”, material-och Tillverkningskonferens, Metalex, Thailand. 1998.
Gibson, i; Cheung, L. K; Chow, S. P; Cheung, W. l; väl, S. L; Savalani, m; Lee, S. H. ”användningen av snabba prototyper för att hjälpa medicinska tillämpningar”. Rapid Prototyping Journal 12/1 (2006) 53-58.
Hench, ll ”Bioceramics: från koncept till klinik”. J. Am. Ceram. Soc., 74 (7) 1487-510 (1991).
Wu, W; Shang, Y; Li, H; Wang, W. ”tillverkning av reparation av skallbenfel baserat på snabb prototypning”. Journal of Bioactive och kompatibla polymerer, Vol. 24-maj 2009.
Bertol, L. S; Junior, W. K; Silva, F. P. d. ; Aumund-Kopp, C.”medicinsk design: direkt metall laser sintring av Ti-6Al-4V”. Material och Design (2010), doi: 10.1016/j.matdes.2010.02.050.
Oliveira, R. S. D; Brigato, R; Madureira, J. F. g; Cruz, A. A. V; Filho, F. V. d. M; Alonso, N; Machado, HR ”rekonstruktion av en stor komplex skallefel hos ett barn: en fallrapport och litteraturöversikt”. Childs Nerv Syst (2007) 23:1097-1102.
Drstvensek, i; Hren, N. i; Strojnik, T; Brajlih, T; Valentan, B; Pogacar, V; Hartner, TZ ”tillämpningar av snabb prototypning vid kranio-Maxilofacial kirurgi”. Internacional Journal of Biology och biomedicinsk teknik. Utgåva 1, volym 2, 2008.
Ning, C. Q; Zhou, Y. ” in vitro bioaktivitet av en biokomposit Tillverkad av HA-och Ti-pulver med pulvermetallurgimetod. Biomaterial 23 (2002) 2909-2915.
Ning, C. Q; Zhou, Y.”korrelationer mellan in vitro och in vivo bioaktiviteten hos Ti/HA-kompositerna tillverkade med en pulvermetallurgimetod”. Acta Biomaterialia 4 (2008) 1944-1952.