A Microbial Biorealm page on the genus Citrobacter freundii
Classification
Higher order taxa
Bacteria; Proteobacteria; Gammaproteobacteria; Enterobacteriales; Enterobacteriaceae; Citrobacter
Species
NCBI: Taxonomy
Citrobacter Freundii
Description and significance
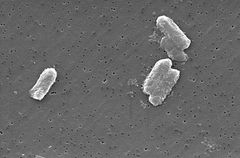 Photo: Pete Wardell / CDC
Photo: Pete Wardell / CDC
Citrobacter-arterna, inklusive Citrobacter freundii, är aeroba gramnegativa baciller. Citrobacter freundii är långa stavformade bakterier som vanligtvis är 1-5 kcal långa . De flesta C. freundii-celler är omgivna av många flageller som används för att röra sig, men några är icke-rörliga. Dess livsmiljö inkluderar miljön (jord, vatten, avlopp), mat och tarmkanalerna hos djur och människor . Det tillhör familjen Enterobacteriaceae.
som en opportunistisk patogen är C. freundii ansvarig för ett antal signifikanta opportunistiska infektioner. Det är känt att vara orsaken till en mängd olika nosokomiala infektioner i luftvägarna, urinvägarna, blodet och flera andra normalt sterila platser hos patienter . C. freundii representerar cirka 29% av alla opportunistiska infektioner . Därför är en av de främsta orsakerna till att många olika stammar och plasmider av C. freundii-genomet sekvenseras för att hitta antibiotika som kan bekämpa dessa opportunistiska infektioner.
överraskande spelar denna smittsamma mikrobe hos människor en positiv roll i miljön. C. freundii ansvarar för att minska nitrat till nitrit i miljön . Denna avgörande omvandling är ett viktigt steg i kvävecykeln. Och återvinning av kväve är mycket viktigt eftersom jordens atmosfär är cirka 85% kväve . På grund av dess viktiga bidrag till miljön är därför en annan motivation för att sekvensera genomet av C. freundii.släktet Citrobacter upptäcktes 1932 av Werkman och Gillen. Kulturer av C. freundii isolerades och identifierades samma år från markextrakt .
Genomstruktur
Ingen information om hela genomet av C. freundii finns tillgänglig online, även om vissa enskilda stammar och plasmider av mikroben har sekvenserats. Den mest framträdande är plasmid pCTX-M#3 eftersom den är den största plasmid och kodar för en stor mängd proteiner. Dess sekvens slutfördes den 6 januari 2005. Det är en cirkulär DNA-plasmid och den är 89 468 nukleotidbaspar lång. Plasmidlängden är 0,089468 (Mbp). Den består av 51,0% GC-innehåll och kodar för 105 proteiner .
en annan viktig egenskap hos C. freundii-genomet är att det är den enda mikroben i Enterobacteriaceae-familjen som innehåller en plasmid som kodar för L-metionin-Bisexuell-lyas (MGL). Nukleotidsekvensen för plasmid innehåller en 3000 bp lång EcoRI-insats . Fragmentet innehåller också två öppna läsramar. Den första ramen består av 1 194 nukleotider och den andra 1 296 nukleotider.Den första ramen, känd som megL-genen, kodar för ett protein med 398 aminosyrarester som har sekvenshomologi med MGL från olika källor. Den andra ramen kodar för ett protein med sekvenshomologi med proteiner som tillhör familjen permeaser .
C. freundii OS60 AMPC Bisexuell-laktamas-genen har också sekvenserats och den består av 1197 nukleotider. Den kodar en 380 aminosyra lång föregångare och innehåller en 19 restsignalpeptid i 5 ’ – änden . Denna gen kodar för ett moget protein som har en molekylmassa av 39 781 Dalton. Aminosyrapositionerna i dessa prekursorer är suprisinlgy identiska med rester i E. coli K12 kromosomala AMPC-laktamaser.
en annan viktig stam i genomet av C. freunii är GN346, vilket är ett kliniskt isolat som återhämtades 1965. Denna stam producerar enzymet cefalosporinas, som har förmågan att hydrolysera och inaktivera anibitoikerna cefalosporiner och cephamyciner . De strukturella och promotorregionerna i cefalosporinasgenen är 1408 nukleotider långa. Aminosyrasekvensen för det mogna enzymet består av 361 aminosyror med en molekylmassa av 39 878 Da .
cellstruktur och metabolism
cellstrukturen hos C. freundi är lång och stavformad vanligtvis 1-5 kg i längd. Utsidan av cellen innehåller många flageller som används för motalitet . Eftersom C. freundii är gramnegativa bakterier innehåller den två membran (inre och yttre).Det periplasmiska utrymmet ligger mellan de två membranen. Det yttre membranet innehåller inte en energikälla; men det innehåller många poriner inbäddade i det som hjälper organismen att förvärva viktiga joner . Till skillnad från gram-positiva bakterier innehåller C. freundii-celler inte en tjock cellvägg bestående av peptidoglykan.
för metabolism har C. freundii en fantastisk förmåga att växa på glycerol som enda kol och energikälla. I denna process fermenteras glycerol genom en dismutationsprocess. Denna process kräver två vägar . I den första vägen dehydrogeneras glycerol av ett NAD1-länkat glyceroldehydrogenas till dihydroxiaceton. Dihydroxiacetonen fosforyleras sedan och kanaliseras till glykolys av dihydroxiacetonkinas . I den andra vägen dehydreras glycerol av koenzym B12-beroende glyceroldehydratas för att bilda 3-hydroxipropionaldehyd . Denna produkt reduceras till den huvudsakliga fermentationsprodukten 1,3-propandiol av det NADH-länkade 1,3-propandioldehydrogenas, som regenererar NAD1. Dha regulon kodar för de fyra väsentliga enzymerna i dessa två vägar. Förvånansvärt induceras uttrycket av dha regulon endast när glycerol är närvarande .
celler av C. freundii kan också metabolisera laktos eller citrat som kolkälla .
ekologi
Citrobacter freundii finns ofta i miljön, främst i mark, vatten och avlopp. De är en indikator på potentiell förorening av vatten. De finns också på olika organ av sjuka djur, inklusive däggdjur, fåglar, reptiler och amfibier . De är inte kända för att interagera med andra organimer.
i miljön kan C. freundii omvandla nitrat eller ammoniumjonen (som är en kväveatom kombinerad med fyra väteatomer) till nitrit; denna reaktion sker i miljön såväl som i matsmältningskanalen hos människor och andra djur . Efter det omvandlar nitrat till nitrit i miljön omvandlas nitrit till kväve, och detta sista steg fullbordar kvävecykeln i jordens atmosfär, som består av 85% kväve . Denna organisms ekologiska roll inkluderar inte bara dess viktiga roll i kvävecykeln, eftersom den också kan ackumulera uran (vilket är grundmaterialet för kärnteknik) genom att bygga fosfatkomplex .
Citrobacter freundii har också undersökts för biologisk nedbrytning av garvsyra som används i tannerys .
patologi
som en opportunistisk patogen är Citrobacter freundii ofta orsaken till signifikanta opportunistiska infektioner, vilket innebär att det i allmänhet inte orsakar sjukdom hos friska humana värdar. De påverkar bara patienter med svagt immunförsvar, vilket innebär att de behöver en ”möjlighet” att infektera personen . Därför är Citrobacter-arter kända för att orsaka en mängd olika nosokomiala infektioner i luftvägarna, urinvägarna och blodet hos patienter med ett undertryckt immunsystem . Lever -, gall-och bukspottkörtelsjukdom är också vanliga sjukdomar som orsakas av C. freundii. Gallvägarna är den vanligaste infektionsstället av C. freundii-bacillerna .
en dödlig sjukdom som C. freundii har associerats med är neonatal meningit. Neonatal meningit är inflammation i hjärnhinnorna (membransystemet som omger CNS) på grund av bakteriell invasion . Dödligheten för Citrobacter meningit är oacceptabelt hög, med dödsgraden hos patienter som sträcker sig från 25 till 50 %. Dessutom kvarstår allvarliga neurologiska problem hos 75% av de överlevande. I denna sjukdom kan Citrobacter freundii penetrera blod-hjärnbarriären som består av choroid plexusepitel och hjärnkapillärendotel .
tester utförda av Badger et. al i artikeln ”Citrobacter freundii invaderar och replikerar i mänskliga Hjärnmikrovaskulära endotelceller”föreslår att bakteriell proliferation av C. freundii äger rum på intracellulär nivå, vilket hade strider mot den allmänna vetenskapliga tanken. Resultaten indikerar att C. freundii korsar vakuoler, replikerar och släpps ut i den basolaterala sidan av de mänskliga hjärnmikrovaskulära endotelcellerna (HBMEC) för att korsa blod-hjärnbarriären. Ytterligare analys kan potentiellt möjliggöra terapeutiska strategier för att behandla infektioner. Det finns fortfarande ingen terapeutisk behandling tillgänglig .
vissa sjukdomar som studerats i öring och cyprinider orsakas också av C. freundii. C. freundii orsakar onormala inflammatoriska förändringar i tarmen av öring och inflammatoriska och nekrotiska förändringar i de inre organen av cyprinider. Sjukdomen upptäcktes genom artificiell infektion med en ren kultur av C. freundii. Denna upptäckt etablerade C. freundii som en orsak till fisksjukdom .
i en fallstudie av Journal of Medical Microbiology utvecklade en patient peritonit och tunnelinfektion på grund av Citrobacter freundii vilket är ovanligt. Patienten var på kontinuerlig ambulatorisk peritonealdialys. Vanligtvis är de orsakande agenterna gram-positiva mikroorganismer, särskilt Staphylococcus aureus och Staphylococcus edpidermis. Det finns också inga kända rapporter om tunnelinfektion på grund av C. freundii. Initial antibiotikabehandling fungerade inte och infektionen fortsatte att kvarstå tills katetern avlägsnades. Detta är kliniskt signifikant eftersom Citrobacter Freundii visar olika antibiotikaresistens, varför initial behandling inte lyckades. Patienten svarade inte på behandlingen förrän katetern avlägsnades och visade att Citrobacter freundii är opportunistiska patogener som påverkar sjukhus och immunkompromitterade patienter .
ansökan till bioteknik
i bioteknikindustrin producerar Citrobacter freundii många viktiga enzymer.De första enzymerna som den producerar är fosfatas. Fosfatasaktivitet av C. freundii har postulerats för att vara involverad i blyackumulering, vilket kan ha spelat en viktig roll i bioteknikindustrin. Fosfatasaktiviteten hos C. freundii har också upptäckts ha resistens mot vissa diagnostiska reagenser .rening och karakterisering av bakteriell selenocystein beta-lyas, ett enzym som specifikt katalyserar klyvningen av L-selenocystein till L-alanin, har renats från Citrobacter freundii. Enzymet är monomer med en molekylvikt av ca. 64 000 och innehåller 1 mol pyridoxal 5 ’ – fosfat som en kofaktor per mol enzym. Enzymet katalyserar också alfa, beta eliminering av beta-klor-L-alanin för att bilda NH3, pyruvat .
C. Freundii-stammar bär också en plasmid som kodar för klass 1 AmpC-cefalosporinas. Dessa enzymer kan hydrolysera inaktivera nya cephamyciner och cefalosporiner .
aktuell forskning
en liten skala forskning om vissa stammar av C. freundii gjordes nyligen vid University of Tennessee, Knoxville. Betydelsen av vissa tetracyklin – och streptomycinresistensgener och klass 1-integroner i C. freundii isolerad från mjölkjordbruksjord och icke-mjölkjord utvärderades. En stam av C. freundii extraherad från mjölkjordar Bar klass 1-integroner med olika införda genkassetter. Resultaten av denna lilla studie föreslog att närvaron av flera resistensgener och klass 1-integroner i C. freundii i mjölkgårdsjord kan fungera som en reservoar av antimikrobiella resistensgener och kan spela en roll i spridningen av dessa antimikrobiella resistensgener till andra kommensala och inhemska mikrobiella samhällen i jord. Men ytterligare långsiktiga studier utförda på fler platser behövs för att stödja denna hypotes .
en andra forskning concering C. freundii gjordes för att utforma en polymeraskedjereaktion (PCR) – metod som samtidigt använder tre par specifika primers för att detektera gener av vissa mikrober (inklusive C. freundii). Metoden inkluderade att utforma tre primerpar som var: SPVC-1 och SPVC-2, INVA-1 och INVA-2; och VIAB-1 och VIAB-2. PCR utfördes med användning av dessa tre primers för att identifiera 14 kliniskt viktiga bakterieorganismer. Följande stammar identifierades snabbt med PCR: (1) C. freundii; (2) S. Typhi; och S. Paratyphi C; (3) S. Dublin (virulence antigen-positive); och (4) Salmonella serovarer som har en SPV-typ virulensplasmid. Även om denna PCR-metod är ny, med teknikens framsteg i framtiden kan denna metod möjliggöra identifiering av C. freundii hos däggdjur omedelbart så att lämplig antibiotikabehandling kan initieras utan dröjsmål .
en tredje studie concering C. freundii gjordes vid universitetet i Barcelona, Spanien. Mekanismerna för resistens mot fluorokinoloner i två Citrobacter freundii-stammar studerades. Båda stammarna isolerades från samma patient. Denna studie möjliggjorde partiell karaktärisering av acrA-och acrB-generna i denna mikroorganism. Uttryck av gener i båda stammarna analyserades med användning av DNA-mikroarrayer för Escherichia coli. Nukleotidlikhet mellan de delvis sekvenserade acrA-och acrB-generna av C. freundii och E. coli var 80,7% respektive 85%. AcrA-och acrB-generna av C. freundii liknar dem i E. coli och deras överuttryck kan spela en viktig roll för att modulera den slutliga minsta hämmande koncentrationen av fluorokinoloner .
en fjärde studie om C. freundii gjordes i Taiwan. Ett team av forskare isolerade en diabetespatient som utvecklade nekrotiserande fasciit som orsakades av C. freundii från en skada som uppstod av ett marint djur. Nekrotiserande fasciit är en infektion i det djupare lagret av huden och subkutan vävnad. Vid behandling av patienten tog de ett prov från vätskan i såret och fann C. freundii. Efter tre dagar efter att antibiotikabehandlingarna påbörjades med cefotaxmin och cefepmin ackumulerades subkutana abscesser. Efter 6, 10, 14 och 21 dagars vård till patienten gav vissa antibiotika patienten viss lättnad, men ingen långsiktig återhämtning uppnåddes. Cefotoaxime, cefepime, ciprofloxamin är bland de antibiotika som inte matchade C. freundii. Patienten återhämtade sig helt efter 42 dagars behandling med ertapenem. Forskarna hade isolerat två kolonier av C. freundii inom 5 dagar från varandra. När isolaten odlades blev de oerhört resistenta mot cefotaxim och cefepim. Anledningen till att entrapenem arbetade mot C. freundii beror på att den är aktiv mot AmpC-producerande Enterobacteriaceae .
antibiotikaresistens
Citrobacter-arter är en vanlig orsak till nosokomiala infektioner associerade med patienter som genomgår långvariga sjukhusbehandlingar. C. freundii har nyligen rapporterats uttrycka resistens mot bredspektrumantibiotinker inklusive piperacillin, piperacillintazobactam, vankomycin och cefalosporiner. Isolering av ceftriaxonresistent Citrobacter freundii (CRCF) har associerats med de överordinerade bredspektrumantibiotika. De framväxande nya CRCF-stammarna kan föreslå induktion eller depression av resistensgener såväl som eliminering av konkurrerande organismer. CRCF har mestadels isolerats från patienter med signifikanta komorbiditeter inklusive AIDS, perifer kärlsjukdom och cerebrovaskulär sjukdom. Användningen av fluorokinolon har också rapporterats ha någon inverkan mot isoleringen av CRCF .
Citrobacter freundii är också känt för att innehålla i sin kromosom en gen som kodar för cefalosporinas. Detta enzym hydrolyserar-CO-nh-bindning i laktamringen av cefalosporiner och cephamycis vilket gör bakterierna resistenta mot denna typ av antibiotika. Men när de exponerades för nya tredje generationens cephems och cerbapenems, kliniskt isolerade C. freundii visade känslighet för dessa ämnen.Ett litet utbrott av C. freundii resistent mot tredje generationens cephems har observerats i den kirurgiska avdelningen vid Nagoya Universitetssjukhus hos patienter som genomgick kirurgiska ingrepp. C. freundii isolerades från patientens galla, sårgas, avföring, pus och ascites. Det föreslogs att dessa nya stammar av C. freundii innehöll en plasmidkodning AmpC celphalosporinas men vid misslyckande att överföra cephems resistens från C. freundii till E. coli drogs slutsatsen att enzymet måste kodas i kromosomen av C. freundii. Eftersom C. freundi är associerad med nosokomiala infektioner rekommenderas försiktighet mot dessa nya stammar .
1. Wang JT, Chang SC, Chen YC, Luh KT. ”Jämförelse av antimikrobiell mottaglighet av Citrobacter freundii isolerar i två olika tidsperioder.”Journal of Microbiology, Immunology och infektion. 2000 December; 33 (4): 258-62.
2. Whalen JG, Mully TW, Enlgish JC 3rd. ”Spontan Citrobacter freundii-infektion hos en immunkompetent patient.”Arkiv för dermatologi. 2007 januari; 143 (1): 124-5.
3. Puchenkova SG. ”Enterobakterier i vattenområden längs Krimkusten.”Mikrobiolohichny Xiaomi zhurnal. 1996 Mar-April; 58 (2): 3-7.
4.http://www.ncbi.nlm.nih.gov/sites/entrez?db=genomeprj&cmd=Retrieve&dopt=Overview&list_uids=13123
5. Ilya V. Manukhov, Daria V. Mamaeva, Sergei M. Han är en av de mest kända och mest kända i världen. ”En gen som kodar för L-Metioninuctui-lyas är närvarande i familjen Enterobacteriaceae genom: identifiering och karakterisering av Citrobacter freundii L-Metioninuctui-lyas.”Journal of Bacteriology. 2005 juni; 187 (11): 3889-3893.
6. Lindberg, Frederik; Westman, Lennart; Normark, Staffan. ”Regulatoriska komponenter i Citrobacter freundii AMPC Bisexuell-laktamas induktion.”Proceedings of National Academy of Sciences i Amerikas förenta stater. 1985 juli; 82 (14): 4620-4624.
7. Tsukamoto K, Tachibana K, Yamazaki N, Ishii Y, Ujiie K, Nishida N, Sawai T. ”Roll lysin-67 i den aktiva platsen för klass C beta-laktamas från Citrobacter freundii GN346.”European Journal of Biochemistry / FEBS. 1990 Februari 22; 188 (1): 15-22.
8. Keevil CW, Hough JS, Cole Ja. ”Prototrofisk tillväxt av Citrobacter freundii och den biokemiska grunden för dess uppenbara tillväxtkrav i luftade medier.”Journal of General Microbiology. 1997 januari; 98 (1): 273-6.
9. Marco S. A., Turabian Ormbunke, D. A., D. A., D. A., D. A., D. A., D. A., D. A., D. A., D. A., D. A., D. ”Dödlig Citrobacter Freundii bronkopneumoni förvärvad i samhället i en kompromisslös Patient.”Revista Cl Brasilinica Espa Brasiliola. 1985 April; 176 (6): 320
10. Julie L. Badger, Monique F. Stins och Kwang Sik Kim. ”Citrobacter freundii invaderar och replikerar i mänskliga Hjärnmikrovaskulära endotelceller.”Hinyokika kiyo. Acta Urologica Japonica. 1985 Juli; 31 (7): 1159-70.
11. Drelichman V, Band JD. ”Bakterier på grund av Citrobacter diversus och Citrobacter freundii. Incidens, riskfaktorer och kliniskt resultat.”Arkiv för internmedicin. 1985 oktober; 145 (10): 1808-10.
12. Srinivasan V, Nam HM, Sawant AA, Headrick SI, Nguyen LT, Oliver SP. ”Distribution av tetracyklin-och Streptomycinresistensgener och klass 1-Integroner i Enterobacteriaceae isolerade från mjölk-och icke-Mjölkjordbruk.”Mikrobiell Ekologi. 2007 augusti 15.
13. S oskyl-C Oskyl-pedes J, Vila J. ” partiell karakterisering av acrAB locus i två Citrobacter freundii kliniska isolat.”International Journal of Antimicrobial Agents. 2007 September; 30 (3): 259-63.
14. Ci
15. Chocat P, Esaki N, Tanizawa K, Nakamura K, Tanaka H, Soda K. ” rening och karakterisering av selenocystein beta-lyas från Citrobacter freundii.”Journal of Bacteriology. 1985 Augusti; 163 (2): 669-76.
16. Hillel S Levinson, Inga Mahler. ”Fosfatasaktivitet och blyresistens i Citrobacter freundii och Staphylococcus aureus.”FEMS mikrobiologi bokstäver. 1998 April; 161 (1): 135-138.
17. Murakami K, Yoshida T. ” kovalent bindning av moxalaktam till cefalosporinas av Citrobacter freundii.”Antimikrobiella medel och kemoterapi. 1985 Maj; 27 (5): 727-32.
18. Dervisoglu, E., Yegenaga, I., Yumuk, Z. ”Citrobacter Freundii peritonit och tunnel infektion i en patient på kontinuerlig ambulatorisk peritonealdialys.”Journal of Medical Microbiology, 2008. Volym 57. s. 125-127.
19. Kim PW, Harris AD, Roghmann MC, Morris jg Jr, Strinivasan A, Perencevich EN. ”Epidemiologiska riskfaktorer för isolering av ceftriaxonresistenta kontra-mottagliga citrobacter freundii hos sjukhuspatienter” Antimicrob-medel Chemother, 2003 Sep;47(9): s.2882-2887.
20. Nada T, Baba H, Kawamura K, Ohkura T, Torii K, Ohta M. ”Ett litet utbrott av tredje generationens cephemresistenta Citrobacter freundii-infektion på en kirurgisk avdelning” JPN J infektera Dis. 2004 Aug;57 (4): s.181-182.
21. Chuang, Y., Tseng, S., Teng, L., Ho, Y. och Hsueh, P. ”Uppkomst av cefotaximresistens i Citrobacter freundii som orsakar nekrotiserande fasciit och osteomyelit” Journal of Infection, 2006. Volym 53. s. e161-e163.
22.Badger, J., Stins, M. och Sik Kim, K. ”Citrobacter freundii invaderar och replikerar i mänskliga Hjärnmikrovaskulära endotelceller” infektion och immunitet, 1999. Volym67. S. 4208-4215.
redigerad av Sumaira Akbarzada, student av Rachel Larsenredigerad av Greg Vargas och Darren Zhen, studenter vid M Glogowskiat Loyola Universityredigerad av Gergana Grigorova och Michal Olszewski, studenter vid M Glogowskiat Loyola Universityredigerad av Alex Kula och Joanna Aiken, studenter vid M Glogowskiat Loyola University