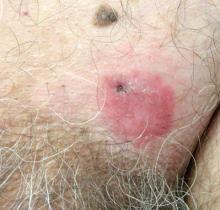
en 70-årig man presenterade en nonpruritisk erytematös skalig plack i den vänstra suprapubiska regionen på 6 månaders varaktighet som inte hade svarat på terbinafinkräm 1% efter 1 månad av behandling av misstänkt tinea cruris. Hans medicinska historia var anmärkningsvärd för högt blodtryck, hyperlipidemi, kronisk obstruktiv lungsjukdom, godartad prostatahyperplasi, en abdominal aortaaneurysm, alkoholberoende, tobaksmissbruk och oavsiktlig viktminskning på 15 lb under det senaste året.
diagnosen: Extramammary Paget Disease
en biopsi av plack avslöjade en intraepidermal proliferation av stora celler med riklig klar cytoplasma och stora vesikulära kärnor fördelade över epidermis (Figur 1). De neoplastiska cellerna färgades positivt för både periodisk syra-Schiff-fläck (Figur 2) och CK7 (Figur 3). Kemi-och leverfunktionspanel, urinanalys, karcinoembryoniska antigennivåer och prostataspecifika antigennivåer var inom referensområdet. Ett fullständigt antal blodkroppar avslöjade mild megaloblastisk anemi. Efterföljande datortomografi av bröstet, buken och bäckenet avslöjade en abdominal aortaaneurysm och prostataförstoring utan några tecken på potentiella maligniteter. Koloskopi avslöjade flera hyperplastiska polyper och ett rörformigt adenom. Cystoskopi var normalt, förutom bevis på prostataförstoring. Urincytologi var unremarkable. Patienten remitterades för excision av lesionen med Mohs mikrografisk kirurgi. Uppföljning rekommenderades var 3: e månad under de första 2 åren efter operationen och var 6: e månad därefter för att övervaka för återfall eller sekundära neoplasmer.
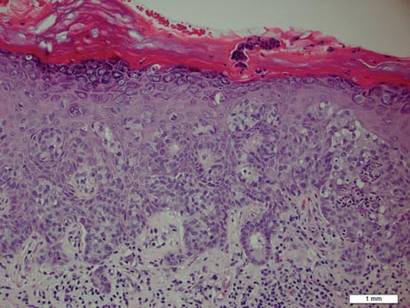
Figur 1. Intraepidermal proliferation av stora celler med riklig klar cytoplasma och stora vesikulära kärnor fördelade över epidermis som enskilda celler och som variabla aggregat av celler (H&E, original förstoring 200). (Referensfältet anger 1 mm.)
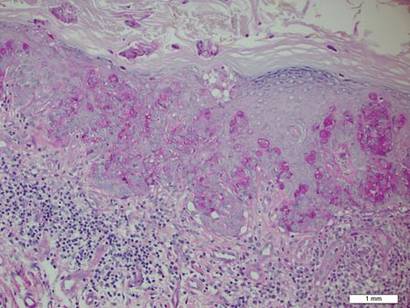
Figur 2. Granulär cytoplasma var positiv vid periodisk syra-Schiff-färgning(original förstoring 200). (Referensfältet anger 1 mm.)
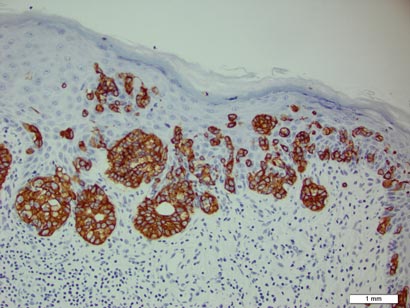
Figur 3. Neoplastiska Paget-celler var karakteristiskt positiva vid färgning för CK7 (originalförstoringaboken 200). (Referens bar indikerar 1 mm.)
Sir James Paget beskrev först Bröst Paget sjukdom i bröstvårtan i 1874 i sin rapport av 15 kvinnor med hudutslag i bröstvårtan och vårtgården och efterföljande karcinom av den underliggande Bröst.1 Paget beskrev också en patient med liknande utbrott på glanspenisen och Crocker2 beskrev extramammary Paget disease (EMPD) i pungen och penis 1889. Principskillnaden mellan mammary Paget disease och EMPD är den anatomiska platsen.
Extramammary Paget-sjukdom är ett sällsynt tillstånd som vanligtvis drabbar patienter i åldern 50 till 80 år och är vanligare hos kvinnor och vitskinniga raser.3 Extramammary Paget-sjukdom riktar sig ofta mot kutana platser som är rika på apokrina körtlar. Den vanligast drabbade platsen är vulva följt av perineal, perianal, scrotal och penishud. Mindre vanligt kan axillae, skinkor, lår, ögonlock och yttre hörselkanaler påverkas.4
patienter med EMPD förekommer vanligtvis med väl avgränsade, icke-lösande, erytematösa och ekosematösa plack som kan ha associerat skorpa, skalning, papillomatösa utväxter, lichenifiering, sårbildning eller blödning. Det vanligaste symptomet är klåda, följt av brännande, irritation, smärta och ömhet.5 tio procent av patienterna är asymptomatiska. Det genomsnittliga intervallet mellan symptomstart och diagnos är 2 år.5
Histopatologi avslöjar diffust infiltrerande, oregelbundna, neoplastiska Paget-celler i epidermis som är stora och vakuolerade med riklig blekblå cytoplasma och stora vesikulära kärnor, som kan komprimeras centralt eller i sidled. Cellerna kan distribueras var för sig eller i grupper som strängar, bon eller körtelmönster i nedre epidermis, rete åsar och adnexala strukturer. Hyperkeratos, akantos och parakeratos kan också vara närvarande. Paget-celler fläckar för immunhistokemiska markörer av apokrin och eccrine-derivat inklusive cytokeratiner med låg molekylvikt, brutto cystisk sjukdomsvätskeprotein 15, periodisk syra-Schiff–fläck och karcinoembryoniskt antigen.5 perrotto et al6 studerade 98 prover från 61 patienter och fann att CK7 var positivt i alla EMPD-prover, medan CK20 och gross cystic disease fluid protein 15 var positiva i stora delmängder av både primär och sekundär EMPD. Fall av EMPD sekundärt till anorektalt adenokarcinom var till stor del ErbB2 (tidigare HER2/neu) negativa och CDX2 positiva.6
diagnos av EMPD bör följas av en grundlig undersökning av underliggande karcinom. I en genomgång av 197 fall av EMPD hade 24% av patienterna med EMPD ett associerat underliggande in situ eller invasivt adnexalt apokrinkarcinom, vilket var förknippat med en högre dödlighet än hos patienter utan denna underliggande malignitet. Dessutom hade 12% av EMPD-patienterna en associerad underliggande inre malignitet.7 dessa maligniteter kan inkludera karcinom i urinröret, urinblåsan, vagina, livmoderhalsen, endometrium, prostata, kolon och rektum. Perianal EMPD har en högre frekvens av associerade maligniteter än vulvar EMPD.5 placeringen av EMPD är relaterad till placeringen av den underliggande maligniteten; till exempel är perianal EMPD associerad med kolorektala adenokarcinom, och EMPD i penis, pungen och ljumsken är associerad med genitourinära maligniteter. Undersökningar för att söka efter associerade maligniteter hos patienter med EMPD kan inkludera ultraljud i bäcken och/eller magnetisk resonansavbildning, hysteroskopi, koloskopi, sigmoidoskopi, cystoskopi, intravenöst pyelogram, mammogram och/eller röntgen i bröstet.