hjärtmyocyten är den huvudsakliga cellen som är involverad i ombyggnad. Fibroblaster, kollagen, interstitium och kranskärlskärlen i mindre utsträckning spelar också en roll. Ett vanligt scenario för ombyggnad är efter hjärtinfarkt. Det finns myokardiell nekros (celldöd) och oproportionerlig gallring av hjärtat. Detta tunna, försvagade område kan inte motstå tryck-och volymbelastningen på hjärtat på samma sätt som den andra friska vävnaden. Som ett resultat är det dilatation av kammaren som härrör från infarktområdet. Den initiala ombyggnadsfasen efter ett hjärtinfarkt resulterar i reparation av det nekrotiska området och myokardiell ärrbildning som i viss utsträckning kan anses vara fördelaktigt eftersom det finns en förbättring eller underhåll av LV-funktion och hjärtutgång. Men med tiden, när hjärtat genomgår pågående ombyggnad, blir det mindre elliptiskt och mer sfäriskt. Ventrikulär massa och volymökning, som tillsammans påverkar hjärtfunktionen negativt. Så småningom kan diastolisk funktion eller hjärtats förmåga att slappna av mellan sammandragningar försämras, vilket ytterligare orsakar nedgång.
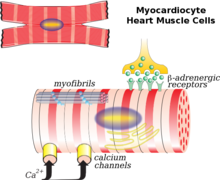
efter ett hjärtinfarkt (MI) kan hjärtmyocytdöd utlösas av nekros, apoptos eller autofagi, vilket leder till gallring av hjärtväggen. De överlevande hjärtmyocyterna ordnar antingen parallellt eller i serie med varandra, vilket bidrar till ventrikulär dilatation eller ventrikulär hypertrofi, beroende på belastningsspänningen på ventrikulär vägg. Dessutom tros minskat uttryck av V1-mysoin och L-typ kalciumkanaler på hjärtmyocyter också orsaka hjärtremodellering. Under normala kroppsförhållanden står fettsyra för 60 till 90% av hjärtans energiförsörjning. Post MI, som fettsyraoxidation minskar, leder det till minskad energiförsörjning för hjärtmyocyterna, ackumulering av fettsyror till toxiska nivåer och dysfunktion av mitokondrier. Dessa konsekvenser ledde också till ökningen av oxidativ stress på hjärtat, vilket orsakade proliferation av fibroblaster, aktivering av metalloproteinaser och induktion av apoptos, vilket skulle förklaras nedan. Dessutom bidrar inflammatoriskt immunsvar efter MI också till ovanstående förändringar.
dessutom är hjärtinterstitium som bestod av till stor del typ i och typ III kollagenfibrer också involverade i hjärtremodellering. Hjärtkollagen syntetiseras av fibroblaster och bryts ned av metalloproteinaser. Fibroblaster aktiveras efter MI, vilket leder till ökad kollagensyntes och fibros i hjärtat. Ökat uttryck av MMP1 och MMP9 ledde till nedbrytning av kollagenfibrer och därefter utvidgning av hjärtat. Flera signalvägar såsom Angiotensin II, transformerande tillväxtfaktor beta (TGF-beta) och endotelin 1 är kända för att utlösa syntes och nedbrytning av kollagenfibrer i hjärtat.
andra faktorer som högt blodtryck, aktivering av sympatiskt system som frisätter noradrenalin, aktivering av renin–angiotensinsystem som frisätter renin och anti-diuretiska hormoner är viktiga bidragsgivare till hjärtremodellering. Emellertid anses atriell natriuretisk peptid vara hjärtskyddande.