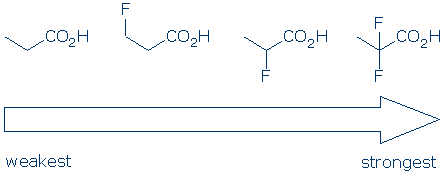
tunnista molekyylin Happamin H
metodinen lähestymistapa toimii parhaiten. Yksinkertaisesti sanottuna, sinun täytyy skannata molekyylin happamien funktionaalisten ryhmien ja sitten sijoitus näiden ryhmien reaktiivisuus. Happavin funktionaalinen ryhmä pitää yleensä hallussaan koko molekyylin happaminta H: ta.
”Scan and rank” kuulostaa yksinkertaiselta, mutta se kätkee sisäänsä useita jäljempänä käsiteltyjä vaikeuksia.
skannaa molekyylistä tunnetut happamat funktionaaliset ryhmät
happamat protonit sitoutuvat yleensä O: han tai n: ään. Siksi ensimmäinen askel on etsiä kaikkia OH-ja NH-sidoksia.
PAIKANTAESSASI OH-ja NH-sidoksia sinun on kuitenkin päätettävä, pitäisikö nämä sidokset niputtaa funktionaaliseksi ryhmäksi naapuriatomien kanssa.
ainoa kätevä tapa funktionaalisen ryhmän tunnistamiseen on jo joidenkin tunteminen. Jos esimerkiksi tiedät, että ROH, RCO2H ja RSO3H ovat yleisiä happamia funktionaalisia ryhmiä, sinulla ei ole vaikeuksia löytää happamia ryhmiä seuraavasta molekyylistä (oikeat ryhmät on merkitty punaisella).
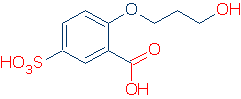
Rank OH ja NH happamuudet erikseen
yhteisten OH-ja NH-happojen pKa-arvot ulottuvat laajoille alueille ja niiden vaihteluvälit limittyvät. Ranking etenee nopeammin, jos rankataan OH-ja NH-hapot erikseen ja vertaillaan sitten kunkin kategorian kärkiehdokkaita.
kätevin tapa asettaa happamat ryhmät paremmuusjärjestykseen on tietää jo niiden ominaiset pKa-arvot. Jos tiedät nämä arvot kaikille molekyylisi happamille ryhmille, niin ryhmä, jolla on alhaisin pKa, sisältää eniten happamia H. tapaus suljettu.
Jos et muista kaikkien happamien ryhmien pKa-arvoja, muutama yleinen periaate voi opastaa.
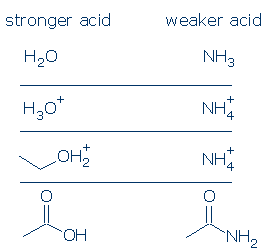
#1 merkitys – positiivisesti varautuneet hapot ovat vahvempia kuin neutraalit hapot. Negatiivisesti varautuneet hapot ovat harvoin happamia. Jos vertaat tavallisten OH-happojen pKa-arvoja, huomaat, että ROH2+ – hapot (joihin kuuluvat H3O+ ja R2OH+) ovat huomattavasti vahvempia kuin neutraalit hapot, kuten RCO2H, PhOH ja ROH. Ainoat neutraalit hapot, jotka ovat voimakkaampia kuin ROH2+, ovat H2SO4 ja eräät muut RSO3H.
muodollinen varaussääntö pätee vielä voimakkaammin NH-hapoille. PKa: n ero H3O+: n ja H2O: n välillä on 18 yksikköä, kun taas pKa: n ero NH4+: n ja NH3: n välillä on jättimäiset 26 yksikköä.
#2 Importance – look for activating groups, including RSO2, RC=O, and Ph. seuraava kaavio osoittaa, miten kukin atomiryhmä aktivoi Oh-happoa (pKa-arvot vaihtelevat 16: sta -2: een):
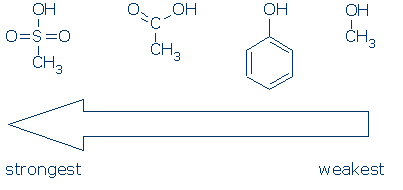
CH3 katsotaan katsomoryhmäksi kaikkialla, missä se esiintyy näissä molekyyleissä. Se on ei-polaarinen eikä sillä ole merkittävää kenttäinduktiivista vaikutusta, eikä se kykene delokalisoimaan varausta. Näin ollen CH3 on mahdollista korvata muilla katsojaryhmillä (esimerkiksi H ja muu R) vaikuttamatta juurikaan reaktiivisuuteen.
aktivoivista ryhmistä on tehtävä vielä kaksi lisäpistettä.
ensin ryhmät vaikuttavat NH-happoihin samalla tavalla (ja aktivoiva sekvenssi on sama: RSO2 > RC=O > Ph). Koska se tapahtuu, sinun tarvitsee vain oppia vaikutus Ph NH+ Tämän kurssin:
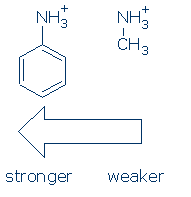
toiseksi aktivoivien ryhmien on liityttävä suoraan OH-ryhmään (tai NH-ryhmään) aktivoidakseen sen. Seuraavilla yhdisteillä on samanlaiset pKa-arvot, koska aktivoivat ryhmät eivät ole sitoutuneet suoraan OH: CH3C(=O)CH2OH, PhCH2OH ja CH3CH2OH.
#3 merkitys – Koska kaikki asiat ovat yhtä, OH-happo on happamampi kuin NH-happo. Tämä periaate voi olla erittäin hyödyllinen, jos sitä käytetään oikein. Olen huolissani siitä, että ymmärrät, mitä tarkoittaa ” kaikki asiat ovat samanarvoisia.”Tämä tarkoittaa, että O: lla ja N: llä on oltava sama muodollinen varaus (kohde #1) ja ne on sidottava samaan aktivoivaan ryhmään (kohde #2). Katsojaryhmien eroilla ei kuitenkaan ole merkitystä.
joitakin valideja vertailuja ovat:
#4 merkitys – funktionaalisessa ryhmäluokassa käytetään substituenttiefektejä happojen vertailuun. Elektronegatiiviset substituentit parantavat yleensä funktionaalisen ryhmän happamuutta kenttä-ja induktiivisten efektien yhdistelmällä. Nämä vaikutukset tehostuvat, kun 1) substituentti sijaitsee lähempänä happamaa ryhmää ja 2) substituentteja on useita. Näiden periaatteiden vuoksi odotamme näiden karboksyylihappojen happamuuden noudattavan tätä suuntausta: