John E. Cunningham
wprowadzenie
Pseudarthrosis, lub non-union, jest zbyt powszechnym i kosztownym powikłaniem operacji fuzji kręgosłupa, z kosztem za QALY (quality-adjusted life year) uzyskanym szacuje się na około US$118,945.1 szacunki stóp różnią się znacznie w zależności od badań z wykorzystaniem różnych technik chirurgicznych i populacji pacjentów.
Pseudarthrosis jest zwykle definiowany jako niepowodzenie połączenia kostnego między dwoma kręgami w ciągu 12 miesięcy po operacji.3 dopóki nie dojdzie do fuzji kości stałej, chirurg nie powinien brać pod uwagę osiągnięcia przez pacjenta chirurgicznego punktu końcowego, niezależnie od początkowego wskazania do operacji fuzji.
zapobieganie rzekomej chorobie stawów może być trudne, podobnie jak diagnostyka i leczenie. Częścią trudności w zapobieganiu mogą być czynniki ryzyka pacjenta, które często nie są modyfikowane w krótkim okresie. Chirurdzy są zachęcani do zwrócenia uwagi na te czynniki ryzyka i modyfikowania ich leczenia chirurgicznego, aby złagodzić te zagrożenia jak najlepiej. Czasami może to obejmować opóźnianie lub nawet anulowanie interwencji chirurgicznej, jeśli ryzyko wystąpienia pseudarthrosis i wynikający z tego zły wynik przewyższają wszelkie przewidywane korzyści z zabiegu.
prezentacja pseudarthrosis najczęściej obejmuje ból, który jest zwykle centralny charakter i początek, który może być wiele miesięcy po operacji. Badanie i diagnoza najczęściej polega na precyzyjnym cięciu tomografii komputerowej i zawsze należy uwzględnić współistniejące infekcje. Leczenie najczęściej polega na chirurgii rewizji stosując wiele technik.
czynniki ryzyka
czynniki pacjenta odgrywają istotną rolę w odniesieniu do ryzyka rzekomego zapalenia stawów. Palenie jest jednym z lepiej zbadanych czynników ryzyka.4,5 Brown et al., przeprowadzono randomizowane badanie 100 pacjentów poddanych dwupoziomowej nieinstrumentowanej fuzji z L4 do kości krzyżowej.6 odsetek osób niepalących wynosił 8%, podczas gdy u zwykłych palaczy odsetek ten był pięciokrotnie wyższy-40%. W nowszym badaniu zbadano wpływ palenia w obecności oprzyrządowania śrubowego szypułkowego, ale bez urządzeń międzyzębowych.7 W przypadku fuzji jednopoziomowych nie stwierdzono różnic w szybkości fuzji, ale w przypadku fuzji dwupoziomowych pseudarthrosis był trzykrotnie wyższy (29% vs. 11%).
inne czynniki wpływające na wskaźnik związkowy to te, które nie powinny być zaskoczeniem dla chirurga ortopedy, ponieważ są one podobne do tych dla ogólnych nie-związków. Należą do nich wiek, stosowanie sterydów i NLPZ, cukrzyca, niedożywienie i wcześniejsza operacja.8,9 promieniowanie okołooperacyjne zmniejsza również szybkość fuzji, 10 co należy wziąć pod uwagę podczas leczenia pacjentów z nowotworami.
z chirurgicznego punktu widzenia liczba poziomów zwiększa ryzyko zapalenia stawów rzekomych, podobnie jak stosowanie sztywnego zamocowania.9,11 wszelkiego rodzaju Oprzyrządowanie zwiększa szybkość fuzji w stosunku do fuzji bez oprzyrządowania.12 w kolejności szybkości fuzji, obwodowa lokalizacja fuzji daje najwyższą (zarówno międzylądową, jak i tylno-boczną), a następnie tylną międzylądową, przednią międzylądową, a następnie tylno-boczną.11 istnieją dowody na to, że tytanowe urządzenia międzyzębowe łączą się szybciej i częściej niż te wykonane z PEEK.13-15
Pedicle Subtraction Osteotomy
operacja pedicle subtraction osteotomy (PSO) jest wykonywana w coraz większej liczbie zarówno ze względu na nasze większe uznanie dla niedowładu strzałkowego, jak i naszej starzejącej się populacji.Jednym z głównych powikłań jest rzekoma choroba stawów, występująca u około 10% pacjentów.Pseudarthrosis najczęściej występuje na poziomie osteotomii, a czynniki ryzyka obejmują wykonanie operacji w celu zarządzania wcześniej istniejącą pseudarthrosis, promieniowanie przedoperacyjne, obecność zaburzenia neurologicznego lub zapalnego oraz brak zespolenia międzyprzedmiotowego bezpośrednio nad osteotomią. Ta ostatnia obserwacja jest poparta badaniami zwłok.18 wydaje się, że klatki międzyzębowe poprawiają szybkość syntezy poprzez zwiększenie sztywności konstrukcji. Z tego też powodu autorzy decydują się na dodanie trzeciego pręta do konstrukcji PSO, od poziomu powyżej do poziomu poniżej miejsca osteotomii za pomocą łączników side-to-side i chromowo-kobaltowego pręta, podobnego do techniki opisanej przez Hyun et al.19
operacja deformacji kręgosłupa
w jednym z badań operacji deformacji obejmujących kość krzyżową stwierdzono, że odsetek stawów rzekomych wynosił 24%.Wszystkie rzekomobłoniaki zostały wykryte przed czterema latami po operacji, średnio po 27 miesiącach i występowały albo w odcinku piersiowo-lędźwiowym, albo w odcinku lędźwiowo-krzyżowym. Zidentyfikowanymi czynnikami ryzyka były: kifoza piersiowo-lędźwiowa i podejście do klatki piersiowej i śródstopia (w przypadku rzekomej choroby klatki piersiowej i lędźwiowej), choroba zwyrodnieniowa stawów biodrowych i dodatni bilans strzałkowy ≥ 5 cm (w przypadku rzekomej choroby lędźwiowo-krzyżowej) oraz wiek > 55. Zgodnie z oczekiwaniami, pacjenci z rzekomą chorobą stawów mieli niższe wyniki Scoliosis Research Society (SRS) niż pacjenci z fuzją stałą (71 vs.90/120).
prezentacja
Pseudarthrosis może prezentować się na trzy różne sposoby. Pacjent może być bezobjawowy i mieć dobrą funkcję, mogą być objawowe, lub mogą mieć pseudarthrosis związane z innym patologicznym podmiotem, takim jak zakażenie.
wyniki czynnościowe
nie jest jasne, dlaczego wielu pacjentów z chorobą rzekomą stawów pozostaje bezobjawowych i mają dobre wyniki czynnościowe. W małym badaniu z 1968 r.porównano wyniki pacjentów z fuzją ciał stałych w porównaniu do pseudarthrosis i stwierdzono niewielką różnicę.21 Opis fuzji podaje się jako typu Hibbs lub „H”, dlatego można przypuszczać, że autorzy wykonywali Fuzje nieinstrumentowane. Bardziej nowoczesne badanie nieinstrumentowanych fuzji nie wykazało takich samych wyników, przy czym tylko 56% pacjentów z chorobą rzekomą stawów osiągnęło zadowalające wyniki w porównaniu do 86% pacjentów z fuzją stałą.22
patrząc na badania instrumentowanych fuzji, istnieją mieszane dowody na korelację między solidnym związkiem a dobrym wynikiem. Recenzja Resnick et al. stwierdził, że ” większość dowodów medycznych klasy III sugeruje, że pomyślna fuzja radiologiczna wiąże się z poprawą wyników klinicznych.”23 niektóre z tych badań były randomizowane, ale nadal były klasyfikowane jako klasa III ze względu na wysoki wskaźnik krzyżowania.
w badaniu kolejnych pacjentów z deformacją w jednej placówce, u wszystkich pacjentów z potwierdzoną chorobą rzekomą w wieku jednego roku lub więcej, nie udało się poprawić wyników SRS lub Oswestry Disability Index (ODI).W rzeczywistości, brak poprawy w tych wynikach był bardziej dokładny w wykrywaniu pseudarthrosis niż zwykłe rentgenowskie. Zauważono to również w omawianym wcześniej badaniu skoliozy.20 to odkrycie prowadzi autorów do wniosku, że punktacja wyników czynnościowych jest niezbędna do monitorowania pacjentów z deformacją pooperacyjną i powinna służyć jako impuls do dalszych badań w kierunku rzekomego zapalenia stawów.
bezobjawowa choroba zwyrodnieniowa stawów
wykrycie choroby zwyrodnieniowej stawów u bezobjawowego pacjenta jest zwykle wynikiem obserwacji przez chirurga i skłania do ciekawego rozważenia. Na przykład, jeśli pacjent ma pseudarthrosis, a jednak jest bezobjawowy i funkcjonuje dobrze, czy coś można uzyskać, wystawiając ich na promieniowanie, aby znaleźć anomalię, która najprawdopodobniej nie będzie wymagała interwencji chirurgicznej? W jakich okolicznościach wykrycie rzekomego zapalenia stawów zmieni postępowanie chirurga u bezobjawowego pacjenta? Rozsądne byłoby, aby po dowolnej wielopoziomowej procedurze lub osteotomii wczesne wykrycie i leczenie bezobjawowej choroby rzekomej mogło zapobiec katastrofalnym komplikacjom w przyszłości, a zatem Nadzór jest uzasadniony. Można to zrobić skutecznie i efektywnie dzięki standardowym systemom punktacji. Po procedurze jednego poziomu jest jednak mało prawdopodobne, aby w przyszłości wystąpiły jakiekolwiek poważne komplikacje, nawet jeśli nie zjednoczyły się, więc badanie radiologiczne jest prawdopodobnie mniej ważne.
objawowa Pseudarthrosis
W przypadku objawowej pseudarthrosis występuje zwykle nasilenie osiowego bólu pleców. Ból może być pogorszeniem pierwotnego bólu operacji („nigdy się nie polepszyło”) lub może być nowym początkiem. Pacjenci ze skoliozą mogą skarżyć się na pogorszenie deformacji, choć nie jest to częste zjawisko. W przypadku zesztywniającego zapalenia stawów kręgosłupa, pacjenci mogą być wrażliwe na ich horyzoncie wzrokowym. Objawy neurologiczne są nietypowe, chyba że deformacja segmentowa jest znaczna.
współistniejąca Pseudarthrosis
najbardziej prawdopodobnym rozpoznaniem współistniejącej choroby jest zakażenie. Historia gorączki, nieplanowany powrót na salę operacyjną, długotrwała antybiotykoterapia i rana po rozładowaniu jest silnie wskazująca na infekcję. Prezentacji może towarzyszyć utrata masy ciała i złe samopoczucie. Wszelkie inne portale infekcyjne powinny zostać zbadane.
badanie
badanie podejrzenia rzekomej choroby rzekomej powinno uwzględniać prawdopodobną diagnozę różnicową lub towarzyszącą. Chociaż początkowo trudne do interpretacji, należy zbadać CRP i ESR, podobnie jak wszelkie inne krwinki sugerujące zakażenie. Ranę należy zbadać i udokumentować obrzęk tkanek miękkich lub pobranie. Wszelkie pobrane płyny należy pobrać i przesłać do mikroskopii, hodowli i badań wrażliwości. Nawet badania przedoperacyjne mogą ominąć infekcje o niskim stopniu zaawansowania, więc chirurg musi być przygotowany na wypadek napotkania ropnego płynu po rewizji.
badania obrazowe
Analiza statystyczna
każda dyskusja na temat badań obrazowych lub innych testów diagnostycznych w tym zakresie musi zawierać ocenę czułości i swoistości oraz wartości 𝜅 (kappa). Każdy chirurg musi być zaznajomiony z tymi terminami i sposobem ich wykorzystania do podejmowania decyzji. Do celów czytania poniższego tekstu, testy są analizowane jako próby wykrycia fuzji. W związku z tym czułość odnosi się do szansy na prawidłową identyfikację fuzji, podczas gdy swoistość odnosi się do szansy na prawidłową identyfikację stawu rzekomego.
test niskiej czułości może „przegapić” solidną fuzję i może zachęcić chirurga do wykonywania niepotrzebnych zabiegów w celu naprawienia pozornej rzekomej stawów, która jest w rzeczywistości solidna. Z drugiej strony test o niskiej swoistości może „przegapić” pseudarthrosis i pozostawić chirurga i pacjenta w przekonaniu, że fuzja jest solidna, podczas gdy w rzeczywistości tak nie jest.
wartość kappa, lub współczynnik kappa Cohena, jest miarą umowy między obserwatorami i waha się między 0 (Brak umowy, lub umowa tylko przez przypadek) i 1 (umowa doskonała). Wartość 0,41-0.60 uznaje się za umiarkowane, a 0,61-0,80 za znaczące. Wartości powyżej 0,81 są uważane za” prawie doskonałe ” porozumienie w dziedzinie biomedycyny.Praktyczne znaczenie tego zjawiska polega na tym, że nawet jeśli test ma wysoką czułość i swoistość, niska wartość kappa powinna wskazywać chirurgowi, że rzeczywisty wynik może być w dużym stopniu zależny od obserwatora. Sposobem na obejście tego może być uzyskanie konsensusu poprzez prezentację wyników wielu specjalistom.
zdjęcia rentgenowskie
zdjęcia rentgenowskie zwykłe
dwa najlepsze zdjęcia rentgenowskie to Zdjęcia Brodskiego i Kanta.26,27 ich wyniki były dość podobne. Korelacja pomiędzy zwykłym statycznym promieniowaniem rentgenowskim a badaniem chirurgicznym wynosiła 64-68%, z czułością 85-89%, ale niską swoistością 60-62%. Jeśli prześwietlenie rentgenowskie wykazuje fuzję stałą, innymi słowy, prawdopodobnie jest ona stała, ale jeśli sugeruje pseudarthrosis, nie można na niej polegać. Czas od operacji do wykrycia stawu rzekomego za pomocą zdjęcia rentgenowskiego jest również dość długi, średnio 3,5 roku.20
Kolejną kwestią jest duża zmienność interpretacji promieniowania rentgenowskiego, zarówno między -, jak i wewnątrz – obserwatora. W jednym badaniu, w którym promieniowanie rentgenowskie zostało ocenione przez dwóch chirurgów i dwóch radiologów, 𝜅 = 0,4–0,7, co wskazuje na słabą korelację. Dlatego, pomimo względnego niedrogiego charakteru zwykłych promieni rentgenowskich i ich dostępności, autorzy nie zalecają ich do oceny fuzji stałej.
gięcie lub dynamiczne promienie rentgenowskie
gięcie lub dynamiczne filmy, znane również jako badania zgięcia i rozszerzenia, wykonują podobnie jak zwykłe promienie rentgenowskie podczas badania pseudarthrosis. W tym samym badaniu przez Brodsky et al. jak wspomniano powyżej, stwierdzono, że chociaż brak ruchu w tych badaniach dobrze korelował z fuzją ciała stałego, ruch niekoniecznie wskazuje na pseudarthrosis.26
tomografia komputerowa (CT)
w omawianym już badaniu Brodsky i wsp., Tomografia komputerowa wykazała jedynie czułość 63%, swoistość 86%, dodatnią wartość prognostyczną 72% i ujemną wartość prognostyczną 81%. Wyniki te nie różniły się diametralnie od zwykłego promieniowania rentgenowskiego, ale należy pamiętać, że badanie to, i wiele podobnych, zostało przeprowadzone pod koniec lat 80. nie powinno dziwić, dlatego też, że bardziej nowoczesne badania, z bardziej nowoczesnymi spiralnymi skanerami wielościennymi, wykazały znacznie lepsze wyniki. Niestety, niewielu porównało obrazowanie do badań chirurgicznych.
Fuzje tylno-boczne
Dwa ostatnie badania porównały wyniki tomografii komputerowej z wynikami badań chirurgicznych. W swojej pracy z 2007 roku,28 Carreon et al. wykorzystano 1 mm wycinek osiowy tomografii komputerowej wydrukowanej na folii i poddano je ocenie trzech chirurgów kręgosłupa. Co ciekawe, udokumentowali fuzję w stawie fasetowym, jak również fuzję w tylno-bocznych rynnach. Kiedy fuzja była obserwowana w obu aspektach i obu tylno-bocznych rynnach, szansa na fuzję stałą w eksploracji wynosiła 96%. Jeśli było widoczne tylko w tylno-bocznych rynnach, to spadło to do 89%, a w końcu, jeśli było widoczne tylko fuzja przez stawy, to szansa na zobaczenie stałej fuzji podczas eksploracji wynosiła 74%. Jednak brak zespolenia w obu stawach fasetowych lub w jednej rynnie tylno-bocznej nie przewidywał w sposób wiarygodny pseudarthrosis podczas badania.
Fuzje międzykręgowe przedniego odcinka lędźwiowego (ALIF)
w drugim artykule poświęconym fuzjom międzykręgowym przedniego odcinka lędźwiowego przy użyciu metalowych klatek autorstwa Carreon i wsp., 29 zastosowano podobny protokół. Chociaż obserwatorzy wykazywali znaczną zmienność, po uzyskaniu konsensusu badanie tomografii komputerowej wykazało 93% czułości i 46% swoistości fuzji. Przedni znak wartowniczy30 wykazywał jedynie czułość 20% i swoistość 92% w wykrywaniu fuzji, podczas gdy tylny znak wartowniczy30 okazał się bardziej dokładny, z czułością 67% i swoistością 79%. Brak przedniego znaku wartownika to dobry test na pseudarthrosis.
Fuzje Międzyprzedsionkowe lędźwiowe (PLIF/TLIF)
ocena fuzji międzyprzedsionkowej jest często problematyczna. Artefakt może często zakłócać obrazowanie CT, szczególnie w przypadku wykonywania na starych maszynach, a znaczniki tantalu w klatkach PEEK lub z włókna węglowego mogą często pozostawiać dramatyczny artefakt (rys. 4-1). Nowoczesne wielowarstwowe maszyny spiralne z bardziej wyrafinowanymi algorytmami usuwania artefaktów znacznie ułatwiły zadanie, a rekonstrukcje płaszczyzn koronalnych są doskonałe do wizualizacji międzypłytkowej masy fuzji.
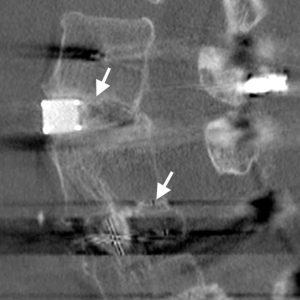
31 wykonano tomografię komputerową pacjentów 6 miesięcy po operacji, którzy przeszli PLIF z użyciem klatek tytanowych, w których zapakowano jedyny przeszczep kostny w klatkach. Opisał pomostową trabekulację kostną zarówno wewnątrz klatek, jak i poza klatkami, w których nie zapakowano przeszczepu kostnego. Zauważono podobieństwa do znaku sentinel. Odkrył również, że CT jest znacznie bardziej czułe przy określaniu obecności lub braku radiolucent endplate Cage interface niż X-ray, z bardzo dużą zgodnością między obserwatorami. Fogel i in., 32 Z drugiej strony, okazało się, że nie było małej różnicy między tomografią komputerową a promieniami rentgenowskimi przy ocenie fuzji po PLIF. Trudność w pracy polega jednak na tym, że na 172 poziomach chirurgicznie zbadanych znaleziono tylko cztery przypadki pseudarthrosis. Przy tak niskim wskaźniku pseudarthrosis 2.3%, obliczenia czułości i swoistości mogą mieć duży wpływ na stosunkowo niewielkie zmiany w wykrywaniu.
bardzo przydatny artykuł autorstwa Kanemury i in.33 śledzone zmiany radiograficzne w czasie. Przebadano 153 pacjentów do 5 lat po zabiegu PLIF z użyciem miejscowego przeszczepu kości i grzebienia biodrowego. Odkryli, że ruch ≥ 5° na dynamicznych promieniach rentgenowskich był maksymalny po roku, ale następnie stopniowo zmniejszał się w czasie. Podobnie, odkryli, że przy użyciu promieni rentgenowskich i tomografii komputerowej, strefy promieniotwórcze wokół śrub szypułkowych były również maksymalne w ciągu jednego roku, ale następnie rozwiązane bez interwencji chirurgicznej przez trzy do czterech lat. Przednia kość mostkowa zaczęła tworzyć się po trzech miesiącach,a następnie kontynuowana. Objętość przeszczepu międzykostnego zmniejszała się o 6 miesięcy, a następnie ponownie zwiększała się po dwóch do trzech latach.
przy tak wielu zmianach związanych z pseudarthrosis obecnych w 6 – do 12-miesięcznym znaku pooperacyjnym, ten artykuł wzywa chirurga do opóźnienia interwencji chirurgicznej w przypadku pseudarthrosis, dopóki nie miną co najmniej dwa lub trzy lata, ponieważ wiele zmian rozwiąże się bez interwencji. Czy któraś ze zmian wiąże się z ewentualną diagnozą rzekomej choroby stawów? Jedynym znalezionym predyktorem była obecność strefy promieniotwórczej wokół klatki międzykomórkowej większej niż 1 mm po 12 i 18 miesiącach. Był to niezależny predyktor związany z osiadaniem, ruchem i zmniejszaniem przeszczepu kości międzykostnej.
obrazowanie metodą rezonansu magnetycznego
chociaż przeprowadzono pewne badania dotyczące dokładności MRI,34,35, nie porównano go korzystnie z tomografii komputerowej lub eksploracji operacyjnej. Może to dać chirurgowi informacje o zmianach modowych obecnych w przestrzeni dysku, ale nie wykazano, aby wiarygodnie korelować z fuzją lub rzekomą stawową.
Analiza Stereofotogrametryczna Roentgena (RSA)
RSA jest techniką, w której markery tantalu są osadzone w kościstych kręgach w czasie operacji. Standaryzowane obrazowanie jest następnie pobierane z kulek w okresie pooperacyjnym, a ruch można dokładnie zmierzyć.36 technika ta cierpi na podobny problem do dynamicznych promieni rentgenowskich, w tym ruchu, lub jego brak, niekoniecznie koreluje z rzekomej stawów. Na przykład, zgodnie z RSA może nie być ruchu w całym segmencie bezpośrednio po zabiegu, ale oczywiście nie ma fuzji jeszcze ustalone.Jest on stosowany wyłącznie do celów badawczych, a korelacja kliniczna z fuzją termojądrową powinna być starannie opracowana.
Medycyna nuklearna
skanowanie kości technetu-99m jest często używane do oceny aktywności kości wokół masy fuzyjnej. Uważa się, że koreluje z fuzją, ponieważ skanowanie jest „zimne”. Brak jednak dowodów na jego przydatność. W porównaniu do badań chirurgicznych, chociaż był specyficzny (93%), brakowało czułości (50%) i miał tylko dodatnią wartość prognostyczną 40%, gdy szukał pseudarthrosis.38 podobnych wyników stwierdzono u pacjentów ze skoliozą.39 uważa się, że głównym problemem jest to, że technika nie jest w stanie odróżnić ustalonej pseudartrozy od niedojrzałej masy fuzyjnej.
USG
zastosowanie USG oceniono w jednym małym badaniu, porównując wygląd struktur tylnych do eksploracji chirurgicznej.40 chociaż wydaje się obiecujący, ma ograniczoną zdolność do oceny przedniej masy fuzyjnej. Nie przeprowadzono dalszych badań.
klasyfikacja
fuzja tylno-boczna
Heggeness i Esses jako pierwsi sklasyfikowali morfologicznie różne typy fuzji tylno-bocznej (tabela 4-1).41 opisali również „znak żwiru”, który jest powszechnie spotykany w typie żwiru pseudarthrosis, w którym fragment kości unoszący się za tylnymi elementami podczas patrzenia na osiowy wycinek CT. Klasyfikacja ta jest przydatna, ponieważ sugeruje przyczynę rzekomej choroby stawów.
| Typ | opis |
| zanikowa | zanik i resorpcja fuzyjnej masy kostnej |
| poprzeczna | odpowiednia masa kostna, ale pozioma nieciągłość utrzymuje się |
| gonty | zmienność poprzeczna, w której nieciągłość jest ukośna |
| kompleks | obecność wielu wad zespolenia |
Lenke i in.42 opisał bardziej jakościową klasyfikację tylno-bocznej masy fuzyjnej, od „zdecydowanie stałej” do „zdecydowanie nie stałej” (tabela 4-2). Chociaż może to być przydatne do opisania fuzji, to daje pomoc chirurga w diagnozowaniu lub leczeniu powikłań.
| Typ | Skrót | opis |
| a | zdecydowanie solidny | solidny duży obustronne masy termojądrowe trabekulowane |
| b | prawdopodobnie stała | jednostronna duża masa termojądrowa z kontralateralną małą masą termojądrową |
| C | prawdopodobnie nie stała | małe, cienkie masy fuzyjne |
| D | zdecydowanie nie stała | resorpcja przeszczepu obustronnie lub masa fuzyjna z oczywistą obustronną pseudartrozą |
fuzja międzyzębowa
Brantigan i Steffee po raz pierwszy opisali klasyfikację fuzji międzyzębowej poprzez klatkę z włókna węglowego.43 później zmodyfikowana przez Frasera, jest zwykle znana jako klasyfikacja BSF (Brantigan, Steffee, Fraser) (tabela 4-3).32,44 Pseudarthrosis ocenia się za pomocą tomografii komputerowej i klasyfikuje jako BSF-1, gdzie występują poważne oznaki ruchu (Fig. 4-2), lub BSF-2, gdzie w przestrzeni międzyzębowej znajduje się pozioma lucencja (rys. 4-3). Ten ostatni jest zwykle znany jako „zablokowana pseudarthrosis”. Jeśli chodzi o fuzję, uważali, że fuzja jest solidna, jeśli widziano, że kość rośnie przez jedną z klatek PLIF, nawet jeśli druga miała lucencję.
| opis | |
| BSF-1 | upadek konstrukcji
|
| BSF-2 / td> | radiograficznie zablokowana pseudarthrosis jest wskazana przez Lucency widoczne w środek klatki z Litą kością wyrastającą do klatki z każdej płytki kręgowej. |
| BSF-3 | radiograficzna fuzja: Mostki kostne co najmniej w połowie obszaru fuzji o gęstości co najmniej pierwotnie uzyskanej podczas operacji. |
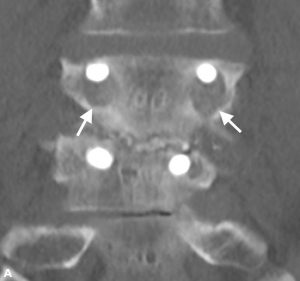
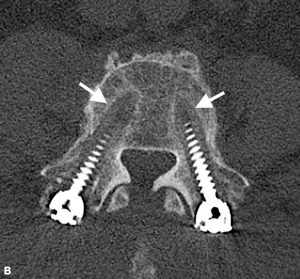
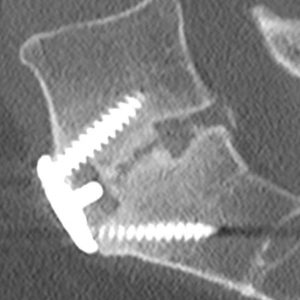
strategie chirurgiczne
decyzja o interwencji chirurgicznej zawsze musi być równowagą ryzyka i korzyści. Bezobjawowy pacjent z pojedynczym poziomie pseudarthrosis może nie wymagać interwencji, ale pacjent z długim fuzji, nawet jeśli bezobjawowe, może uzasadniać rozważenia, aby uniknąć podejmowania przyszłych operacji znacznie trudniejsze. Należy zauważyć, że nawet po udanej fuzji pacjenci, którzy cierpieli na pseudarthrosis, nie radzą sobie tak dobrze, jak ci, którzy mieli udaną fuzję po początkowej operacji.5
podejście
różnice w leczeniu operacyjnym stawu rzekomego są tak liczne i zróżnicowane, jak metody wykonywania fuzji w pierwszej kolejności. Ogólne zasady, których należy przestrzegać, to poprawa stabilizacji, wykonanie nowego szczepienia i przywrócenie wyrównania strzałkowego.45 w celu poprawy stabilizacji należy wymienić wyraźnie luźne i uszkodzone oprzyrządowanie. Często śruby szypułkowe mogą być „powiększone” o milimetr lub dwie średnicy, aby uzyskać dobry chwyt w wcześniej luźnej trajektorii śruby. Czasami możliwe jest również wydłużenie śrub, ale wymaga starannego planowania przedoperacyjnego. Rozszerzenie fiksacji na sąsiedni segment należy rozważyć zwłaszcza, jeśli jest to związane z chorobą sąsiedniego segmentu, ale należy pamiętać, że nowo wbudowane poziomy również muszą osiągnąć fuzję. W praktycznym sensie, w przypadku nieudanego fuzji lędźwiowo-krzyżowej, rozciąganie fiksacji do kości biodrowej jest często bardzo skuteczne w poprawie stabilizacji.
dodanie przeszczepu międzyprzedsionkowego do nieudanego zespolenia tylno-bocznego jest sposobem dodawania materiału przeszczepu pod ściskaniem, a także poprawy stabilizacji. Dzięki zastąpieniu „miękkiej” przestrzeni dyskowej stosunkowo sztywniejszą klatką i kombinacją przeszczepu, poprawia się podparcie przedniej kolumny. W zależności od poziomu, może to być wykonane poprzez podejście przednie lub boczne. Można również zastosować technikę TLIF lub PLIF, ale najprawdopodobniej napotkają one blizny i zwiększą ryzyko uszkodzenia nerwów i łez twardówki.
równowaga strzałkowa
równowaga strzałkowa zawsze musi być zmierzona i rozliczona. Pacjent z pseudarthrosis w słabym wyrównaniu strzałkowym nadal będzie miał słaby wynik z fuzji stałej, jeśli ich wyrównanie nie jest adresowane. OSTEOTOMIA poprzez pseudarthrosis może być konieczne do osiągnięcia korekty, ale po raz kolejny, chirurg musi zoptymalizować szansę fuzji poprzez osiągnięcie dobrego dopasowania kości, sztywne i mocne konstrukcje oraz poprawę własnych czynników ryzyka pacjenta.
Stymulacja
istnieją pewne badania wspierające wykorzystanie stymulatorów PRĄDU STAŁEGO,47,48, a także impulsowej stymulacji pola elektromagnetycznego.49-51 niestety żadna z metod nie wykazała niezmiennie dobrych wyników i w dużej mierze nie wyszła z powszechnego stosowania.
przeszczep kości
nie ma syntetycznego substytutu przeszczepu grzebienia biodrowego, a to zawsze powinno być źródłem materiału przeszczepowego, gdy jest dostępny do leczenia pseudarthrosis. Podczas gdy wykazano, że rhBMP-2 jest równoważny autologicznemu przeszczepowi kości w dwóch dużych przeglądach systematycznych, 52,53 nie jest bez kosztów i powikłań. Allogeniczne przeszczepy nie mają właściwości osteoindukcyjnych, podobnie jak ceramika, taka jak fosforan trójwapniowy, a gdy chirurg leczy pseudarthrosis, należy unikać biologicznie obojętnych „wypełniaczy” takich jak te.
wniosek
Pseudarthrosis jest nadal jednym z najtrudniejszych problemów stojących przed chirurgiem kręgosłupa, a ryzyko jego wystąpienia należy omówić ze wszystkimi potencjalnymi pacjentami fuzji. Minimalizacja ryzyka pseudarthrosis rozpoczyna się na długo przed skalpel dotyka skóry, z badania przedoperacyjne zakończone, planowanie wykonywane, i wszystkie czynniki ryzyka złagodzone.
każdy pacjent fuzji, który nie reaguje w zwykły sposób, powinien zgłosić chirurgowi możliwość rozwoju pseudarthrosis. Chirurg, który „obwinia” pacjenta, nie wymierza sprawiedliwości swojemu pacjentowi ani sobie. Istotne badania obejmują rentgenowskie i tomografii komputerowej; subtelne zmiany w czasie Należy zauważyć.
Po ustaleniu diagnozy należy przeprowadzić ostrożną i otwartą dyskusję na temat korzyści i ryzyka interwencji chirurgicznej, ponieważ decyzja ta nie zawsze jest jasna. Po podjęciu decyzji o interwencji chirurgicznej chirurg musi wziąć pod uwagę sposób niepowodzenia, a także niezbędne kroki, które podejmie, aby osiągnąć fuzję w akceptowalnym ustawieniu. Niestety, nie można oczekiwać, że przebieg operacyjny i pooperacyjny będzie rutynowy i należy doradzić pacjentowi, aby nigdy nie osiągnął oczekiwanego wyniku z operacji indeksowej.