Generic Name: epinastine hydrochloride
Dosage Form: ophthalmic solution
Medically reviewed by Drugs.com. Last updated on June 1, 2020.
- Overview
- Side Effects
- Dosage
- Professional
- Pregnancy
- More
Indications and Usage for Epinastine HCl Ophthalmic Solution
Epinastine HCl Ophthalmic Solution 0.05% está indicado para a prevenção de prurido associado a conjuntivite alérgica.a dose recomendada é de uma gota em cada olho duas vezes por dia.o tratamento com
deve ser continuado durante todo o período de exposição (ou seja, até que a estação do pólen termine ou até que a exposição ao alergénio ofensivo termine), mesmo quando os sintomas estejam ausentes.formas posológicas e dosagens
solução contendo 0.5 mg/mL epinastina HCl
Contra-indicações
Nenhum
Avisos e Precauções
a Contaminação da Dica e Solução
os Pacientes devem ser instruídos a evitar permitindo a ponta do recipiente de dispensação de contato com o olho, estruturas circundantes, os dedos ou qualquer outra superfície, a fim de evitar a contaminação da solução de comum bactérias que causam infecções oculares. Danos graves no olho e subsequente perda de visão podem resultar da utilização de soluções contaminadas.o frasco deve ser mantido bem fechado quando não está a ser utilizado.
utilizar com lentes de contacto
os doentes devem ser aconselhados a não usar lentes de contacto se o seu olho estiver vermelho. Solução oftálmica de Epinastina HCl 0, 05% não deve ser utilizada para tratar a irritação relacionada com as lentes de contacto.o conservante na solução oftálmica de Epinastina HCl 0, 05%, cloreto de benzalcónio, pode ser absorvido por lentes de contacto moles. As lentes de contacto devem ser removidas antes da instilação da solução oftálmica oftálmica de Epinastina HCl 0, 05% e podem ser reinseridas 10 minutos após a sua administração.
uso oftálmico tópico apenas
solução oftálmica de Epinastina HCl 0.05% destina-se apenas a uso oftálmico tópico e não a administração ou administração oral.reacções adversas
reacções adversas
estudos clínicos experiência
Uma vez que os estudos clínicos são realizados em condições muito variáveis, as taxas de reacções adversas observadas nos estudos clínicos de um fármaco não podem ser directamente comparadas com as taxas dos estudos clínicos de outro fármaco e podem não reflectir as taxas observadas na prática.
As reacções adversas oculares mais frequentemente notificadas que ocorreram em aproximadamente 1-10% dos doentes foram sensação de ardor nos olhos, foliculose, hiperemia e prurido.
As reacções adversas não oculares notificadas mais frequentemente foram infecções (sintomas de constipação e infecções do tracto respiratório superior), observadas em aproximadamente 10% dos doentes, e cefaleias, rinite, sinusite, tosse aumentada e faringite, observadas em aproximadamente 1 – 3% dos doentes.algumas destas reacções foram semelhantes à doença subjacente a ser estudada.
experiência pós-comercialização
as seguintes reacções foram identificadas durante a utilização pós-comercialização de solução oftálmica oftálmica de Epinastina HCl 0, 05% na prática clínica. Uma vez que são reportados voluntariamente de uma população de tamanho Desconhecido, as estimativas de frequência não podem ser feitas. As reacções, que foram escolhidas para inclusão devido à sua gravidade, frequência de notificação, possível ligação causal à solução oftálmica oftálmica de Epinastina HCl 0, 05%, ou uma combinação destes factores, incluem: aumento do lacrimejo.
USO EM POPULAÇÕES ESPECÍFICAS
a Gravidez
Efeitos Teratogênicos
a Gravidez Categoria C
Em um embryofetal desenvolvimento de estudo em ratas prenhes, a toxicidade materna sem embryofetal efeitos, observou-se uma dose oral que foi cerca de 150.000 vezes o valor máximo recomendado ocular humano dose (MROHD) de 0.0014 mg/kg/dia mg/kg base. Foram observadas reabsorções totais e aborto num estudo embriofetal em coelhos grávidas com uma dose oral que foi aproximadamente 55 000 vezes superior à MROHD. Em ambos os estudos não foram observados efeitos teratogénicos induzidos pelo fármaco.a Epinastina reduziu o aumento de peso corporal das crias após uma dose oral em ratos fêmeas grávidas que foi aproximadamente 90 000 vezes superior à MROHD.não existem, no entanto, estudos adequados e bem controlados em mulheres grávidas. Uma vez que os estudos de reprodução em animais nem sempre são preditivos da resposta humana, a solução oftálmica de HCl Epinastina só deve ser utilizada durante a gravidez em 0, 05% se o potencial benefício justificar o potencial risco para o feto.um estudo em ratos lactantes revelou excreção de epinastina no leite materno. Desconhece-se se este medicamento é excretado no leite humano. Uma vez que muitos fármacos são excretados no leite humano, deve ter-se precaução quando a solução oftálmica oftálmica de Epinastina HCl é administrada a uma mulher a amamentar.a segurança e eficácia em doentes pediátricos com idade inferior a 2 anos não foram estabelecidas.
Utilização geriátrica
não foram observadas diferenças globais na segurança ou eficácia entre doentes idosos e doentes mais jovens.
Epinastina HCl Solução Oftálmica Descrição
Epinastina HCl Solução Oftálmica 0.05% is a clear, colorless, sterile isotonic solution containing epinastine HCl, an antihistamine and an inhibitor of histamine release from the mast cell for topical administration to the eyes.
Epinastine HCl is represented by the following structural formula:
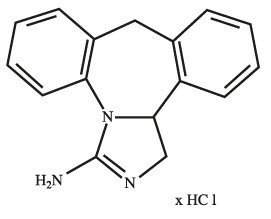
C16H15N3HCl Mol. Wt. 285.78
Chemical Name:
3-Amino-9,13b-dihydro-1H-dibenzimidazoazepine hydrochloride
Each mL contains: Active: Epinastine HCl 0.05% (0.5 mg/mL) equivalent to epinastine 0.044% (0.44 mg/mL); Preservative: Benzalkonium chloride 0.01%; Inactives: Edetato dissódico di-hidratado; água purificada; cloreto de sódio; fosfato de sódio monobásico, anidro; hidróxido de sódio e/ou ácido clorídrico (para ajuste do pH).
solução oftálmica de HCl Epinastina 0, 05% tem um pH de aproximadamente 7 e um intervalo de osmolalidade de 250 a 310 mOsm / kg.
solução oftálmica de Epinastina HCl-Farmacologia Clínica
mecanismo de Acção
Epinastina é um antagonista directo dos receptores H1 topicamente activo e um inibidor da libertação de histamina a partir da célula do mastro. A epinastina é selectiva para o receptor H1 da histamina e tem afinidade para o receptor H2 da histamina. A epinastina também possui afinidade para os receptores α1, α2 e 5-HT2.14 indivíduos, com conjuntivite alérgica, receberam uma gota de solução oftálmica de Epinastina HCl 0, 05% em cada olho, duas vezes por dia, durante 7 dias. No dia 7, foram atingidas concentrações plasmáticas máximas médias de epinastina de 0, 04±0, 014 ng/ml após cerca de duas horas, indicando uma baixa exposição sistémica. Embora estas concentrações tenham representado um aumento em relação às observadas após uma dose única, os valores do dia 1 e do dia 7 sob a curva (AUC) permaneceram inalterados, indicando que não há aumento na absorção sistémica com doses múltiplas. A epinastina liga-se 64% às proteínas plasmáticas. A depuração sistémica total é de aproximadamente 56 L / H e a semi-vida de eliminação plasmática terminal é de cerca de 12 horas. A epinastina é principalmente excretada inalterada. Cerca de 55% de uma dose intravenosa é recuperado inalterado na urina, com cerca de 30% nas fezes. Menos de 10% é metabolizado. A eliminação renal é principalmente por secreção tubular activa.carcinogénese, mutagénese, diminuição da fertilidade em estudos de carcinogenicidade dietética de 18 meses ou 2 anos em ratinhos ou ratos, respectivamente, a epinastina não foi carcinogénica em doses até 40 mg/kg .a Epinastina em lotes recentemente sintetizados foi negativa para Mutagenicidade no teste de Ames/Salmonella e no ensaio in vitro de aberração cromossómica utilizando linfócitos humanos. Foram observados resultados positivos com lotes iniciais de epinastina em dois estudos in vitro de aberração cromossómica realizados na década de 1980 com linfócitos periféricos humanos e com células V79, respectivamente. A epinastina foi negativa nos estudos de clastogenicidade in vivo, incluindo o ensaio de micronúcleo no ratinho e o ensaio de aberração cromossómica em hamsters chineses. A epinastina foi também negativa no ensaio de transformação celular utilizando células embrionárias de hamster sírio, no ensaio de mutação do ponto de células de mamíferos V79/HGPRT e no ensaio de síntese não programada de ADN in vivo/in vitro utilizando hepatócitos primários de ratos.a Epinastina não teve efeito na fertilidade de ratos machos. Observou-se uma diminuição da fertilidade em ratos fêmeas com uma dose oral até aproximadamente 90.000 vezes a MROHD.
Estudos Clínicos
Epinastina HCl a 0,05% demonstrou ser significativamente superior à do veículo para melhorar o prurido ocular em pacientes com conjuntivite alérgica em estudos clínicos usando dois modelos diferentes: (1) conjuntival antigen desafio (CAC), onde os pacientes foram dosados e, em seguida, recebeu o antigen passada na inferior, fundo de saco conjuntival; e (2) Estudos de campo ambiental em que os doentes foram tratados e avaliados durante a época de alergia no seu habitat natural. Os resultados demonstraram um rápido início de Acção para a epinastina HCl 0, 05% em 3 a 5 minutos após a provocação do antigénio conjuntival. A duração do efeito foi de 8 horas, tornando adequado um regime de duas vezes por dia. Este regime posológico demonstrou ser seguro e eficaz até 8 semanas, sem evidência de taquifilaxia.solução oftálmica de Epinastina HCl 0.05% é fornecido esterilizado em branco opaco LDPE garrafas de plástico com o conta-gotas dicas-e-branco em polipropileno (PP) caps da seguinte forma:
| 5 mL em frasco de 10 mL | NDC 51991-836-75 |
Armazenamento: Armazenar em 20° – 25°C (68° – 77°F) . Manter o frasco bem fechado e fora do alcance das crianças.
Informação do aconselhamento do doente
esterilidade da Ponta Do conta-gotas
os doentes devem ser aconselhados a não tocar na ponta do conta-gotas em qualquer superfície, uma vez que esta pode contaminar o Conteúdo (ver advertências e precauções, 5.1).
a utilização concomitante de lentes de contacto
os doentes devem ser aconselhados a não usar uma lente de contacto se o seu olho estiver vermelho. As doentes devem ser avisadas de que a solução oftálmica de Epinastina HCl 0, 05% não deve ser utilizada para tratar a irritação relacionada com o Lente de contacto. Os doentes devem também ser aconselhados a remover as lentes de contacto antes da instilação da solução oftálmica oftálmica de Epinastina HCl 0, 05%.o conservante na solução oftálmica de Epinastina HCl 0, 05%, cloreto de benzalcónio, pode ser absorvido por lentes de contacto moles. As lentes podem ser reinseridas após 10 minutos após a administração da solução oftálmica oftálmica de Epinastina HCl 0, 05%
uso oftálmico tópico apenas
apenas para administração oftálmica tópica.
Rx only
distribuído por:
Breckenridge Pharmaceutical, Inc.
Berlin, CT 06037
Manufactured by:
PrimaPharma, Inc.
San Diego, CA 92121
Rev: 04/2020
2323 04/20
PRINCIPAL DISPLAY PANEL – 5 mL Bottle Carton
NDC 51991-836-75
Epinastine HCl
Ophthalmic
Solution,
0.05%
FOR USE IN THE
EYES ONLY
sterile
Rx Only
5 mL sterile
breckenridge
A Towa
Company

| EPINASTINE HYDROCHLORIDE epinastine hydrochloride solution/ drops |
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
Labeler – Breckenridge Pharmaceutical, Inc. (150554335)
| Establishment | |||
| Name | Address | ID/FEI | Operations |
| PrimaPharma, Inc. | 079699106 | MANUFACTURE(51991-836) | |
More about epinastine ophthalmic
- Side Effects
- during Pregnancy or Breastfeeding
- dosage Information
- Pricing & Coupons
- em Espanhol
- 3 Reviews
- drug class: oftálmica anti-histamínicos e descongestionantes
recursos para o Consumidor
- Informações do Paciente
- Epinastina Oftálmica (Leitura Avançada)
recursos
- Informação de Prescrição
- Epinastina (Profissional Paciente Conselhos)
Outras marcas Elestat
Relacionados guias de tratamento
- Conjuntivite Alérgica
Medical Disclaimer