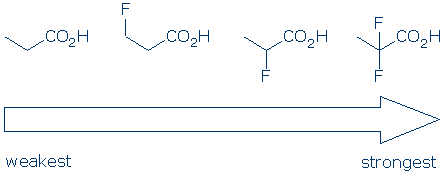
identificați cel mai acid H al unei Molecule
o abordare metodică funcționează cel mai bine. Pur și simplu, trebuie să scanați molecula pentru grupuri funcționale acide și apoi să clasificați reactivitatea acestor grupuri. Cel mai acid grup funcțional deține de obicei cel mai acid H din întreaga moleculă.
„scanare și rang” sună simplu, dar ascunde mai multe dificultăți care sunt elaborate mai jos.
scanați o moleculă pentru grupe funcționale acide cunoscute
protonii acizi sunt de obicei legați de O sau N. Prin urmare, primul pas este să căutați toate legăturile OH și NH.cu toate acestea, pe măsură ce localizați legăturile OH și NH, va trebui să decideți dacă acești atomi legați ar trebui să fie grupați într-un grup funcțional cu atomi vecini.
singura metodă convenabilă pentru identificarea unui grup funcțional este de a cunoaște deja unele. De exemplu, dacă știți că ROH, RCO2H și RSO3H sunt grupuri funcționale acide comune, nu veți avea probleme să găsiți grupuri acide în următoarea moleculă (grupurile corecte sunt marcate cu roșu).
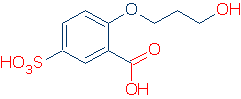
clasifică separat aciditatea OH și NH
Valorile pKa ale acizilor Oh și NH comuni se întind pe intervale largi și intervalele lor se suprapun. Clasamentul se desfășoară mai repede dacă clasificați acizii OH și NH separat, apoi comparați candidații de top din fiecare categorie.
metoda cea mai convenabilă pentru clasarea grupurilor acide este de a cunoaște deja valorile lor caracteristice pKa. Dacă cunoașteți aceste valori pentru toate grupările acide din molecula dvs., atunci grupul cu cel mai mic pKa conține cel mai acid H. caz închis.
dacă nu vă amintiți valorile pKa pentru toate grupele acide, câteva principii generale vă pot ghida.
#1 importanță – acizii încărcați pozitiv sunt mai puternici decât acizii neutri. Acizii încărcați negativ sunt rareori acizi. Dacă comparați valorile pKa ale acizilor Oh obișnuiți, veți vedea că acizii ROH2+ (care include H3O+ și R2OH+) sunt considerabil mai puternici decât acizii neutri, cum ar fi RCO2H, PhOH și ROH. Singurii acizi neutri care sunt mai puternici decât ROH2+ sunt H2SO4 și anumite alte RSO3H.
regula de încărcare formală se aplică și mai puternic acizilor NH. Diferența în pKa între H3O + și H2O este de 18 unități, în timp ce diferența în pKa între NH4+ și NH3 este de 26 de unități gigantice.
#2 importanță – căutați grupuri de activare, inclusiv RSO2, RC=O și pH.următoarea diagramă arată modul în care fiecare grup de atomi activează un acid OH (valorile pKa variază de la 16 la -2):
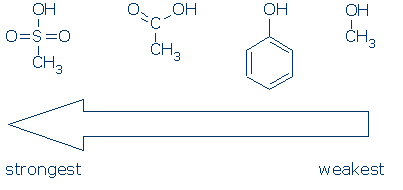
CH3 este considerat un grup de spectatori oriunde apare în aceste molecule. Este nepolar și nu exercită un efect inductiv semnificativ în câmp și este incapabil să delocalizeze sarcina. În consecință, este posibil să înlocuiți CH3 cu alte grupuri de spectatori (de exemplu, H și alte R) fără a afecta mult reactivitatea.
trebuie făcute două puncte suplimentare cu privire la grupurile de activare.
în primul rând, grupurile exercită un efect similar asupra acizilor NH (iar secvența de activare este aceeași: RSO2> RC=o> Ph). Așa cum se întâmplă, trebuie doar să înveți efectul Ph-ului asupra NH+ pentru acest curs:
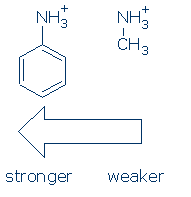
În al doilea rând, grupurile de activare trebuie să fie legate direct de grupul OH (sau NH) pentru a-l activa. Următorii compuși au valori pKa similare, deoarece grupurile de activare nu sunt legate direct de OH: CH3C(=o)CH2OH, PhCH2OH și CH3CH2OH.
#3 importanță – toate lucrurile fiind egale, un acid OH este mai acid decât un acid NH. Acest principiu poate fi foarte util dacă este utilizat corect. Preocuparea mea este că înțelegeți ce se înțelege prin „toate lucrurile fiind egale.”Aceasta înseamnă că O și N trebuie să aibă aceeași sarcină formală (articolul #1) și trebuie să fie legați de același grup de activare (articolul #2). Cu toate acestea, diferențele dintre grupurile de spectatori nu contează.
unele comparații valide includ:
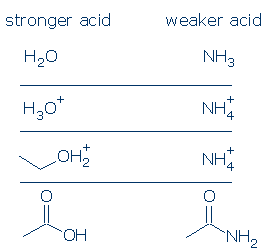
#4 importanță – în cadrul unei categorii de grup funcțional, utilizați efecte substituente pentru a compara acizii. Substituenții electronegativi sporesc de obicei aciditatea unui grup funcțional printr-o combinație de efecte de câmp și inductive. Aceste efecte sunt îmbunătățite atunci când 1) substituentul este situat mai aproape de grupul acid și 2) există substituenți multipli. Având în vedere aceste principii, ne așteptăm ca aciditatea acestor acizi carboxilici să urmeze această tendință: