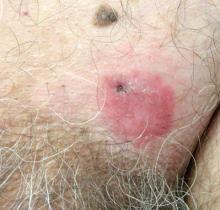
Un uomo di 70 anni presentava una placca eritematosa squamosa non pruriginosa nella regione sovrapubica sinistra della durata di 6 mesi che non aveva risposto all’ 1% di crema di terbinafina dopo 1 mese di trattamento di sospetta tinea cruris. La sua storia medica è stata notevole per l’ipertensione, iperlipidemia, broncopneumopatia cronica ostruttiva, iperplasia prostatica benigna, aneurisma dell’aorta addominale, dipendenza da alcol, disturbo da uso di tabacco e perdita di peso involontaria di 15 lb nell’ultimo anno.
La diagnosi: Malattia extramammaria di Paget
Una biopsia della placca ha rivelato una proliferazione intraepidermica di grandi cellule con abbondante citoplasma chiaro e grandi nuclei vescicolari distribuiti in tutta l’epidermide (Figura 1). Le cellule neoplastiche hanno macchiato positivo sia per la macchia periodica acido-Schiff (Figura 2) e CK7 (Figura 3). Il pannello di chimica e funzionalità epatica, l’analisi delle urine, i livelli di antigene carcinoembrionico e i livelli di antigene prostatico specifico erano compresi nell’intervallo di riferimento. Un conteggio completo delle cellule del sangue ha rivelato una lieve anemia megaloblastica. La successiva tomografia computerizzata del torace, dell’addome e del bacino ha rivelato un aneurisma aortico addominale e un allargamento prostatico senza alcuna evidenza di potenziali neoplasie. La colonscopia ha rivelato polipi iperplastici multipli e un adenoma tubulare. La cistoscopia era normale, tranne che per l’evidenza di ingrossamento della prostata. La citologia delle urine era insignificante. Il paziente è stato indirizzato per l’escissione della lesione con chirurgia micrografica di Mohs. Il follow-up è stato raccomandato ogni 3 mesi per i primi 2 anni successivi all’intervento chirurgico e ogni 6 mesi successivamente per monitorare eventuali recidive o neoplasie secondarie.
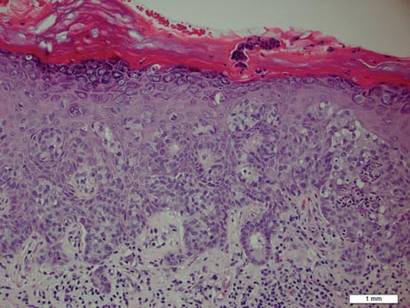
Figura 1. Proliferazione intraepidermica di grandi cellule con abbondante citoplasma chiaro e grandi nuclei vescicolari distribuiti in tutta l’epidermide come singole cellule e come aggregati di cellule di dimensioni variabili (H&E, ingrandimento originale ×200). (La barra di riferimento indica 1 mm.)
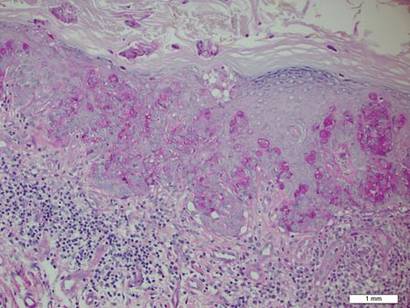
Figura 2. Il citoplasma granulare è risultato positivo alla periodica colorazione acido-Schiff (ingrandimento originale ×200). (La barra di riferimento indica 1 mm.)
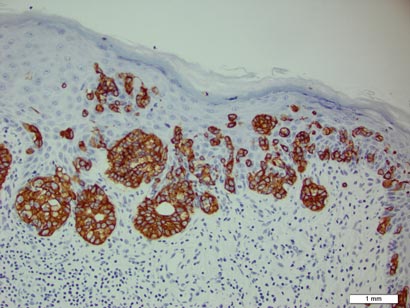
Figura 3. Le cellule neoplastiche di Paget sono risultate caratteristicamente positive alla colorazione per CK7 (ingrandimento originale ×200). (La barra di riferimento indica 1 mm.)
Sir James Paget descrisse per la prima volta la malattia mammaria di Paget del capezzolo nel 1874 nella sua relazione di 15 donne con eruzioni cutanee del capezzolo e dell’areola e successivo carcinoma del seno sottostante.1 Paget descrisse anche un paziente con un’eruzione simile sul glande e Crocker2 descrisse la malattia extramammaria di Paget (EMPD) dello scroto e del pene nel 1889. La differenza principale tra la malattia di Paget mammaria e l’EMPD è la posizione anatomica.
La malattia extramammaria di Paget è una condizione rara che colpisce tipicamente pazienti di età compresa tra 50 e 80 anni ed è più comune nelle donne e nelle razze dalla pelle bianca.3 La malattia di Paget extramammaria colpisce frequentemente i siti cutanei ricchi di ghiandole apocrine. Il sito più comunemente colpito è la vulva seguita da pelle perineale, perianale, scrotale e del pene. Meno comunemente, le ascelle, le natiche, le cosce, le palpebre e i canali uditivi esterni possono essere interessati.4
I pazienti con EMPD presentano tipicamente placche ben delimitate, non risolutive, eritematose ed eczematose che possono aver associato croste, desquamazione, escrescenze papillomatose, lichenificazione, ulcerazione o sanguinamento. Il sintomo più comune è il prurito, seguito da bruciore, irritazione, dolore e tenerezza.5 Dieci per cento dei pazienti sono asintomatici. L’intervallo medio tra insorgenza dei sintomi e diagnosi è di 2 anni.5
L’istopatologia rivela cellule di Paget neoplastiche diffusamente infiltranti, irregolari, all’interno dell’epidermide che sono grandi e vacuolate con abbondante citoplasma bluastro pallido e grandi nuclei vescicolari, che possono essere compressi centralmente o lateralmente. Le cellule possono essere distribuite singolarmente o in gruppi come fili, nidi o modelli ghiandolari all’interno dell’epidermide inferiore, creste di rete e strutture annessiali. Possono essere presenti anche ipercheratosi, acantosi e paracheratosi. Colorazione delle cellule di Paget per marcatori immunoistochimici di derivazione apocrina ed eccrina, comprese citocheratine a basso peso molecolare, proteina liquida della malattia cistica 15, macchia periodica acido–Schiff e antigene carcinoembrionico.5 Perrotto et al6 hanno studiato campioni 98 da pazienti 61 e hanno scoperto che CK7 era positivo in tutti i campioni EMPD, mentre CK20 e gross cystic disease fluid protein 15 erano positivi in grandi sottoinsiemi di EMPD primaria e secondaria. I casi di EMPD secondari all’adenocarcinoma anorettale sono stati in gran parte ERBB2 (precedentemente HER2/neu) negativo e CDX2 positivo.6
La diagnosi di EMPD deve essere seguita da un’indagine approfondita per i carcinomi sottostanti. In una revisione di 197 casi di EMPD, il 24% dei pazienti con EMPD presentava un carcinoma apocrino adnexale sottostante associato in situ o invasivo, che era associato a un tasso di mortalità più elevato rispetto ai pazienti senza questa neoplasia sottostante. Inoltre, il 12% dei pazienti con EMPD aveva una malignità interna sottostante associata.7 Queste neoplasie possono includere carcinomi dell’uretra, della vescica, della vagina, della cervice, dell’endometrio, della prostata, del colon e del retto. L’EMPD perianale ha una maggiore frequenza di neoplasie associate rispetto all’EMPD vulvare.5 La posizione dell’EMPD è correlata alla posizione della malignità sottostante; ad esempio, l’EMPD perianale è associato ad adenocarcinomi colorettali e l’EMPD del pene, dello scroto e dell’inguine è associato a neoplasie genitourinarie. Le indagini per la ricerca di neoplasie associate in pazienti con EMPD possono includere ecografia pelvica e/o risonanza magnetica, isteroscopia, colonscopia, sigmoidoscopia, cistoscopia, pielogramma endovenoso, mammografia e / o radiografia del torace.