de nulde wet van de thermodynamica
de nulde wet van de thermodynamica stelt dat systemen in thermisch evenwicht bij dezelfde temperatuur zijn.
leerdoelstellingen
Identificeer belangrijke implicaties van de nulde wet van de thermodynamica
Key Takeaways
Key Points
- aangenomen dat A, B en C drie systemen zijn, als A en C in thermisch evenwicht zijn, en A en B in thermisch evenwicht, dan zijn B en C in thermisch evenwicht.
- twee systemen zijn in thermisch evenwicht als ze warmte tussen elkaar kunnen overdragen, maar dat is niet het geval.
- de nulde wet van de thermodynamica impliceert dat temperatuur een hoeveelheid is die het waard is om te meten.
sleuteltermen
- thermisch evenwicht: twee systemen zijn in thermisch evenwicht als ze warmte tussen elkaar zouden kunnen overdragen, maar niet.
- Nulde wet van de thermodynamica: laat a, B en C drie systemen zijn. Als A en C in thermisch evenwicht zijn, en A en B in thermisch evenwicht, dan zijn B en C in thermisch evenwicht.
de nulde wet van de thermodynamica
Er zijn een paar manieren om de nulde wet van de thermodynamica vast te stellen, maar de eenvoudigste is als volgt: systemen die in thermisch evenwicht bestaan bij dezelfde temperatuur.
systemen zijn in thermisch evenwicht als ze geen warmte overdragen, ook al zijn ze in een positie om dat te doen, op basis van andere factoren. Bijvoorbeeld, voedsel dat ‘ s nachts in de koelkast is geweest is in thermisch evenwicht met de lucht in de koelkast: warmte stroomt niet meer van de ene bron (het voedsel) naar de andere bron (de lucht) of terug.
wat de nulde wet van de thermodynamica betekent is dat temperatuur iets waard is om te meten, omdat het aangeeft of warmte tussen objecten zal bewegen. Dit zal waar zijn, ongeacht hoe de objecten interageren. Zelfs als twee objecten elkaar niet raken, kan er nog steeds warmte tussen stromen, zoals door straling (als van een warmtelamp). Echter, volgens de nulde wet van de thermodynamica, als de systemen in thermisch evenwicht, geen warmtestroom zal plaatsvinden.
Er zijn meer formele manieren om de nulde wet van de thermodynamica vast te stellen, die gewoonlijk op de volgende wijze wordt gesteld:
zij A, B en C drie systemen. Als A en C in thermisch evenwicht zijn, en A en B in thermisch evenwicht, dan zijn B en C in thermisch evenwicht.
dit statement wordt symbolisch weergegeven in. Temperatuur wordt niet expliciet genoemd, maar het is impliciet dat temperatuur bestaat. Temperatuur is de hoeveelheid die altijd gelijk is voor alle systemen in thermisch evenwicht met elkaar.
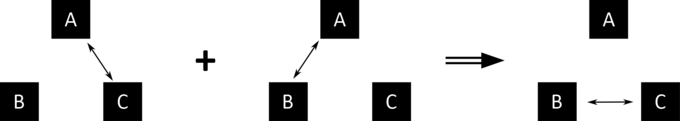
Nulde wet van de thermodynamica: de dubbele pijl staat voor thermisch evenwicht tussen systemen. Als systemen A en C in evenwicht zijn, en systemen A en B in evenwicht zijn, dan zijn systemen B en C in evenwicht. De systemen A, B en C hebben dezelfde temperatuur.