L’intolérance orthostatique est un sujet déroutant. Une partie de la confusion provient de l’appréciation récente des variantes cliniques de la maladie, d’autres proviennent de la compréhension émergente de ses diverses physiopathologies sous-jacentes, et d’autres proviennent de sa nomenclature, qui semble changer au moins chaque année.
Le terme orthostase signifie littéralement se tenir debout. L’intolérance orthostatique (OI) peut être définie comme « le développement de symptômes en position verticale, pendant la position debout qui sont soulagés par la position couchée. »Bien que l’utilisation d’un terme tel que l’intolérance orthostatique implique logiquement la présence de signes et de symptômes en position verticale, des variations du débit sanguin et de la régulation de la pression artérielle (TA) se retrouvent également en position couchée ou assise, mais celles-ci peuvent nécessiter un équipement spécial pour les détecter et peuvent donc ne pas être facilement discernables jusqu’à ce que le stress orthostatique devienne évident.
La position debout nécessite l’interaction du volume sanguin, des facteurs physiques, neurologiques, humoraux et vasculaires qui compensent les effets de la mise en commun veineuse gravitationnelle. Dans des conditions ordinaires, les altérations humorales aiguës ont peu à voir avec la réponse initiale à la position debout, mais peuvent jouer un rôle important lors d’une intolérance orthostatique chronique ou relativement tard pendant la position debout. En outre, les modifications de ces facteurs peuvent affecter les réponses au repos ou toniques et peuvent donc influencer la régulation vasculaire globale par des effets de fond.
Si les symptômes commencent en décubitus dorsal, il n’y a pas d’OI. L’OI transitoire est généralement ressentie lors de la déshydratation ou d’une maladie infectieuse. Les signes et symptômes typiques comprennent: perte de conscience ou déficits cognitifs moindres (perte de mémoire, diminution du raisonnement et de la concentration); difficultés visuelles; étourdissements; maux de tête; fatigue; augmentation de la TA (hypertension), diminution de la TA (hypotension); faiblesse; nausées et douleurs abdominales; transpiration; tremblements; et intolérance à l’exercice. Sauf en cas de danger (par exemple, debout sur une falaise), l’IO n’est pas mortelle. Certaines découvertes d’OI, telles que la nausée et la transpiration, se rapportent directement à l’activation autonome. Cependant, la perte de conscience, l’étourdissement sévère et la perte neurocognitive sont liés à un dysfonctionnement du système nerveux central (SNC) et obligent à la couché.
Les symptômes du SNC sont produits par une altération du flux sanguin cérébral impliquant peut-être le tronc cérébral. La vitesse du flux sanguin cérébral (CBF) est indiquée dans l’image ci-dessous pour deux formes courantes d’OI, la syncope vasovagale (VVS) et le syndrome de tachycardie posturale (POTS). L’autorégulation cérébrale peut être compromise comme dans les POTS et les VV et peut être réduite par une hyperventilation et une vasoconstriction cérébrale hypocapnéique. Une hyperventilation posturale involontaire, principalement une hyperpnée, est observée chez tous les patients VVS et 50% des patients POTS dans notre laboratoire. L’activité du nerf trijumeau, sympathique ou parasympathique peut également affecter le CBF orthostatique.
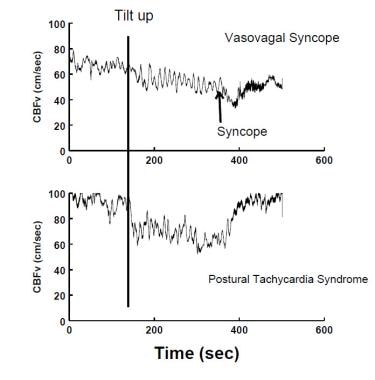 La diminution du CBFv mesurée par l’échographie Doppler transcrânienne survient lors d’un VVS (panneau supérieur) et dans le syndrome de tachycardie posturale (POTS) (panneau inférieur). Au cours de la VVS, la FBC diminue progressivement au début, puis de manière plus abrupte lorsque le patient perd connaissance de manière aiguë. Dans les POTS, le CBF est réduit de manière assez uniforme; il n’y a pas de perte de conscience bien que l’étourdissement soit typique.
La diminution du CBFv mesurée par l’échographie Doppler transcrânienne survient lors d’un VVS (panneau supérieur) et dans le syndrome de tachycardie posturale (POTS) (panneau inférieur). Au cours de la VVS, la FBC diminue progressivement au début, puis de manière plus abrupte lorsque le patient perd connaissance de manière aiguë. Dans les POTS, le CBF est réduit de manière assez uniforme; il n’y a pas de perte de conscience bien que l’étourdissement soit typique. L’intolérance orthostatique n’est pas toujours due à un dysfonctionnement autonome ou compensatoire et peut être due à des réponses inadéquates des mécanismes compensatoires aux facteurs de stress environnementaux. Par exemple, une personne déshydratée peut être incapable de se lever sans hypotension orthostatique résultante, mais aucun dysfonctionnement autonome n’est présent et, par conséquent, une hypotension orthostatique neurogène n’est pas présente; au lieu de cela, les systèmes autonomes et autres régulateurs ne peuvent pas compenser adéquatement la perte de volume sanguin circulant.
D’autre part, l’OI neurogène, dans laquelle la vasoconstriction adrénergique est défectueuse, est associée à une insuffisance autonome primaire; les patients atteints de maladies apparentées ne peuvent pas rester debout et présentent des anomalies autonomes détectables dans toutes les positions posturales. Par conséquent, l’IO englobe toute condition avec une insuffisance de débit sanguin, de fréquence cardiaque et de régulation cardiorespiratoire démontrable en position verticale mais pouvant également présenter des résultats anormaux dans toutes les positions. Dans de telles circonstances, l’IO est souvent la manifestation la plus évidente d’une altération plus répandue de la physiologie neurovasculaire intégrative.
Les différents types d’OI sont discutés dans les sections qui suivent.
Hypotension orthostatique initiale
L’hypotension orthostatique (OH) est définie comme une réduction soutenue de la pression artérielle systolique >20 mmHg ou de la pression artérielle diastolique > 10 mmHg dans les 3 minutes suivant la position debout ou après une inclinaison tête haute à ≥60o. L’exigence d’une réduction soutenue exclut hypotension orthostatique (OHI). Cette définition est relativement récente et a été élaborée par un groupe de consensus en 2011. Avant cela, il n’y avait pas de définition cohérente de OH. L’OH non neurogène peut être causé par des médicaments, une déshydratation, une perte de sang, l’âge et des maladies qui provoquent secondairement une hypovolémie aiguë ou chronique. L’OH neurogène est identifié avec une défaillance autonome due à une libération inadéquate de noradrénaline des neurones vasomoteurs sympathiques conduisant à une défaillance vasoconstrictrice. L’OH neurogène est rare chez les jeunes, car la plupart des causes d’insuffisance autonome sont acquises avec l’âge soit comme primaire (p. ex., insuffisance autonome pure, PAF) ou maladie secondaire (diabète). L’insuffisance autonome peut être primaire avec des formes de dysfonctionnement sympathique pré-ganglionnaires, post-ganglionnaires ou les deux (par exemple, la maladie de Parkinson). Cependant, il existe des variantes génétiques congénitales telles que la dysautonomie familiale (syndrome de Riley-Day) et le déficit en dopamine bêta-hydroxylase extrêmement rare (déficit en DBH). L’insuffisance autonome peut être auto-immune et peut se présenter avec le syndrome de Guillain-Barre post-infectieux, bien que le dysfonctionnement autonome semble avoir peu d’effet sur le résultat final. L’insuffisance autonome est le plus souvent acquise comme un aspect secondaire d’une maladie systémique telle que le diabète. La dénervation cardiaque sympathique est un aspect central de la maladie de Parkinson et peut être trouvée dans d’autres formes d’insuffisance autonome. L’innervation parasympathique cardiaque est également souvent défectueuse, ce qui entraîne une baisse constante de la TA avec une tachycardie réflexe faible lors d’un défi orthostatique, comme le montre l’image ci-dessous.
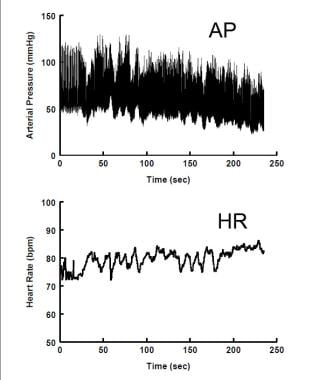 . La pression artérielle (panneau supérieur) diminue régulièrement en position verticale, tandis que la fréquence cardiaque (panneau inférieur) n’augmente que légèrement.
. La pression artérielle (panneau supérieur) diminue régulièrement en position verticale, tandis que la fréquence cardiaque (panneau inférieur) n’augmente que légèrement. L’OH non neurogène est relativement fréquent chez les jeunes. Elle peut être causée par des médicaments ou une hypovolémie (par exemple, déshydratation, hémorragie). C’est de loin la forme d’OH la plus courante chez les jeunes. Il n’y a pas de défaillance de la fonction autonome mais plutôt une compensation incomplète des facteurs de stress non autonomes excessifs.
L’OH (NOH) neurogène signifie une maladie autonome grave. Il est identifié avec une véritable défaillance vasoconstrictrice autonome due à la libération inadéquate de noradrénaline par les nerfs sympathiques et la HR peut ne pas augmenter de manière appropriée avec la position debout.
Syndrome de tachycardie posturale
Le syndrome de tachycardie posturale (POTS) est défini par des symptômes quotidiens d’intolérance orthostatique (OI) associés à une tachycardie verticale excessive mais pas à une hypotension (voir image ci-dessous).
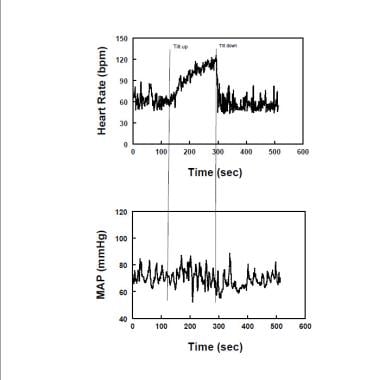 Diagramme montrant la fréquence cardiaque représentative (panneau supérieur) et la pression artérielle moyenne (MAP – panneau inférieur) pendant l’inclinaison verticale chez un patient atteint du syndrome de tachycardie posturale (POTS). La fréquence cardiaque augmente, tandis que la CARTE est stable tout au long de l’inclinaison dans les POTS.
Diagramme montrant la fréquence cardiaque représentative (panneau supérieur) et la pression artérielle moyenne (MAP – panneau inférieur) pendant l’inclinaison verticale chez un patient atteint du syndrome de tachycardie posturale (POTS). La fréquence cardiaque augmente, tandis que la CARTE est stable tout au long de l’inclinaison dans les POTS. Une tachycardie excessive chez l’adulte se définit par une augmentation verticale de l’heure supérieure à 30 bpm ou à une fréquence cardiaque supérieure à 120 bpm. Rappelons que la réponse HR normale à l’orthostase est une augmentation de la HR alors que les patients en insuffisance autonome n’ont souvent pas d’augmentation significative de la HR lorsqu’ils sont debout. Des incréments de fréquence cardiaque plus importants sont observés chez les jeunes avec des POTS, ce qu’il est important de savoir pour éviter le surdiagnostic. Les symptômes de l’OI doivent être concomitants à la tachycardie excessive. Pas de symptômes, pas de POTS. Une tachycardie et des symptômes concomitants sont très souvent observés lors de tests orthostatiques extrêmement prolongés qui sont donc à éviter si le diagnostic spécifique des POTS doit être posé. Les POTS ont souvent été divisés en sous-groupes désignés « POTS neuropathiques », dans lesquels il est supposé qu’une dénervation sympathique partielle ou une hypoactivité adrénergique est présente, et « POTS hyperadrénergiques », dans lesquels la suractivité adrénergique verticale domine l’image.
POTS neuropathiques
Comme décrit à l’origine, les POTS neuropathiques sont causés par une diminution de la vasoconstriction adrénergique sympathique dans les membres inférieurs, associée à une réduction des débordements de noradrénaline dans les jambes et une réduction de la vasoconstriction des membres inférieurs. Il y a souvent une augmentation du flux sanguin (« débit élevé ») dans les membres inférieurs même en décubitus dorsal. Une autre variante neuropathique présente une hémodynamique normale des membres inférieurs (« écoulement normal ») mais une diminution de la vasoconstriction adrénergique sympathique régionale dans la circulation splanchnique. Les POTS neuropathiques peuvent représenter une neuropathie autonome auto-immune. Ainsi, lorsqu’ils sont debout, les patients atteints de POTS neuropathiques ont une redistribution du sang supérieure à la normale vers le système vasculaire dépendant, provoquant une tachycardie et une vasoconstriction médiées par le baroréflexe. La réponse baroréflexe cardiaque est également émoussée dans des POTS. L’hypovolémie centrale peut également entraîner une hyperpnée et une hypocapnie chez près de 50% des patients par un mécanisme médié par le baroréflexe.
POTS hyperadrénergiques
La tachycardie des POTS hyperadrénergiques est causée par une augmentation de la potentialisation adrénergique pré-synaptique ou post-synaptique. Cela pourrait inclure une activité sympathique centrale et une activité nerveuse sympathique accrue. Une augmentation de l’activité sympathique en décubitus dorsal a été signalée, mais pas universellement. À ce jour, notre laboratoire n’a observé qu’une augmentation de l’activité sympathique musculaire verticale chez un patient de POTS. Une cause des POTS hyperadrénergiques est l’augmentation de la noradrénéphrine synaptique. L’hétérozygote de déficit en transporteur de noradrénaline est le meilleur exemple de ce mécanisme, mais a été trouvé comme une mutation autosomique dans un seul pedigree. Une déficience moins grave, peut-être épigénétique du transporteur de noradrénaline (NET) a également été démontrée récemment et pourrait avoir une prévalence plus large.
D’autres considérations de mécanisme incluent la modulation de la synapse adrénergique par une synthèse et une libération améliorées de la noradrénaline, et une affinité post-synaptique améliorée, qui peut être modulée par des transmetteurs locaux et humoraux. Ainsi, par exemple, les actions réciproques de l’oxyde nitrique (NO) et de l’angiotensine-II réduisent et améliorent respectivement l’activité adrénergique. Le rôle du NO en tant que neurotransmetteur inhibiteur est maintenant bien connu. Le NO nitrergique libéré par des nerfs ayant une activité parasympathique agit aux sites pré-synaptiques et post-synaptiques pour diminuer la transduction adrénergique, le processus par lequel une influx nerveux sympathique provoque une contraction du muscle lisse vasculaire. Cela comprend la réduction de la libération et de la liaison de la noradrénaline par la synapse neurovasculaire, l’interférence avec la neurotransmission post-synaptique, la dénaturation chimique de la noradrénaline et la régulation négative des récepteurs adrénergiques.
Inversement, des études de sympathoexcitation montrent que l’angiotensine-II agit à travers les récepteurs AT1 pour augmenter la production d’oxygène réactif (ROS) et d’espèces azotées dans le cerveau au niveau des neurones sympathiques pré-synaptiques et agissent en périphérie où ils produisent une augmentation pré- et post-synaptique de la transduction sympathique et une régulation positive des récepteurs adrénergiques. De plus, la libération et la liaison de la noradrénaline sont facilitées, tout comme les effets de la noradrénaline, en présence d’angiotensine-II. Cela dépend de manière critique de la formation de ROS, qui diminue également le NO, souvent en découplant l’oxyde nitrique synthase. Ce mécanisme se produit dans une variante de « POTS hyperadrénergiques » associée à une tachycardie, une pâleur, une vasoconstriction (« faible débit ») et une hypovolémie absolue même en décubitus dorsal. NON, la rénine plasmatique et l’aldostérone sérique sont diminuées, tandis que l’angiotensine-II plasmatique est augmentée par un défaut d’ECA-2.
La syncope posturale (syncope vasovagale, OI aiguë, évanouissement simple)
La syncope (évanouissement) est définie comme « une perte complète de conscience due à une hypoperfusion cérébrale globale transitoire caractérisée par un début rapide, une courte durée et une récupération complète spontanée. »La plupart des syncopes sont causées par une hypotension systémique et une diminution du flux sanguin cérébral. Il est possible qu’un accident vasculaire cérébral se présente de la même manière, bien qu’il n’ait jamais été signalé en pédiatrie. La syncope peut être causée par une hypotension orthostatique (OH), qui a déjà été discutée. OH est facilement exclu par un test debout de 3 minutes (voir la figure ci-dessous).
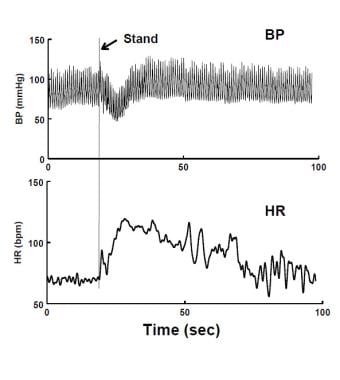 Hypotension orthostatique immédiate (IOH) au repos. Il y a une diminution de courte durée de la pression artérielle (BP – panneau supérieur) et une augmentation de la fréquence cardiaque (HR – panneau inférieur). La chute de BP est résolue en 20 secondes. Le patient a présenté des étourdissements transitoires.
Hypotension orthostatique immédiate (IOH) au repos. Il y a une diminution de courte durée de la pression artérielle (BP – panneau supérieur) et une augmentation de la fréquence cardiaque (HR – panneau inférieur). La chute de BP est résolue en 20 secondes. Le patient a présenté des étourdissements transitoires. La syncope est divisée entre la syncope cardiovasculaire, la maladie cardiopulmonaire fréquemment arythmique ou structurelle et la syncope à médiation réflexe ou neurale. La syncope cardiogénique peut mettre la vie en danger et avoir un mauvais pronostic à moins que la physiopathologie cardiaque ne soit traitée. La syncope cardiogénique n’est pas OI car la position couchée ne produit pas d’amélioration spécifique. La syncope réflexe a un bon pronostic. La syncope réflexe comprend la syncope vasovagale et la syncope situationnelle, y compris la syncope des sinus carotidiens, qui est essentiellement inconnue de la pédiatrie. La déglutition, la défécation, la miction et la syncope de la toux sont rarement observées chez les jeunes; et les variantes de toilettage des cheveux et de syncope d’étirement chez les adolescents sont particulières à l’adolescence. L’évanouissement pendant l’exercice soulève un « drapeau rouge » pour la syncope cardiogénique et toute activité sportive ultérieure doit être réduite jusqu’à la fin de l’évaluation cardiaque. Néanmoins, la cause la plus fréquente de syncope liée à l’exercice chez les jeunes ISVV. La syncope cardiogénique, bien qu’elle ne soit généralement pas liée à la position, ne peut pas être automatiquement rejetée après un premier évanouissement. Par conséquent, les premiers épisodes consécutifs avant l’évaluation cardiovasculaire doivent être traités comme urgents. Si l’évanouissement s’avère par la suite non cardiogénique, l’urgence est réduite et de simples manœuvres suffisent souvent pour faire face de manière aiguë aux circonstances. Les cardiologues sont souvent impliqués dans l’évaluation précoce de la syncope, car les évaluations initiales doivent déterminer si l’affection est d’étiologie cardiaque ou non cardiaque. Les maladies cardiaques, lorsqu’elles sont détectées, sont traitées spécifiquement. La syncope cardiaque peut d’abord se manifester pendant l’exercice, ce qui exerce le stress le plus physiologique sur les circulations coronaires, systémiques et pulmonaires et sur la fonction cardiaque globale. Une syncope liée à l’exercice ou une syncope avec des symptômes cardiaques (par exemple, tachycardie, douleur thoracique) indique une recherche d’une maladie cardiaque sous-jacente. Cependant, la syncope liée à l’exercice chez les jeunes est le plus souvent non cardiogénique et la physiologie peut ressembler à de simples évanouissements.
Cependant, même en cas d’hypotension neurocardiogène, la physiopathologie et les antécédents cliniques peuvent être plus complexes, impliquant des modifications de la respiration avec dyspnée et un dysfonctionnement chimioréflexe et baroréflexe pouvant suggérer une maladie cardiaque provoquée par l’exercice. Pourtant, malgré le degré relatif de préoccupation lié à l’évanouissement chez le jeune athlète, la plupart de ces épisodes sont d’origine non cardiogénique. Néanmoins, cela ne devrait pas éviter la nécessité d’évaluer ces patients pour une maladie cardiaque potentiellement mortelle. La syncope cardiogénique est bien décrite ailleurs et n’est pas discutée ici.
La syncope posturale et la syncope émotionnelle ou phobique comprennent les VV, le plus grand sous-groupe de la catégorie des syncopes réflexes. La perte de vasodilatation régionale ou à l’échelle du système est un élément de tous les VV, au moins en tant qu’événement terminal; cela peut ne pas toujours être dû à une perte d’activité nerveuse sympathique. La syncope posturale est une OI aiguë et environ les deux tiers des patients sont des femmes, tandis que les adolescents atteints de cette maladie ont tendance à être grands, minces et à croître rapidement. La perte de conscience est souvent précédée d’un prodrome de symptômes d’OI, en particulier des étourdissements, des nausées, des sueurs, une faiblesse et une vision floue. Traditionnellement, on croyait que la syncope posturale était due à des réflexes d’un cœur hypercontractile et sous-rempli analogue au réflexe de Bezold-Jarisch. Des preuves du contraire se sont accumulées; un tel stimulus serait de courte durée. En raison du déchargement des barorécepteurs, très peu de nerfs afférents ont été excités dans les expériences originales d’Oberg et Thoren chez le chat hémorragique moribond. Les VV peuvent survenir dansun receveur de greffe dénervé ventriculaire et le cœur n’est ni vide ni hypercontractile avant la syncope. Jusqu’à présent, nous ne comprenons pas complètement la physiopathologie de la simple évanouissement.
Dans la variante la plus courante d’évanouissement postural survenant chez les patients jeunes, l’évanouissement postural comprend trois étapes (voir l’image ci-dessous), qui ressemblent fortement aux modifications circulatoires constatées lors d’une hémorragie.
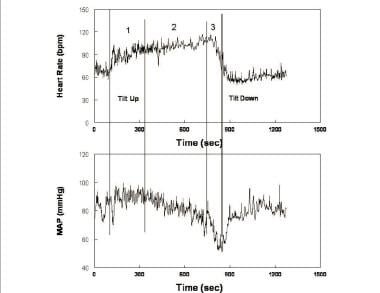 Fréquence cardiaque (panneau supérieur) et pression artérielle moyenne (MAP – panneau inférieur) lors de l’inclinaison verticale chez un patient syncope postural représentatif. Les changements au cours de l’inclinaison se produisent en trois étapes: au cours de la première étape (1), après l’hypotension initiale, la MAP se stabilise légèrement plus que la pression au repos tandis que la fréquence cardiaque augmente. Au cours de la deuxième étape (2), la MAP commence à baisser progressivement, tandis que la fréquence cardiaque continue d’augmenter. Notez que l’augmentation de la fréquence cardiaque du décubitus dorsal au debout répond aux critères de tachycardie pour le syndrome de tachycardie posturale (POTS). Au cours de la troisième étape (3), la MAP puis la fréquence cardiaque chutent brusquement et rapidement à mesure que la perte de conscience s’accentue.
Fréquence cardiaque (panneau supérieur) et pression artérielle moyenne (MAP – panneau inférieur) lors de l’inclinaison verticale chez un patient syncope postural représentatif. Les changements au cours de l’inclinaison se produisent en trois étapes: au cours de la première étape (1), après l’hypotension initiale, la MAP se stabilise légèrement plus que la pression au repos tandis que la fréquence cardiaque augmente. Au cours de la deuxième étape (2), la MAP commence à baisser progressivement, tandis que la fréquence cardiaque continue d’augmenter. Notez que l’augmentation de la fréquence cardiaque du décubitus dorsal au debout répond aux critères de tachycardie pour le syndrome de tachycardie posturale (POTS). Au cours de la troisième étape (3), la MAP puis la fréquence cardiaque chutent brusquement et rapidement à mesure que la perte de conscience s’accentue. Après hypotension orthostatique initiale et restauration de l’homéostasie circulatoire, la TA se stabilise tandis que la HR augmente au stade 1. La stabilité de la pression artérielle distingue les faibles posturaux des vrais OH. BP présente souvent des fluctuations rythmiques au cours de cette étape appelée « ondes de Mayer” avec une période d’environ 10 secondes (0,1 Hz). Une périodicité similaire est partagée par les fluctuations de la fréquence cardiaque, de l’activité du nerf sympathique et de la résistance périphérique. Les fluctuations sont le temps en boucle fermée de la réponse baroréflexe sympathique (c’est-à-dire le temps nécessaire à la détection et à la compensation des changements de BP). Les oscillations sont accentuées lors des réductions du volume sanguin central, comme lors de l’orthostase. Au cours de cette étape, la résistance périphérique totale augmente pour maintenir la pression artérielle face à un débit cardiaque réduit (voir l’image ci-dessous).
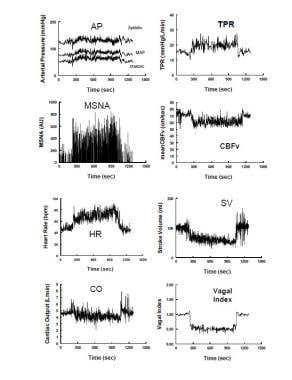 Changements hémodynamiques et neurovasculaires au cours de l’inclinaison verticale chez un volontaire sain représentatif. Le panneau de gauche montre de haut en bas: la pression artérielle, l’activité du nerf sympathique musculaire (ARNSM) du nerf péronier, la fréquence cardiaque (HR) et le débit cardiaque. Le panneau de droite montre de haut en bas: résistance périphérique totale (TPR), vitesse du flux sanguin cérébral (CBFv) par échographie Doppler transcrânienne, volume d’AVC et indice vagal calculé à partir de la composante arythmie sinusale respiratoire du spectre de fréquence de la variabilité HR. Pendant l’inclinaison verticale à 275 secondes (s), les pressions systolique, diastolique et artérielle augmentent légèrement, tandis que la pression du pouls diminue avec une diminution du volume de la course d’environ 40%. HR augmente de sorte que le débit cardiaque n’est diminué que de 20% en raison de l’augmentation de HR. CBFv diminue de 5 à 10%. La résistance vasculaire périphérique totale et l’activité nerveuse sympathique musculaire augmentent, tandis que l’indice vagal diminue, reflétant respectivement l’activation sympathique et le retrait parasympathique.
Changements hémodynamiques et neurovasculaires au cours de l’inclinaison verticale chez un volontaire sain représentatif. Le panneau de gauche montre de haut en bas: la pression artérielle, l’activité du nerf sympathique musculaire (ARNSM) du nerf péronier, la fréquence cardiaque (HR) et le débit cardiaque. Le panneau de droite montre de haut en bas: résistance périphérique totale (TPR), vitesse du flux sanguin cérébral (CBFv) par échographie Doppler transcrânienne, volume d’AVC et indice vagal calculé à partir de la composante arythmie sinusale respiratoire du spectre de fréquence de la variabilité HR. Pendant l’inclinaison verticale à 275 secondes (s), les pressions systolique, diastolique et artérielle augmentent légèrement, tandis que la pression du pouls diminue avec une diminution du volume de la course d’environ 40%. HR augmente de sorte que le débit cardiaque n’est diminué que de 20% en raison de l’augmentation de HR. CBFv diminue de 5 à 10%. La résistance vasculaire périphérique totale et l’activité nerveuse sympathique musculaire augmentent, tandis que l’indice vagal diminue, reflétant respectivement l’activation sympathique et le retrait parasympathique. Au cours de l’étape 2, la TA diminue lentement à mesure que le baroréflexe augmente encore la HR. La diminution de la TA est le plus souvent liée à une diminution du débit cardiaque, même si l’activité sympathique et la résistance artérielle périphérique sont maintenues. Par la suite, les oscillations de résistance et de pression diminuent malgré une sympathoexcitation soutenue. L’hyperpnée et l’hypocapnie surviennent à ce stade chez la plupart des patients. Chez certains patients, le stade 2 est abrégé. Cela est particulièrement vrai pour les patients atteints de syncope convulsive chez lesquels des épisodes surviennent brusquement en association avec une asystolie.
La syncope convulsive ou asystolique (voir l’image ci-dessous) se distingue de l’épilepsie par une diminution de l’activité de l’EEG dans la première et par une résolution presque immédiate de la posture opisthotonique par couché. Malgré les apparences, les évanouissements asystoliques ne sont pas cardiogéniques mais à médiation réflexe et constituent une forme relativement rare d’évanouissement vasovagal simple qui peut également être trouvée dans les évanouissements phobiques.
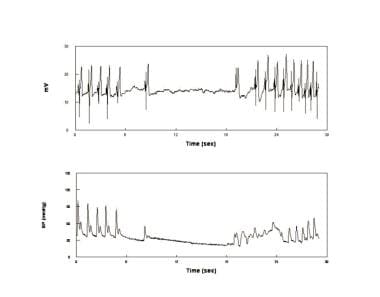 Un évanouissement asystolique. Électrocardiogramme (panneau supérieur) et pression artérielle (TA) (panneau inférieur) chez un patient qui a présenté une asystole pendant un évanouissement. Ceci est épisodique, relativement peu fréquent et sans rapport avec la maladie intrinsèque du nœud sinusal. Les évanouissements asystoliques sont associés à des postures opisthotoniques et ont parfois été appelés syncopes convulsives.
Un évanouissement asystolique. Électrocardiogramme (panneau supérieur) et pression artérielle (TA) (panneau inférieur) chez un patient qui a présenté une asystole pendant un évanouissement. Ceci est épisodique, relativement peu fréquent et sans rapport avec la maladie intrinsèque du nœud sinusal. Les évanouissements asystoliques sont associés à des postures opisthotoniques et ont parfois été appelés syncopes convulsives. Plusieurs mécanismes ont été proposés pour le VVS chez certains patients. Les patients VVS avec une diminution de la pression artérielle au repos avaient une réduction de la synthèse de la tyrosine hydroxylase et de la NE, et un groupe de normotenseurs présentait un excès NET. Un déficit sélectif de vasoconstriction splanchnique et de venoconstriction a également été démontré. Les symptômes de l’OI prodromique commencent au stade 2 et les cliniciens peuvent donc poser un diagnostic de POTS en laboratoire. L’histoire clinique offre le meilleur moyen de distinguer les patients présentant des évanouissements épisodiques aigus avec de longues périodes exemptes de symptômes (syncope posturale) des POTS, dans lesquels les symptômes sont chroniquement présents; En effet, le prodrome de l’évanouissement simple et les signes et symptômes des POTS sont similaires car ils peuvent avoir une physiopathologie initiale similaire – réduction excessive du volume sanguin central entraînant une tachycardie réflexe. Des évanouissements posturaux, correspondant à des patients en POTS hyperadrénergiques pâles et vasoconstrictés, ne sont généralement pas observés. Pour la plupart, dans notre expérience, les patients de POTS ont des symptômes quotidiens mais ne s’évanouissent pas, tandis que les patients syncopes ont des évanouissements épisodiques mais pas des symptômes quotidiens. Cette distinction est devenue moins claire avec le temps. Ainsi, certains patients souffrant d’IO chroniques (POTS) s’évanouissent et certains évanouissements épisodiques présentent également des symptômes quotidiens sous-jacents d’IO. Cependant, l’évanouissement des patients de POTS en laboratoire doit être considéré avec prudence et ne peut pas, en soi, être considéré comme une preuve d’évanouissement réel. Une histoire clinique ”réelle » compatible avec l’évanouissement est obligatoire.
Dans la dernière étape, l’étape 3, le CBF, le BP et le HR tombent rapidement dans cet ordre, défiant apparemment la causalité du BP–CBF. Des effets similaires sont souvent observés dans des systèmes non linéaires de toutes sortes lorsqu’un signal externe suffisamment fort entraîne des signaux liés. Ainsi, des travaux récents montrent que les bras efférents baroréflexes cardiovagaux et sympathiques sont altérés avant l’évanouissement et que les ondes de Mayer disparaissent. De même, l’autorégulation cérébrale devient altérée avec l’entraînement de CBF, BP et HR par un signal extrinsèque, qui peut être une respiration hyperpnéique. On ne sait pas encore pourquoi l’intégrité baroréflexe est perdue, mais cela entraîne des relations fonctionnelles anormales BP-HR et BP-MSNA telles que HR, BP et l’activité du nerf sympathique diminuent, entraînant une bradycardie, une hypotension et un silence sympathique. La faiblesse est associée à une vasodilatation systémique marquée tandis que la FBC diminue avec une baisse de la pression artérielle. Des travaux récents remettent en question la nécessité du silence sympathique en tant que précipitant de l’hypotension finale. Alors que la vasodilatation se produit toujours, le baroréflexe sympathique peut échouer avec ou sans silence sympathique en raison d’une perte de la relation fonctionnelle entre la pression artérielle et l’activation sympathique. La perte de connexions fonctionnelles entre la BP et l’activité du nerf sympathique, mais pas la fréquence cardiaque, survient chez les patients présentant une syncope vasodépressive où une vasodilatation sans bradycardie se produit. Bien qu’il y ait une perte du baroréflexe efférent sympathique entraînant une perte progressive de vasoconstriction compensatoire, le baroréflexe cardiovagal reste intact.
Les POTS et la syncope posturale sont tous deux associés à une hyperventilation hyperpnéique. L’hyperpnée et l’hypocapnie qui en résulte précèdent l’inconscience chez pratiquement tous les patients atteints de syncope vasovagale. L’hypotension et la bradycardie peuvent s’expliquer par le réflexe d’étirement pulmonaire sans entrave par des effets baroréflexes compensateurs. La cause de l’hyperpnée n’est pas claire, mais peut être liée au bras efférent ventilatoire du baroréflexe artériel. Des résultats similaires d’hyperpnée sont trouvés chez environ 50% des patients POTS atteints d’hypovolémie centrale qui ne s’évanouissent pas.
Une syncope très fréquente ou extrêmement prolongée peut indiquer une syncope psychogène ou des réponses de conversion. Ceux-ci se distinguent facilement de la vraie syncope en laboratoire car il n’y a pas d’hypotension ou de CBF réduite, mais les attaques peuvent être réelles pour le patient. Certains patients peuvent avoir eu des VV de bonne foi entrecoupées d’épisodes psychogènes plus fréquents sous forme de réponses apprises ou conditionnées. Une école de pensée suggère que de tels patients éprouvent réellement les symptômes de véritables VV sans les signes.
L’intolérance orthostatique est courante mais souvent mal comprise. L’étude de la maladie est un domaine évolutif de l’étude physiologique intégrative. Le VVS postural est identifié avec une intolérance orthostatique aiguë. Malgré son omniprésence, les scientifiques ne comprennent pas encore pourquoi certaines personnes s’évanouissent. POTS est identifié avec une intolérance orthostatique chronique. POTS, cependant, reste une entité hétérogène, probablement d’étiologies variées. Jusqu’à ce qu’une meilleure compréhension soit obtenue, le traitement reste plus conjectural que scientifique.