A Microbial Biorealm page on the genus Citrobacter freundii
Classification
Higher order taxa
Bacteria; Proteobacteria; Gammaproteobacteria; Enterobacteriales; Enterobacteriaceae; Citrobacter
Species
NCBI: Taxonomy
Citrobacter Freundii
Description and significance
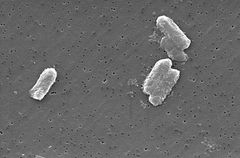 Photo: Citrobacter arter, herunder Citrobacter freundii, er aerobe gram-negative baciller. Citrobacter freundii er lange stavformede bakterier typisk 1-5 liter i længden . De fleste C. freundii-celler er omgivet af mange flageller, der bruges til at bevæge sig rundt, men nogle få er ikke-bevægelige. Dens habitat omfatter miljøet (jord, vand, spildevand), mad og tarmkanalerne hos dyr og mennesker . Det tilhører familien af Enterobacteriaceae.
Photo: Citrobacter arter, herunder Citrobacter freundii, er aerobe gram-negative baciller. Citrobacter freundii er lange stavformede bakterier typisk 1-5 liter i længden . De fleste C. freundii-celler er omgivet af mange flageller, der bruges til at bevæge sig rundt, men nogle få er ikke-bevægelige. Dens habitat omfatter miljøet (jord, vand, spildevand), mad og tarmkanalerne hos dyr og mennesker . Det tilhører familien af Enterobacteriaceae.
som et opportunistisk patogen er C. freundii ansvarlig for en række signifikante opportunistiske infektioner. Det vides at være årsagen til en række nosokomiale infektioner i luftvejene, urinvejen, blodet og flere andre normalt sterile steder hos patienter . 29% af alle opportunistiske infektioner . Derfor er en af hovedårsagerne til, at mange forskellige stammer og plasmider af C. freundii-genomet sekventeres, for at finde antibiotika, der kan bekæmpe disse opportunistiske infektioner.
overraskende spiller denne infektiøse mikrobe hos mennesker en positiv rolle i miljøet. C. freundii er ansvarlig for at reducere nitrat til nitrit i miljøet . Denne afgørende omdannelse er et vigtigt stadium i kvælstofcyklussen. Og genanvendelse af kvælstof er meget vigtigt, fordi Jordens atmosfære er omkring 85% nitrogen . På grund af dets vigtige bidrag til miljøet er der derfor en anden motivation for sekventering af genomet af C. freundii.Citrobacter slægten blev opdaget i 1932 af Gillen. Kulturer af C. freundii blev isoleret og identificeret i samme år fra jordekstrakter .
Genomstruktur
ingen oplysninger om det komplette genom af C. freundii er tilgængelig online, selvom nogle individuelle stammer og plasmider af mikroben er blevet sekventeret. 3, fordi det er det største plasmid og koder for en stor mængde proteiner. Dens sekvens blev afsluttet den 6. januar 2005. Det er et cirkulært DNA-plasmid, og det er 89.468 nukleotidbasepar lange. Længden af plasmidet er 0,089468 (Mbp). Det består af 51,0% GC-indhold og koder for 105 proteiner .
et andet vigtigt træk ved C. freundii-genomet er, at det er den eneste mikrobe i Enterobacteriaceae-familien, der indeholder et plasmid, der koder for L-methionin-lyase (MGL). Nukleotidsekvensen af plasmidet indeholder en 3000 bp lang EcoRI-indsats . Fragmentet indeholder også to åbne læserammer. Den første ramme består af 1.194 nukleotider, og den anden-1.296 nukleotider.Den første ramme, kendt som megL-genet, koder for et protein med 398 aminosyrerester, der har sekvenshomologi med MGL ‘ er fra forskellige kilder. Den anden ramme koder for et protein med sekvenshomologi med proteiner, der tilhører familien af permeaser .
C. freundii OS60 AmpC-Kurt-lactamase-genet er også blevet sekventeret, og det er sammensat af 1197 nukleotider. Det koder for en 380 aminosyre lang forløber og indeholder et 19 restsignalpeptid i 5′ – enden . Dette gen koder for et modent protein, der har en molekylvægt på 39 781 Dalton. Aminosyrepositionerne i disse precursorer er suprisinlgy identiske med rester i E. coli K12 kromosomale AmpC-Kurt-lactamaser .
en anden vigtig stamme i genomet af C. freunii er GN346, som er et klinisk isolat, der blev genvundet i 1965. Denne stamme producerer cephalosporinase, som har evnen til at hydrolysere og inaktivere anibitoics cephalosporiner og cephamyciner . De strukturelle og promotorregioner i cephalosporinase-genet er 1408 nukleotider lange. Aminosyresekvensen er sammensat af 361 aminosyrer med en molekylvægt på 39.878 Da .
cellestruktur og metabolisme
cellestrukturen af C. freundi er lang og stangformet, normalt 1-5 liter i længden. Ydersiden af cellen indeholder mange flageller, der bruges til motalitet . Da C. freundii er gram-negative bakterier, indeholder den to membraner (indre og ydre).Det periplasmiske rum ligger mellem de to membraner. Den ydre membran indeholder ikke en energikilde; men den indeholder mange poriner indlejret i, der hjælper organismen med at erhverve vigtige ioner . I modsætning til gram-positive bakterier indeholder C. freundii-celler ikke en tyk cellevæg, der består af peptidoglycan. for metabolisme har C. freundii en fantastisk evne til at vokse på glycerol som den eneste kulstof-og energikilde. I denne proces fermenteres glycerol ved en dismutationsproces. Denne proces kræver to veje . I den første vej dehydreres glycerol af en NAD1-bundet glyceroldehydrogenase til dihydroksyaceton. Dette er en af de mest almindelige årsager til denne sygdom . I den anden vej dehydreres glycerol af coensymet B12-afhængig glycerol dehydratase til dannelse af 3-hydroksipropionaldehyd . Dette produkt reduceres til det vigtigste fermenteringsprodukt 1,3-propandiol af den NADH-bundne 1,3-propandiol dehydrogenase, som regenererer NAD1. DHA regulon koder for de fire væsentlige faser af disse to veje. Utroligt nok induceres udtrykket af dha regulon kun, når glycerol er til stede .
celler af C. freundii er også i stand til at metabolisere lactose eller citrat som en carbonkilde .
økologi
Citrobacter freundii findes almindeligvis i miljøet, hovedsageligt i jord, vand og kloakering. De er en indikator for potentiel forurening af vand. De findes også på forskellige organer af syge dyr, herunder pattedyr, fugle, krybdyr og amfibier . De er ikke kendt for at interagere med andre organims.
i miljøet kan C. freundii konvertere nitrat eller ammoniumionen (som er et nitrogenatom kombineret med fire hydrogenatomer) til nitrit; denne reaktion forekommer i miljøet såvel som i fordøjelseskanalen hos mennesker og andre dyr . Efter at det omdanner nitrat til nitrit i miljøet, omdannes nitrit til nitrogen, og dette sidste trin fuldender nitrogencyklussen i Jordens atmosfære, der består af 85% nitrogen . Denne organisms økologiske rolle inkluderer ikke kun sin vigtige rolle i nitrogencyklussen, fordi den også kan akkumulere uran (som er det grundlæggende materiale til nuklear teknologi) ved at opbygge fosfatkomplekser . Citrobacter freundii er også blevet undersøgt for bionedbrydning af garvesyre anvendt i tannerys .
patologi
som et opportunistisk patogen er Citrobacter freundii ofte årsagen til signifikante opportunistiske infektioner, hvilket betyder, at det generelt ikke forårsager sygdom hos raske menneskelige værter. De påvirker kun patienter med et svagt immunsystem, hvilket betyder, at de har brug for en “mulighed” for at inficere personen . Derfor er Citrobacter-arter kendt for at forårsage en lang række nosokomiale infektioner i luftvejene, urinvejen og blodet hos patienter med et undertrykt immunsystem . Lever -, galde-og bugspytkirtelsygdom er også almindelige sygdomme, der er forårsaget af C. freundii. Galdevejen er det mest almindelige infektionssted af C. freundii-bacillerne .
en dødelig sygdom, som C. freundii har været forbundet med, er neonatal meningitis. Neonatal meningitis er betændelse i hjernehinderne (systemet med membraner, der omgiver CNS) på grund af bakteriel invasion . Dødeligheden af Citrobacter meningitis er uacceptabelt høj, med dødsfald hos patienter fra 25 Til 50 %. Desuden vedvarer alvorlige neurologiske problemer stadig hos 75% af de overlevende. I denne sygdom er Citrobacter freundii i stand til at trænge ind i blod-hjernebarrieren, der består af choroidpleksens epitel og hjernekapillærendotelet .
Test udført af Badger et. al i artiklen”Citrobacter freundii invaderer og replikerer i humane Hjernemikrovaskulære endotelceller” antyder, at bakteriel proliferation af C. freundii finder sted på det intracellulære niveau, hvilket havde været i strid med den generelle videnskabelige tanke. Resultaterne indikerer, at C. freundii krydser vakuoler, replikerer og frigives i den basolaterale side af den menneskelige hjerne mikrovaskulære endotelceller (HBMEC) for at krydse blod-hjerne-barrieren. Yderligere analyse kan potentielt muliggøre terapeutiske strategier til behandling af infektioner. Der er stadig ingen terapeutisk behandling tilgængelig .
visse sygdomme undersøgt i ørred og cyprinider er også forårsaget af C. freundii. C. freundii forårsager unormale inflammatoriske ændringer i ørredens tarm og inflammatoriske og nekrotiske ændringer i cyprinids indre organer. Sygdommen blev opdaget ved hjælp af kunstig infektion med en ren kultur af C. freundii. Denne opdagelse etablerede C. freundii som en årsag til fiskesygdom .
i en casestudie af Journal of Medical Microbiology udviklede en patient peritonitis og tunnelinfektion på grund af Citrobacter freundii, hvilket er usædvanligt. Patienten var i kontinuerlig ambulant peritonealdialyse. Normalt er de forårsagende stoffer gram-positive mikroorganismer, især Staphylococcus aureus og Staphyloccus edpidermis. Der er heller ingen kendte rapporter om tunnelinfektion på grund af C. freundii. Indledende antibiotikabehandling virkede ikke, og infektionen fortsatte med at fortsætte, indtil kateteret blev fjernet. Dette er klinisk signifikant, fordi Citrobacter Freundii viser forskellig antibiotisk modtagelighed, hvorfor initial terapi ikke var vellykket. Patienten reagerede ikke på behandlingen, før kateteret blev fjernet, hvilket viser, at Citrobacter freundii er opportunistiske patogener, der påvirker indlagte og immunkompromitterede patienter .
anvendelse til bioteknologi
i biotekindustrien producerer Citrobacter freundii mange vigtige egenskaber.De første stoffer, den producerer, er fosfatase. Fosfataseaktivitet af C. freundii er blevet postuleret til at være involveret i blyakkumulering, som kan have spillet en vigtig rolle i biotekindustrien. Fosfataseaktiviteten af C. freundii er også blevet opdaget at have resistens over for nogle diagnostiske reagenser .dette er en af de mest almindelige metoder til behandling af bakteriel selenocystein-beta-lyase, der anvendes til behandling af bakteriel selenocystein-beta-lyase, som specifikt katalyserer spaltningen af L-selenocystein til L-alanin, er blevet oprenset fra Citrobacter freundii. Den er monomer med en molekylvægt på ca. 64.000 og indeholder 1 mol pyridoksal 5 ‘ – phosphat pr.mol. Det er også vigtigt at bemærke, at det er en af de mest almindelige typer af beta-chlor-L-alanin, der dannes NH3, pyruvat .
C. Freundii-stammer bærer også et plasmid, der koder for klasse 1 AmpC cephalosporinase. Disse kan hydrolysere inaktivere nye cephamyciner og cephalosporiner .
aktuel forskning
en lille skala forskning vedrørende visse stammer af C. freundii blev gjort for nylig på University of Tennessee, Knoksville. Betydningen af visse tetracyclin-og streptomycinresistensgener og klasse 1-integroner i C. freundii isoleret fra mælkejord og ikke-mejeri jord blev evalueret. En stamme af C. freundii ekstraheret fra mælkebedriftsjord bar klasse 1-integroner med forskellige indsatte genkassetter. Resultaterne af denne lille undersøgelse antydede, at tilstedeværelsen af flere resistensgener og klasse 1-integroner i C. freundii i mælkebedriftsjord kan fungere som et reservoir af antimikrobielle resistensgener og kunne spille en rolle i formidlingen af disse antimikrobielle resistensgener til andre commensal og indfødte mikrobielle samfund i jord. Imidlertid er der behov for yderligere længerevarende undersøgelser udført flere steder for at understøtte denne hypotese .
en anden forskning concering C. freundii blev udført for at udtænke en polymerasekædereaktion (PCR) metode, der samtidig bruger tre par specifikke primere til at detektere gener af visse mikrober (inklusive C. freundii). Metoden omfattede design af tre primerpar, som var: SPVC-1 og SPVC-2, INVA-1 og INVA-2; og VIAB-1 og viaB-2. PCR blev udført under anvendelse af disse tre primere til at identificere 14 klinisk vigtige bakterielle organismer. Følgende stammer blev hurtigt identificeret ved hjælp af PCR: (1) C. freundii; (2) S. Typhi; og S. Paratyphi C; (3) S. Dublin (virulensantigenpositiv); og (4) Salmonella serovarer, der har et SPV-virulensplasmid. Selvom denne PCR-metode er ny, kan denne metode med teknologiens fremskridt i fremtiden muliggøre identifikation af C. freundii hos pattedyr med det samme, så passende antibiotikabehandling kan påbegyndes uden forsinkelse .
en tredje undersøgelse concering C. freundii blev udført på universitetet i Barcelona, Spanien. Mekanismerne for resistens over for fluorokinoloner i to Citrobacter freundii-stammer blev undersøgt. Begge stammer blev isoleret fra den samme patient. Denne undersøgelse tillod delvis karakterisering af acrA-og acrB-generne af denne mikroorganisme. Ekspression af gener i begge stammer blev analyseret ved anvendelse af DNA-mikroarrays til Escherichia coli. Nukleotids lighed mellem de delvist sekventerede Acra-og acrB-gener af C. freundii og E. coli var henholdsvis 80,7% og 85%. Acra-og acrB-generne af C. freundii ligner dem i E. coli og deres overekspression kan spille en vigtig rolle i moduleringen af den endelige minimale inhiberende koncentration af fluorokinoloner .
en fjerde undersøgelse vedrørende C. freundii blev udført i Danmark. Et team af forskere isolerede en diabetespatient, der udviklede nekrotiserende fasciitis, som var forårsaget af C. freundii fra en skade, der blev ansporet af et havdyr. Nekrotiserende fasciitis er en infektion i det dybere lag af huden og subkutane væv. Ved behandling af patienten tog de en prøve fra væsken i såret og fandt C. freundii. Efter tre dages start af antibiotikabehandlingen med cefotaksin og cefepmin var der ophobning af subkutane abscesser. Efter 6, 10, 14 og 21 dages pleje af patienten gav nogle antibiotika patienten en vis lettelse, men der blev ikke nået nogen langsigtet bedring. Blandt de antibiotika, der ikke matchede C. freundii. Patienten kom sig fuldt ud efter 42 dages ertapenem-behandling. Forskerne havde isoleret to kolonier af C. freundii inden for 5 dage efter hinanden. Da isolaterne blev dyrket, blev de uhyre modstandsdygtige over for cefotaksime og cefepime. Årsagen til, at entrapenem arbejdede mod C. freundii, er fordi er aktiv mod AmpC-producerende Enterobacteriaceae .
antibiotikaresistens
Citrobacter-arter er en almindelig årsag til nosokomiale infektioner forbundet med patienter, der gennemgår langvarige hospitalsbehandlinger. C. freundii er for nylig blevet rapporteret at udtrykke resistens over for bredspektret antibiotincs, herunder piperacillin, vancomycin og cephalosporiner. Det er en af de mest almindelige typer antibiotika, der anvendes til behandling af antibiotika. De nye nye CRCF-stammer kunne antyde induktion eller depression af resistensgener samt eliminering af konkurrerende organismer. CRCF er for det meste isoleret fra patienter med signifikante comorbiditeter inklusive AIDS, perifer vaskulær sygdom og cerebrovaskulær sygdom. Brugen af fluorokinolon er også rapporteret at have nogen indflydelse mod isolering af CRCF .Citrobacter freundii er også kendt for at indeholde et gen, der koder for cephalosporinase i sit kromosom. Dette hydrolyserer −CO−NH− binding i lactamringen af cephalosporiner og cephamycis, hvilket gør bakterierne resistente over for denne type antibiotika. Men når de blev udsat for nye tredje generation cephems og cerbapenems, klinisk isoleret C. freundii viste følsomhed over for disse stoffer.Et lille udbrud af C. freundii resistent over for tredje generation cephems er blevet observeret i kirurgisk afdeling på Nagoya Universitetshospital hos patienter, der gennemgik kirurgiske procedurer. C. freundii blev isoleret fra patientens galde, sårgas, afføring, pus og ascites. Det blev foreslået, at disse nye stammer af C. freundii indeholdt et plasmid, der koder for AmpC celphalosporinase, men ved manglende overførsel af cephems-resistens fra C. freundii til E. coli blev det konkluderet, at det skal kodes i kromosomet af C. freundii. Da C. freundi er forbundet med nosokomielle infektioner, anbefales det at være forsigtig med disse nye stammer .
1. JT, Chang SC, Chen YC, Luh KT. “Sammenligning af antimikrobiel modtagelighed af Citrobacter freundii isolater i to forskellige tidsperioder.”Journal of Microbiology, Immunology and Infection. 2000 Dec; 33 (4): 258-62.
2. Hvalen JG, Mully TV, Enlgish JC 3rd. “Spontan Citrobacter freundii-infektion hos en immunkompetent patient.”Arkiv for dermatologi. 2007 Jan; 143(1): 124-5.
3. Puchenkova SG. “Enterobakterier i områder med vand langs Krim-kysten.”Mikrobiolohichny. 1996 Mar-Apr; 58 (2): 3-7.
4.http://www.ncbi.nlm.nih.gov/sites/entrez?db=genomeprj&cmd=Retrieve&dopt=Overview&list_uids=13123
5. Ilya V. Manukhov, Daria V. Mamaeva, Sergei M. Han er en af de mest kendte og mest kendte mennesker i verden. “Et gen, der koder for L-methionin-l-Lyase, er til stede i Enterobacteriaceae-Familiegenomer: identifikation og karakterisering af Citrobacter freundii L-methionin-l-Lyase.”Journal of Bacteriology. 2005 juni; 187 (11): 3889-3893.
6. Lindberg, Frederik; Lennart; Normark, Staffan. “Regulatoriske komponenter i Citrobacter freundii ampC Kurt-lactamase induktion.”Proceedings of the National Academy of Sciences i Amerikas Forenede Stater. 1985 Juli; 82 (14): 4620-4624.
7. Tsukamoto K, Tachibana K, Yamasaki N, Ishii Y, Ujiie K, Nishida N, Savai T. “lysin-67′ s rolle i det aktive sted for klasse C beta-lactamase fra Citrobacter freundii GN346.”European Journal of Biochemistry / FEBS. 1990 Februar 22; 188 (1): 15-22.
8. Keevil, Hough JS, Cole JA. “Prototrofisk vækst af Citrobacter freundii og det biokemiske grundlag for dets tilsyneladende vækstkrav i luftede medier.”Tidsskrift for generel mikrobiologi. 1997 Jan; 98 (1): 273-6.
9. Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur Dur A. “Fatal Citrobacter Freundii bronchopneumoni erhvervet i samfundet hos en kompromisløs Patient.”Revista Cl Kurtnica Espa Kurtola. 1985 April; 176 (6): 320
10. Julie L. Badger, Monika F. Stins og Kim. “Citrobacter freundii invaderer og replikerer i humane hjerne mikrovaskulære endotelceller.”Hinyokika kiyo. Acta Urologica Japonica. 1985 Juli; 31 (7): 1159-70.
11. Drelichman V, Band JD. “Bakteriemier på grund af Citrobacter diversus og Citrobacter freundii. Incidens, risikofaktorer og klinisk resultat.”Arkiv for Intern Medicin. 1985 okt; 145 (10): 1808-10.
12. Srinivasan V, Nam HM, savet AA, Headrick SI, Nguyen LT, Oliver SP. “Distribution af tetracyclin-og Streptomycinresistensgener og klasse 1-Integroner i Enterobacteriaceae isoleret fra mejeri-og ikke-Mejerijord.”Mikrobiel Økologi. 2007 August 15.
13. “Delvis karakterisering af acrAB locus i to Citrobacter freundii kliniske isolater.”International Journal of antimikrobielle midler. 2007 Sep; 30 (3): 259-63.
14. Ci corrci IH, Korcan SE, Konuk M, okt Korrk S. “Sammenligning af ALAD-aktiviteter af Citrobacter-og Pseudomonas-stammer og deres anvendelse som biomarkør for PB-forurening.”Miljøovervågning og-vurdering. 2007 22.maj.
15. “Oprensning og karakterisering af selenocystein beta-lyase fra Citrobacter freundii.”Tidsskrift for bakteriologi. 1985 August; 163 (2): 669-76.
16. Hillel S Levinson, Inga Mahler. “Fosfataseaktivitet og blyresistens i Citrobacter freundii og Staphylococcus aureus.”FEMS Mikrobiologi breve. 1998 April; 161 (1): 135-138.
17. Murakami K, Yoshida T. ” kovalent binding af moksalaktam til cephalosporinase af Citrobacter freundii.”Antimikrobielle midler og kemoterapi. 1985 maj; 27 (5): 727-32.
18. “Citrobacter Freundii peritonitis og tunnel infektion hos en patient på kontinuerlig ambulant peritonealdialyse.”Tidsskrift for Medicinsk Mikrobiologi, 2008. Bind 57. s. 125-127.
19. Jørgen Jørgensen, Jørgen Jørgensen, Jørgen Jørgensen, Jørgensen EN. “Epidemiologiske risikofaktorer for isolering af ceftriaksonresistent versus modtagelig citrobacter freundii hos indlagte patienter” Antimicrob-midler Chemother, 2003 Sep;47(9): s.2882-2887.
20. “Et lille udbrud af tredje generation cephem-resistent Citrobacter freundii infektion på en kirurgisk afdeling” Jpn J inficerer Dis. 2004 Aug;57 (4): s.181-182.
21. Chuang, Y., Tseng,S., Teng, L., Ho, Y. og Hsueh, P. “Fremkomsten af cefotaksimal resistens i Citrobactor freundii forårsager nekrotiserende fasciitis og osteomyelitis” Journal of Infection, 2006. Bind 53. s. e161-e163.
22.Badger, J., Stins, M. og Sik Kim, K.” Citrobacter freundii invaderer og replikerer i humane Hjernemikrovaskulære endotelceller ” infektion og immunitet, 1999. Volume67. P. 4208-4215.det er en af de mest populære og mest populære måder at gøre det på, og det er en af de bedste måder at gøre det på.
redigeret af Sumaira Akbarsada ,studerende ved Rachel LarsenEdited af Greg Vargas og Darren en, studerende ved M Glogovskiat Loyola Universitetredigeret af Gergana Grigorova og Michal Olsevski, studerende ved M Glogovskiat Loyola Universitetredigeret af Aleks Kula og Joanna Aiken, studerende ved M Glogovskiat Loyola University