A Microbial Biorealm page on the genus Citrobacter freundii
Classification
Higher order taxa
Bacteria; Proteobacteria; Gammaproteobacteria; Enterobacteriales; Enterobacteriaceae; Citrobacter
Species
NCBI: Taxonomy
Citrobacter Freundii
Description and significance
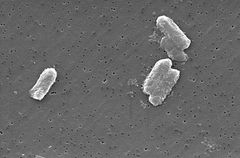 Photo: Pete Wardell/CDC
Photo: Pete Wardell/CDC
Citrobacter-artene, inkludert Citrobacter freundii, er aerobe gram-negative baciller. Citrobacter freundii er lange stavformede bakterier som vanligvis er 1-5 µ i lengde . De Fleste c. freundii-celler er omgitt av mange flagella som brukes til å bevege seg, men noen er ikke-motile. Dens habitat inkluderer miljøet (jord, vann, kloakk), mat og tarmkanaler av dyr og mennesker . Det tilhører Familien Av Enterobacteriaceae.
Som et opportunistisk patogen er c. freundii ansvarlig for en rekke signifikante opportunistiske infeksjoner. Det er kjent for å være årsaken til en rekke nosokomiale infeksjoner i luftveiene, urinveiene, blodet og flere andre normalt sterile steder hos pasienter . C. freundii representerer omtrent 29% av alle opportunistiske infeksjoner . Derfor er en av hovedgrunnene til at mange forskjellige stammer og plasmider av c. freundii-genomet blir sekvensert, for å finne antibiotika som kan bekjempe disse opportunistiske infeksjonene.Overraskende nok spiller denne smittsomme mikroben hos mennesker en positiv rolle i miljøet. C. freundii er ansvarlig for å redusere nitrat til nitritt i miljøet . Denne avgjørende konvertering er et viktig stadium i nitrogen syklusen. Og gjenvinning av nitrogen er svært viktig fordi jordens atmosfære er ca 85% nitrogen . På grunn av sitt viktige bidrag til miljøet er det derfor en annen motivasjon for sekvensering av genomet Av c. freundii.Citrobacter-slekten ble oppdaget i 1932 av Werkman og Gillen. Kulturer av c. freundii ble isolert og identifisert i samme år fra jordekstrakter .
Genomstruktur
ingen informasjon om det komplette genomet Av c. freundii er tilgjengelig online, selv om enkelte individuelle stammer og plasmider av mikroben har blitt sekvensert. Den mest fremtredende er plasmidet pCTX-M # 3 fordi det er det største plasmidet og koder for en stor mengde proteiner. Sekvensen ble fullført 6. januar 2005. DET er et sirkulært DNA plasmid og det er 89,468 nukleotid base par lang. Lengden på plasmidet er 0,089468 (Mbp). DEN består av 51,0% GC-innhold, og koder for 105 proteiner .
Et annet viktig trekk Ved C. freundii-genomet er at det er Den eneste mikroben I Enterobacteriaceae-familien som inneholder et plasmid som koder For L-metionin γ-lyase (MGL). Nukleotidsekvensen av plasmidet inneholder en 3000 bp Lang EcoRI-innsats . Fragmentet inneholder også to åpne leserammer. Den første rammen består av 1.194 nukleotider, og den andre, 1.296 nukleotider.Den første rammen, kjent som megL-genet, koder for et protein av 398 aminosyrerester som har sekvenshomologi med MGLs fra forskjellige kilder. Den andre rammen koder for et protein med sekvenshomologi med proteiner som tilhører familien av permeases .
c. freundii OS60 AmpC β-laktamase-genet er også sekvensert og består av 1197 nukleotider. Den koder for en 380 aminosyre lang forløper og inneholder et 19 restsignalpeptid i 5 ‘ enden. Dette genet koder for et modent protein som har en molekylvekt på 39 781 Dalton. Aminosyreposisjonene i denne forløperen er overraskende identiske med rester i e. coli K12 kromosomale AmpC β-laktamaser .
En annen viktig stamme I genomet Av C. freunii ER GN346, som er et klinisk isolat gjenvunnet i 1965. Denne stammen produserer enzymet cephalosporinase, som har evnen til å hydrolysere og inaktivere anibitoics cefalosporiner og cephamyciner . De strukturelle og promotor regionene av cephalosporinase genet er 1408 nukleotider lange. Aminosyresekvensen av det modne enzymet, består av 361 aminosyrer med en molekylvekt på 39,878 Da .
Cellestruktur og metabolisme
cellestrukturen Til c. freundi er lang og stangformet vanligvis 1-5 µ i lengde. Utsiden av cellen inneholder mange flagella som brukes til motalitet . Siden c. freundii er gram-negative bakterier, inneholder den to membraner (indre og ytre).Det periplasmiske rommet ligger mellom de to membranene. Den ytre membranen inneholder ikke en energikilde; men den inneholder mange poriner innebygd i det som hjelper organismen til å skaffe viktige ioner . I motsetning til gram-positive bakterier inneholder c. freundii-celler ikke en tykk cellevegg som består av peptidoglykan. for metabolisme har c. freundii en fantastisk evne til å vokse på glyserol som eneste karbon-og energikilde. I denne prosessen blir glyserol gjæret ved en dismutasjonsprosess. Denne prosessen krever to veier . I den første veien blir glyserol dehydrogenert AV EN NAD1-bundet glyseroldehydrogenase til dihydroksyaceton. Dihydroksyaceton blir deretter fosforylert og kanalisert til glykolyse av dihydroksyaceton kinase . I den andre veien dehydreres glyserol av koenzym B12-avhengig glyseroldehydratase for å danne 3-hydroksypropionaldehyd . Dette produktet er redusert til det store fermenteringsproduktet 1,3-propandiol av NADH-bundet 1,3-propandiol dehydrogenase, som regenererer NAD1. Dha regulon koder for de fire essensielle enzymene i disse to veiene. Utrolig, uttrykket av dha regulon er bare indusert når glyserol er tilstede . Celler Av c. freundii kan også metabolisere laktose eller citrat som karbonkilde .
Økologi
Citrobacter freundii finnes ofte i miljøet, hovedsakelig i jord, vann og kloakk. De er en indikator på potensiell forurensning av vann. De finnes også på forskjellige organer av syke dyr, inkludert pattedyr, fugler, reptiler og amfibier . De er ikke kjent for å samhandle med andre organims. i miljøet kan c. freundii konvertere nitrat eller ammoniumionet (som er et nitrogenatom kombinert med fire hydrogenatomer) til nitritt; denne reaksjonen skjer i miljøet så vel som i fordøyelseskanalen hos mennesker og andre dyr . Etter at det konverterer nitrat til nitritt i miljøet, blir nitritt omdannet til nitrogen, og dette siste trinnet fullfører nitrogen syklusen i jordens atmosfære, som består av 85% nitrogen . Denne organismens økologiske rolle inkluderer ikke bare dens viktige rolle i nitrogen-syklusen, fordi den også kan akkumulere uran (som er det grunnleggende materialet for atomteknologi) ved å bygge fosfatkomplekser .
Citrobacter freundii har også blitt undersøkt for bionedbrytning av garvesyre som brukes i tannerys .
Patologi
Som et opportunistisk patogen er Citrobacter freundii ofte årsaken til signifikante opportunistiske infeksjoner, noe som betyr at Det generelt ikke forårsaker sykdom hos friske menneskelige verter. De påvirker bare pasienter med svakt immunsystem, noe som betyr at de trenger en «mulighet» til å infisere personen . Derfor, hos pasienter med undertrykt immunsystem, Er Citrobacterarter kjent for å forårsake et bredt utvalg av nosokomiale infeksjoner i luftveiene, urinveiene og blodet . Hepatisk, biliær og bukspyttkjertel sykdom er også vanlige sykdommer som er forårsaket Av c. freundii. Galleveiene er det vanligste stedet for infeksjon Av c. freundii baciller .En dødelig sykdom Som c. freundii har vært assosiert med, er neonatal meningitt. Neonatal meningitt er betennelse i hjernehinnene (systemet av membraner som omgir CNS) på grunn av bakteriell invasjon . Dødeligheten Av citrobacter meningitt er uakseptabelt høy, med dødsfall av pasienter som varierer fra 25 til 50 %. Videre fortsetter alvorlige nevrologiske problemer hos 75% av overlevende. I denne sykdommen er Citrobacter freundii i stand til å trenge inn i blod-hjernebarrieren som består av choroid plexus epitel og hjernekapillær endotel .
Tester utført Av Badger et. al i artikkelen «Citrobacter freundii Invaderer Og Replikerer I Menneskelige Hjerne Mikrovaskulære Endotelceller» antyder at bakteriell spredning Av c. freundii foregår på intracellulært nivå, som hadde vært i strid med den generelle vitenskapelige tanken. Funnene indikerer At c. freundii krysser vakuoler, replikerer og slippes ut i den basolaterale siden av de menneskelige hjernens mikrovaskulære endotelceller (HBMEC) for å krysse blod-hjernebarrieren. Videre analyse kan potensielt tillate terapeutiske strategier for å behandle infeksjoner. Det er fortsatt ingen terapeutisk behandling tilgjengelig .Visse sykdommer studert i ørret og cyprinids er også forårsaket Av c. freundii. C. freundii forårsaker unormale inflammatoriske forandringer i tarm av ørret og inflammatoriske og nekrotiske forandringer i indre organer av cyprinider. Sykdommen ble oppdaget ved hjelp av kunstig infeksjon med en ren kultur Av c. freundii. Denne oppdagelsen etablerte c. freundii som en årsak til fiskesykdom .I En casestudie av Journal Of Medical Microbiology utviklet en pasient peritonitt og tunnelinfeksjon på Grunn Av Citrobacter freundii, noe som er uvanlig. Pasienten var på kontinuerlig ambulatorisk peritonealdialyse. Vanligvis forårsaker agenter er gram-positive mikroorganismer, spesielt Staphylococcus aureus og Staphyloccus edpidermis. Det er heller ingen kjente rapporter om tunnelinfeksjon på Grunn Av c. freundii. Initial antibiotikabehandling virket ikke, og infeksjonen fortsatte å fortsette til kateteret ble fjernet. Dette er klinisk signifikant fordi Citrobacter Freundii viser forskjellig antibiotikaresistens, og derfor var initial terapi ikke vellykket. Pasienten responderte ikke på behandling før kateteret ble fjernet, og viste At Citrobacter freundii er opportunistiske patogener som påvirker sykehus og immunkompromitterte pasienter .
Søknad Til Bioteknologi
I Bioteknologiindustrien produserer Citrobacter freundii mange viktige enzymer.De første enzymer det produserer er fosfatase. Fosfataseaktivitet Av C. freundii har blitt postulert å være involvert i blyakkumulering, som kan ha spilt en viktig rolle i Bioteknologibransjen. Fosfataseaktiviteten Til c. freundii har også blitt oppdaget å ha motstand mot noen diagnostiske reagenser .rensingen og karakteriseringen av bakteriell selenocystein beta-lyase, et enzym som spesifikt katalyserer spaltningen Av L-selenocystein Til L-alanin, har blitt renset Fra Citrobacter freundii. Enzymet er monomert med en molekylvekt på ca. 64 000 og inneholder 1 mol pyridoksal 5 ‘ – fosfat som en kofaktor per mol av enzym. Enzymet katalyserer også alfa, beta eliminering av beta-klor-L-alanin for å danne NH3, pyruvat .
C. Freundii-stammer bærer også et plasmid som koder for klasse 1 AmpC cefalosporinase. Disse enzymene kan hydrolzye inaktivere nye cephamyciner og cephalosporiner .
Nåværende Forskning
en liten skala forskning om visse stammer Av c. freundii ble gjort nylig ved University Of Tennessee, Knoxville. Betydningen av visse tetracyklin-og streptomycin-resistensgener og klasse 1-integroner i C. freundii isolert fra meieri gård jord og nondairy jord ble evaluert. En stamme Av c. freundii ekstrahert fra meieri gård jord gjennomført klasse 1 integroner med forskjellige innsatte genet kassetter. Resultatene av denne lille studien antydet at tilstedeværelsen av flere resistensgener og klasse 1-integroner I C. freundii i melkebedriftsjord kan fungere som et reservoar av antimikrobielle resistensgener og kunne spille en rolle i spredning av disse antimikrobielle resistensgener til andre kommensale og innfødte mikrobielle samfunn i jord. Imidlertid er det behov for flere langsiktige studier utført på flere steder for å støtte denne hypotesen .en annen forskning concering c. freundii ble gjort For å utarbeide en polymerase chain reaction (PCR) metode som samtidig bruker tre par spesifikke primere for å oppdage gener av visse mikrober (inkludert c. freundii). Metoden inkluderte å designe tre primerpar som var: SPVC-1 OG SPVC-2, INVA – 1 OG INVA-2; OG VIAB-1 OG VIAB-2. PCR ble utført ved hjelp av disse tre primere for å identifisere 14 klinisk viktige bakterielle organismer. Følgende stammer ble raskt identifisert VED HJELP AV PCR: (1) C. freundii; (2) S. Typhi; Og S. Paratyphi C; (3) S. Dublin( virulens antigen-positiv); og (4) Salmonella serovarer som havn en spv-type virulens plasmid. SELV OM DENNE PCR-metoden er ny, kan denne metoden i fremtiden tillate identifisering av C. freundii hos pattedyr umiddelbart, slik at passende antibiotikabehandling kan påbegynnes uten forsinkelse .
en tredje studie concering c. freundii ble gjort Ved Universitetet I Barcelona, Spania. Mekanismene for resistens mot fluorokinoloner i to Citrobacter freundii-stammer ble studert. Begge stammer ble isolert fra samme pasient. Denne studien tillot delvis karakterisering av acrA-og acrB-gener av denne mikroorganismen. Ekspresjon av gener i begge stammer ble analysert VED HJELP AV DNA-mikroarrays For Escherichia coli. Nukleotidlikheten mellom de delvis sekvenserte acrA-og acrB-genene Av c. freundii og E. coli var henholdsvis 80,7% og 85%. Acra og acrB gener Av c. freundii er lik de I E. coli og deres overuttrykk kan spille en viktig rolle i å modulere den endelige minimumshemmende konsentrasjonen av fluorokinoloner .
en fjerde studie om c. freundii ble gjort I Taiwan. Et team av forskere isolerte en diabetespasient som utviklet nekrotiserende fasciitt som ble forårsaket Av c. freundii fra en skade oppmuntret av et marine dyr. Nekrotiserende fasciitt er en infeksjon i det dypere laget av hud og subkutant vev. Ved behandling av pasienten tok de en prøve fra væsken i såret og fant C. freundii. Etter tre dager med å starte antibiotikabehandlinger med cefotaxmin og cefepmin, var det opphopning av subkutane abscesser. Etter 6, 10, 14 og 21 dager med å ta vare på pasienten, ga noen antibiotika pasienten litt lettelse, men ingen langsiktig utvinning ble nådd. Cefotoaxime, cefepime, ciprofloxamin er blant antibiotika som ikke var noen kamp For c. freundii. Pasienten ble helt frisk etter 42 dagers behandling med ertapenem. Forskerne hadde isolert to kolonier Av c. freundii innen 5 dager av hverandre. Etter hvert som isolatene ble dyrket, ble de umåtelig resistente mot cefotaxim og cefepim. Grunnen til at entrapenem jobbet mot c. freundii er fordi er aktiv mot AmpC produsere Enterobacteriaceae .
Antibiotikaresistens
Citrobacterarter er en vanlig årsak til nosokomiale infeksjoner assosiert med pasienter som gjennomgår langvarig sykehusbehandling. C. freundii har nylig blitt rapportert å uttrykke resistens mot bredspektret antibiotinc, inkludert piperacillin, piperacillintazobaktam, vancomycin og cefalosporiner. Isolering av ceftriaxonresistent Citrobacter freundii (CRCF) har vært assosiert med overforeskrevet bredspektret antibiotika. De nye CRCF-stammene kan foreslå induksjon eller depresjon av resistensgener, samt eliminering av konkurrerende organismer. CRCF er for det meste isolert fra pasienter med signifikante komorbiditeter, inkludert AIDS, perifer vaskulær sykdom og cerebrovaskulær sykdom. Bruken av fluorokinolon har også blitt rapportert å ikke ha noen innvirkning på isoleringen AV CRCF .Citrobacter freundii er også kjent for å inneholde i sitt kromosom et gen som koder for cefalosporinase. Dette enzymet hydrolyserer-CO-NH-bindingen i laktamringen av cefalosporiner og cephamycis gjør dermed bakteriene resistente mot denne typen antibiotika. Men når de utsettes for nye tredje generasjon cephems og cerbapenems, klinisk isolert c. freundii viste følsomhet for disse stoffene.Et lite utbrudd Av c. freundii resistent mot tredje generasjons cephems har blitt observert i kirurgisk avdeling Av Nagoya Universitetssykehus hos pasienter som gjennomgikk kirurgiske prosedyrer. C. freundii ble isolert fra pasientens galle, sårgass, avføring, pus og ascites. Det ble foreslått at disse nye stammer Av c. freundii inneholdt et plasmid koding AmpC celphalosporinase men ved unnlatelse av å overføre cephems motstand Fra c. freundii Til E. coli ble det konkludert med at enzymet må kodes i kromosomet Av c. freundii. Siden c. freundi er assosiert med nosokomiale infeksjoner, anbefales forsiktighet til disse nye stammene .
1. Wang JT, Chang SC, Chen YC, Luh KT. «Sammenligning av antimikrobiell følsomhet Av Citrobacter freundii isolerer i to forskjellige tidsperioder.»Journal Of Mikrobiologi, Immunologi Og Infeksjon. 2000 Desember; 33 (4): 258-62.
2. Whalen JG, Mully TW, Enlgish JC 3rd. «Spontan Citrobacter freundii infeksjon i en immunkompetent pasient.»Arkiv av dermatologi. 2007 Jan; 143(1): 124-5.
3. Puchenkova SG. «Enterobakterier i områder med vann langs Krim-Kysten.»Mikrobiolohichnyĭ zhurnal. 1996 Mar-April; 58 (2): 3-7.
4.http://www.ncbi.nlm.nih.gov/sites/entrez?db=genomeprj&cmd=Retrieve&dopt=Overview&list_uids=13123
5. A. V. M. M., A. V. M. M. Han ble født i moskva, og ble født i moskva. «Et Gen Som Koder For L-Metionin γ-Lyase Er Tilstede I Enterobacteriaceae Familiegenomer: Identifikasjon Og Karakterisering Av Citrobacter freundii L-Metionin γ-Lyase.»Journal Of Bacteriology. 2005 juni; 187 (11): 3889-3893.
6. Lindberg, Frederik; Westman, Lennart; Normark, Staffan. «Regulatoriske Komponenter I Citrobacter freundii ampC β-laktamase Induksjon.»Proceedings Av National Academy Of Sciences I Usa. 1985 juli; 82 (14): 4620-4624.
7. Tsukamoto K, Tachibana K, Yamazaki N, Ishii Y, Ujiie K, Nishida N, Sawai T. «Rolle av lysin-67 i det aktive stedet for klasse c beta-laktamase Fra Citrobacter freundii GN346.»European Journal Of Biochemistry / FEBS. 1990 Februar 22; 188(1): 15-22.
8. Keevil CW, Hough JS, Cole JA. «Prototrofisk vekst Av Citrobacter freundii og det biokjemiske grunnlaget for dets tilsynelatende vekstkrav i luftet media.»Journal Of General Microbiology. 1997 Jan; 98(1): 273-6.
9. Marco S Hryvnchez F, Turabian Fern Hryvndez JL, Dur@nn Pé-Navarro A. «Fatal Citrobacter Freundii Bronkopneumoni Ervervet I Samfunnet I En Kompromissløs Pasient.»Revista Cl@nica Espa Hryvola. 1985 April; 176 (6): 320
10. I tillegg til å være en av de mest populære. «Citrobacter freundii Invaderer og Replikerer I Menneskelige Hjerne Mikrovaskulære Endotelceller.»Hinyokika kiyo. Acta Urologica Japonica. 1985 Juli; 31 (7): 1159-70.
11. Drelichman V, Band JD. «Bacteremias på Grunn Av Citrobacter diversus og Citrobacter freundii. Forekomst, risikofaktorer og klinisk utfall.»Arkiv For Internmedisin. 1985 Oktober; 145 (10): 1808-10.
12. A. v., Nam HM, Sawant AA, Headrick SI, Nguyen LT, Oliver SP. «Distribusjon Av Tetracyklin Og Streptomycin Resistensgener Og Klasse 1 Integroner I Enterobacteriaceae Isolert Fra Meieri Og Nondairy Gård Jord.»Mikrobiell Økologi. 2007 August 15.
13. Sá-Cé J, Vila J. » Delvis karakterisering av acrAB-lokusen i to Kliniske isolater Av Citrobacter freundii.»Internasjonal Tidsskrift For Antimikrobielle Midler. 2007 September; 30 (3): 259-63.
14. Ciğ ih, Korcan SE, Konuk M, Oztü «Sammenligning AV alad-aktiviteter Av Citrobacter – og Pseudomonas-stammer og deres bruk som biomarkør for pb-forurensning.»Miljøovervåking Og Vurdering. 2007 22.Mai.
15. Chocat P, Esaki N, Tanizawa K, Nakamura K, Tanaka H, Soda K. » Rensing og karakterisering av selenocystein beta-lyase Fra Citrobacter freundii .»Journal Of Bacteriology. 1985 August; 163 (2): 669-76.
16. Hillel S Levinson, Inga Mahler. «Fosfataseaktivitet og blyresistens I Citrobacter freundii og Staphylococcus aureus.»FEMS Mikrobiologi Bokstaver. 1998 April; 161 (1): 135-138.
17. Murakami K, Yoshida T. «Kovalent binding av moxalactam til cephalosporinase Av Citrobacter freundii.»Antimikrobielle Midler Og Kjemoterapi. 1985 Mai; 27 (5): 727-32.
18. Dervisoglu, E., Yegenaga, I., Yumuk, Z. » Citrobacter Freundii peritonitt og tunnelinfeksjon hos en pasient på kontinuerlig ambulatorisk peritonealdialyse .»Journal Of Medical Microbiology, 2008. Volum 57. s. 125-127.
19. Kim PW, Harris AD, Roghmann MC, Morris Jg Jr, Strinivasan A, Perencevich EN. «Epidemiologiske risikofaktorer for isolering av ceftriaxonresistent versus-mottakelig citrobacter freundii hos pasienter på sykehus» Antimikrobmidler Chemother, 2003 September;47 (9): p.2882-2887.
20. Nada T, Baba H, Kawamura K, Ohkura T, Torii K, Ohta M. «et lite utbrudd av tredje generasjon cephem-resistente Citrobacter freundii infeksjon på en kirurgisk avdeling» Jpn J Infisere Dis. 2004 August; 57 (4): p. 181-182.
21. A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A. «Fremveksten av cefotaksimresistens I Citrobactor freundii forårsaker nekrotiserende fasciitt og osteomyelitt» Journal Of Infection, 2006. Volum 53. p. e161-e163.
22.Badger, J., Stins, M., Og Sik Kim, K. «Citrobacter freundii Invaderer Og Replikerer I Menneskelige Hjernemikrovaskulære Endotelceller» Infeksjon og Immunitet, 1999. Volum67. S. 4208-4215.
Redigert Av Sumaira Akbarzada, Student Av Rachel Larsenredigert Av Greg Vargas Og Darren Zhen, studenter Av M Glogowskiat Loyola Universityredigert av Gergana Grigorova og Michal Olszewski, studenter Av M Glogowskiat Loyola Universityredigert Av Alex Kula og Joanna Aiken, studenter Av M Glogowskiat Loyola University